Radiologia Brasileira - Publicação Científica Oficial do Colégio Brasileiro de Radiologia
AMB - Associação Médica Brasileira CNA - Comissão Nacional de Acreditação
 Vol. 42 nº 4 - Jul. / Ago. of 2009
Vol. 42 nº 4 - Jul. / Ago. of 2009
|
ARTIGO ORIGINAL
|
|
|
|
|
Autho(rs): Samuel Martins Moreira, Antonio Massamitsu Kambara, Sergio Ajzen, José de Ribamar Costa Junior |
|
|
Descritores: Stent, Artéria ilíaca, Ultrassonografia de intervenção, Hiperplasia |
|
|
Resumo: >
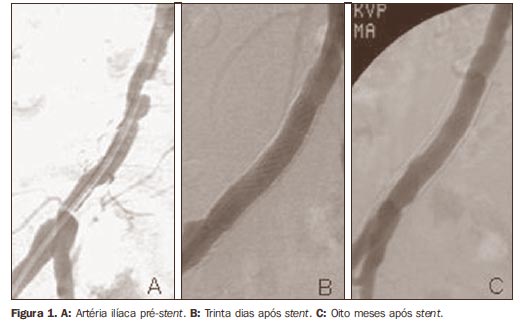
INTRODUÇÃO A angioplastia transluminal percutânea com uso de suporte intravascular metálico (stent) para tratar lesões obstrutivas das artérias ilíacas é um método de tratamento seguro e eficaz(1-3), sendo aceito como a primeira escolha de tratamento em casos selecionados(4-6). A reestenose intra-stent causada pela hiperplasia neointimal tem seu pico de ocorrência em torno do sexto mês após o procedimento (Figura 1), já foi descrita em outros territórios (por exemplo, as artérias coronárias(7-9)), porém esta ocorrência não tem sido relatada com a mesma frequência nas artérias ilíacas.
No presente estudo, foi utilizada ultrassonografia intravascular (intravascular ultrasound - IVUS) para quantificar o volume da hiperplasia neointimal em artérias ilíacas tratadas com angioplastia transluminal percutânea e stent, correlacionando com fatores clínicos causais como tabagismo, hipertensão arterial, hiperlipidemia e diabetes mellitus, com o material dos stents utilizados e fatores arteriais locais como o tipo da obstrução.
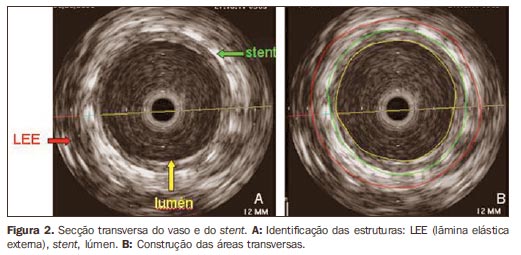
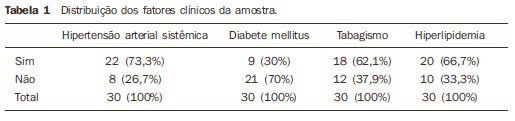
MATERIAIS E MÉTODOS De junho de 2003 a agosto de 2005, 60 pacientes foram submetidos a angioplastia transluminal percutânea e implante de stent para tratamento de lesões obstrutivas das artérias ilíacas. Destes, 30 foram reestudados com IVUS (In-Vision Gold®; Volcano Therapeutics, Rancho Cordova, EUA), sendo 16 do sexo masculino (53,3%) e 14 do sexo feminino (46,7%), com idades entre 39 e 78 anos (média de 60,3 anos). Em relação aos fatores clínicos causais, 22 pacientes tinham hipertensão arterial (73,3%), 18 eram tabagistas (62,1%), 20 4 (dor isquêmica de repouso) e 5 (lesão trófica menor). Em relação ao envolvimento arterial pela placa de ateroma, foi usada a classificação do TASC I, sendo os pacientes classificados nos estágios A, B e C(4). Todos os pacientes foram submetidos aos procedimentos em sala de hemodinâmica, com anestesia local com cloridrato de lidocaína a 2% sem vasoconstritor. Preferencialmente, foi utilizada a via femoral retrógrada ipsilateral, seguida da via femoral retrógrada contralateral, e a via axilar como última escolha. Os stents implantados foram 20 autoexpansíveis de nitinol e 10 stents de aço inoxidável expansíveis por balão, com base em critérios da literatura(10). Em 24 artérias havia estenose (80%) e em 6 artérias, oclusão (20%). Foram administrados os seguintes medicamentos: ácido acetilsalicílico, 200 mg/ dia em dose única, com início dois dias antes do procedimento e mantido continuamente por tempo indefinido; cloridrato de ticlopidina, 500 mg/dia divididos em duas tomadas; ou clopidogrel, 75 mg/dia com início dois dias antes e mantido 30 dias após o procedimento(11). Os pacientes foram acompanhados ambulatorialmente com uma semana, um mês, três meses, seis meses e oito meses, quando então era realizado reestudo com IVUS. Os pacientes que concordaram com a pesquisa e que assinaram termo de consentimento livre e esclarecido foram submetidos ao reestudo. Em sala de hemodinâmica, com anestesia local e por via femoral ipsilateral retrógrada, foi inserido introdutor 6F valvulado e foram injetados 5.000 UI de heparina intra-arterial. A seguir, foi introduzido guia 0,014, sendo posicionado distalmente ao stent, na aorta torácica. Por sobre o guia progredia-se um cateter com transdutor de ultrassonografia de 20 MHz na sua extremidade, conectado a um módulo de leitura do IVUS, posicionando-o antes do início do stent. A seguir, o cateter foi conectado a um sistema fixo de tração (Trak Back II®; Volcano Therapeutics, Rancho Cordova, EUA) com velocidade constante de 1 mm/s. As imagens capturadas foram digitalizadas e armazenadas em disco compacto (CD) e analisadas posteriormente em laboratório de análise quantitativa com auxílio do programa Echoplaque® (Indec Systems; Moutain View, EUA). Com a utilização do IVUS foi possível identificar e delimitar a lâmina elástica externa, o stent e o lúmen (Figura 2). Com estas medidas, foi possível calcular as áreas do vaso, do stent e do lúmen a cada milímetro; a seguir, os cálculos dos volumes foram feitos com auxílio de um programa de computador. Subtraindo-se o volume do lúmen do volume do stent, verificou-se o volume da hiperplasia neointimal.
Um modelo de regressão linear foi ajustado para avaliar a correlação entre o percentual de obstrução intra-stent e hipertensão arterial, tabagismo, hiperlipidemia, diabetes mellitus, aço inoxidável, estenose e oclusão(12,13).
RESULTADOS Trinta pacientes realizaram reestudo com IVUS, com, pelo menos, oito meses após implante do stent, e nenhum deles apresentou complicações. Todos os pacientes mantiveram o resultado clínico conseguido com a angioplastia transluminal percutânea e implante de stent, por ocasião do reestudo.
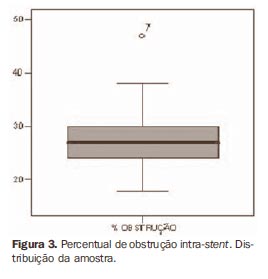
Oito stents foram implantados na artéria ilíaca comum direita, 14 na artéria ilíaca comum esquerda, 5 na ilíaca externa direita e 3 na ilíaca externa esquerda. Foi utilizada a classificação do TASC I para determinar o envolvimento arterial anatômico pela placa de ateroma, e dos 30 pacientes, 4 eram TASC A (13,3%), 15 eram TASC B (50%) e 11, TASC C (36,7%). Em relação ao quadro clínico em que se encontravam os pacientes por ocasião da angioplastia transluminal percutânea e implante de stent, e também para o acompanhamento desses pacientes, foi utilizada a classificação de Rutherford. Com base nessa classificação, nove pacientes (30%) estavam na categoria 5 (lesão trófica menor), nove (30%), na categoria 4 (dor de repouso), nove (30%), na categoria 3 (claudicação severa limitante), e três (10%), na categoria 2 (claudicação moderada), por ocasião da angioplastia transluminal percutânea com stent. No momento do reestudo, 15 pacientes (50%) estavam assintomáticos, 13 apresentavam claudicação para longas distâncias (categoria 1 de Rutherford) e 2 tinham claudicação para moderadas distâncias. A média do volume de hiperplasia neointimal foi de 766,26 mm3 (mínimo de 204 mm3 e máximo de 1.774 mm3). O percentual de obstrução intra-stent causada pela hiperplasia neointimal variou de 18% a 47% (média de 27,4%) (Figura 3).
DISCUSSÃO O reestudo com IVUS demonstrou que, após a angioplastia transluminal percutânea e implante de stent, todos os pacientes desenvolveram hiperplasia neointimal e que esta é uma constante ao tratamento intravascular, porém, nos 30 pacientes deste estudo, ela foi autolimitada e não causou reestenose significativa, sugerindo que em vasos com calibres maiores, como as artérias ilíacas, seria necessária hiperplasia de maior volume para provocar reestenose. Todavia, nos casos em que a reestenose seja significativa, pode ser realizada um nova angioplastia com cateter balão ou cutting balloon, sem uso de um novo stent (14). O uso de IVUS para avaliar a reestenose intra-stent tem-se mostrado superior à angiografia por cateter e à ultrassonografia Doppler transcutânea com transdutores de alta frequência, por conseguir identificar melhor as estruturas e também não subestimar o diâmetro do lúmen(15). A hiperplasia neointimal permanece a principal causa de falência do tratamento intravascular, e muito tem sido realizado para diminuir esta resposta, como o uso de stents com heparina, o uso de anticorpos monoclonais anti-ICAM1(16), que neutralizam a ação facilitadora de adesão molecular da ICAM-1 e, por conseguinte, a hiperplasia neointimal, o uso de probucol(17), que acelera a endotelização dos stents e diminui a formação de hiperplasia, o uso de stents eluídos em drogas que inibem a hiperplasia(18), e mesmo a administração oral de drogas que inibem a hiperplasia neointimal(19). O revestimento com politetrafluoretileno não foi capaz, até o momento, de diminuir a resposta de hiperplasia(20). Estudos comparativos entre o uso primário de stent e o uso de stent em casos selecionados nos quais a angioplastia com cateter balão não obteve bons resultados(21)sugerem que os stents só deveriam ser utilizados nas artérias ilíacas, quando a angioplastia transluminal percutânea com cateter balão apresentar falha. Por outro lado, os materiais usados na composição dos stents utilizados neste estudo - aço inoxidável e nitinol - não mostraram diferenças quanto à hiperplasia neointimal. Os fatores causais - hipertensão arterial, diabetes mellitus, tabagismo e hiperlipidemia - não determinaram diferenças estatisticamente significantes na hiperplasia neointimal e obstrução intra-stent, e também não houve diferença quando havia oclusão arterial ou estenose. Dessa forma, o alto custo das pesquisas, e o preço final dos stents, não se justificam quando as artérias a serem tratadas forem de grosso calibre, como as artérias ilíacas, mesmo que estes pacientes venham a apresentar diabetes mellitus, hipertensão arterial, tabagismo, hiperlipidemias ou oclusões completas dos vasos.
CONCLUSÃO O resultado da análise da regressão linear não demonstrou diferença estatisticamente significante para hipertensão arterial, tabagismo, hiperlipidemia, diabetes mellitus, nitinol, aço inoxidável, estenose e oclusão, quando correlacionada com o percentual de obstrução intra-stent no tratamento de lesões ateroscleróticas das artérias ilíacas.
REFERÊNCIAS 1. Henry M, Amor M, Ethevenot G, et al. Palmaz stent placement in iliac and femoropopliteal arteries: primary and secondary patency in 310 patients with 2-4 year follow-up. Radiology. 1995;197:167-74. [ ] 2. Bosch JL, Hunink MG. Meta-analysis of the results of percutaneous transluminal angioplasty and stent placement for aortoiliac occlusive disease. Radiology. 1997;204:87-96. [ ] 3. De Roeck A, Hendriks JMH, Delrue F, et al. Longterm results of primary stenting for long and complex iliac artery occlusions. Acta Chir Belg. 2006; 106:187-92. [ ] 4. Management of peripheral arterial disease (PAD). TransAtlantic Inter-Society Consensus (TASC). Section C: acute limb ischaemia. Eur J Vasc Endovasc Surg. 2000;19 Suppl A:S115-43. [ ] 5. Norgren L, Hiatt WR, Dormandy JA, et al. Inter-Society Consensus for the Management of Peripheral Arterial Disease (TASC II). Eur J Vasc Endovasc Surg. 2007;34:411-4. [ ] 6. Bosch JL, Tetteroo E, Mali WP, et al. Iliac arterial occlusive disease: cost-effectiveness analysis of stent placement versus percutaneous transluminal angioplasty. Radiology. 1998;208:641-8. [ ] 7. Roubin GS, King SB 3rd, Douglas JS Jr. Restenosis after percutaneous transluminal coronary angioplasty: the Emory University Hospital experience. Am J Cardiol. 1987;60:39B-43B. [ ] 8. Palmaz JC. Intravascular stents: tissue-stent interactions and design considerations. AJR Am J Roentgenol. 1993;160:613-8. [ ] 9. Caramoni PRA, Yamamoto GI, Zago AJ. Reestenose pós-angioplastia. Fisiopatogenia. Arq Bras Cardiol. 1997;69:141-8. [ ] 10. Leung DA, Spinosa DJ, Hagspiel KD, et al. Selection of stents for treating iliac arterial occlusive disease. J Vasc Interv Radiol. 2003;14(2 Pt 1):137-52. [ ] 11. Leon BM, Baim DS, Popma JJ, et al. A clinical trial comparing three antithrombotic-drug regimens after coronary-artery stenting. Stent Anticoagulation Restenosis Study Investigators. N Engl J Med. 1998;339:1665-71. [ ] 12. Siegel S, Castellan NJ Jr. Nonparametric statistics for the behavioral sciences. 2nd ed. New York: McGraw-Hill; 1988. [ ] 13. Neter J, Kutner MH, Nachtsheim CJ, et al. Applied linear statistical models. 4th ed. Chicago: Times Mirror Higher Education Group, Inc.; 1996. [ ] 14. Tsetis D, Belli AM, Morgan R, et al. Preliminary experience with cutting balloon angioplasty for iliac artery in-stent restenosis. J Endovasc Ther. 2008;15:193-202. [ ] 15. Sheikh KH, Davidson CJ, Kisslo KB, et al. Comparison of intravascular ultrasound, external ultrasound and digital angiography for evaluation of peripheral artery dimensions and morphology. Am J Cardiol. 1991;67:817-22. [ ] 16. Kollum M, Hoefer I, Schreiber R, et al. Systemic application of anti-ICAM-1 monoclonal antibodies to prevent restenosis in rabbits: an anti-inflammatory strategy. Coron Artery Dis. 2007;18:117-23. [ ] 17. Tanous D, Bräsen JH, Choy K, et al. Probucol inhibits in-stent thrombosis and neointimal hyperplasia by promoting re-endotelialization. Atherosclerosis. 2006;189:342-9. [ ] 18. Sousa JEMR, Costa MA, Abizaid AC, et al. Lack of neointimal proliferation after implantation of sirolimus-coated stents in human coronary arteries: a quantitative coronary angiography and three-dimensional intravascular ultrasound study. Circulation. 2001;103:192-5. [ ] 19. Waksman R, Pakala R, Baffour R, et al. Optimal dosing and duration of oral everolimus to inhibit in-stent neointimal growth in rabbit iliac arteries. Cardiovasc Revasc Med. 2006;7:179-84. [ ] 20. Dolmatch B, Dong YH, Heeter Z. Evaluation of three polytetrafluoroethylene stent-grafts in a model of neointimal hyperplasia. J Vasc Interv Radiol. 2007;18:527-34. [ ] 21. Klein WM, van der Graaf Y, Seegers J, et al. Dutch iliac stent trial: long-term results in patients randomized for primary or selective stent placement. Radiology. 2005;238:734-44. [ ]
Recebido para publicação em 15/3/2008.
* Trabalho realizado na Universidade Federal de São Paulo/ Escola Paulista de Medicina (Unifesp/EPM), São Paulo, SP, e no Instituto Dante Pazzanese de Cardiologia, São Paulo, SP, Brasil. |
|
Av. Paulista, 37 - 7° andar - Conj. 71 - CEP 01311-902 - São Paulo - SP - Brazil - Phone: (11) 3372-4544 - Fax: (11) 3372-4554