Radiologia Brasileira - Publicação Científica Oficial do Colégio Brasileiro de Radiologia
AMB - Associação Médica Brasileira CNA - Comissão Nacional de Acreditação
 Vol. 42 nº 3 - Maio / Jun. of 2009
Vol. 42 nº 3 - Maio / Jun. of 2009
|
ARTIGO ORIGINAL
|
|
|
|
|
Autho(rs): Marcelo Marcucci, Nitamar Abdala |
|
|
Descritores: Masseter, Esclerose sistêmica, Espectroscopia de próton |
|
|
Resumo:
INTRODUÇÃO A esclerose sistêmica é uma doença inflamatória crônica de origem desconhecida, de natureza autoimune, caracterizada por deposição excessiva de colágeno e glicosaminoglicanos no tecido conjuntivo da derme e dos órgãos internos(1-3). É uma doença de baixa incidência, em média 19 novos casos por milhão de habitantes, com predileção pelo gênero feminino (3:1), e a faixa etária mais atingida encontra-se entre a terceira e quinta décadas de vida(2). A doença apresenta variados aspectos clínicos, sendo usualmente o fenômeno de Raynaud a sua primeira manifestação: espessamento cutâneo(4), dismotilidade esofágica, doença pulmonar restritiva(5-7), hipertensão pulmonar, artralgias, miopatias, miocardiopatia e insuficiência renal progressiva(1-3,8). O envolvimento do sistema musculoesquelético é uma das maiores causas de incapacidade na esclerose sistêmica(9). Frequentemente, são observadas erosões das porções intermediárias e terminais das falanges (acrosteólise), secundárias ao envolvimento cutâneo das extremidades; acomete mais raramente as segunda e quinta costelas, vértebras cervicais, porção distal da clavícula, rádio e ulna(10,11). A esclerose sistêmica apresenta alterações características no complexo maxilomandibular, tais como espessamento do ligamento periodontal e áreas de osteólise na mandíbula. Estas últimas, descritas por Taveras(12) em 1959, são coincidentes com as zonas de inserção dos músculos pterigoideo lateral, temporal, e principalmente, do masseter. Poucos estudos procuraram avaliar o envolvimento do masseter na esclerose sistêmica e sua possível relação com áreas de osteólise mandibular; para tanto, foram empregadas a eletroneuromiografia(13) e a ressonância magnética (RM)(14). Com base em estudos sobre a microvascularização da mandíbula, Ramón et al.(15) propuseram que a osteólise é originada da isquemia muscular resultante da microvasculopatia da esclerose sistêmica. O envolvimento muscular na esclerose sistêmica é provavelmente decorrente de isquemia, que levaria a um aporte insuficiente de oxigênio e nutrientes ao tecido, inflamação ou do próprio processo esclerótico. Assim, a miopatia seria um processo primário da doença e não necessariamente resultante do comprometimento cutâneo sobrejacente(16,17). Estudos sobre a circulação capilar e arteriolar mostram espessamento do lúmen, redução do fluxo, estenose e alterações na arquitetura capilar(18). O objetivo deste estudo foi avaliar a concentração de creatina, colina, lipídio e lactato no masseter em portadores de esclerose sistêmica, por meio da espectroscopia de hidrogênio, e relacionar com a presença de osteólise mandibular.
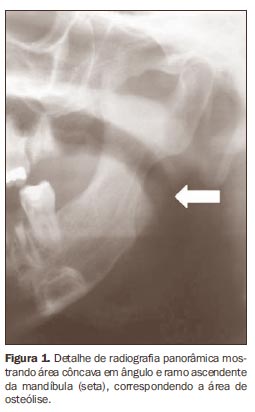
MATERIAIS E MÉTODOS Para este estudo foram selecionados 25 indivíduos de ambos os sexos. Quinze pacientes (idade média de 43,72 ± 7,59 anos) possuíam esclerose sistêmica na forma difusa e 10 indivíduos (idade média de 31,82 ± 12,64 anos) não tinham a doença, estes constituindo o grupo controle. Pacientes que apresentavam esclerose sistêmica na forma limitada ou associada com outras doenças reumáticas foram excluídos. Os 15 pacientes com esclerose sistêmica foram distribuídos em dois grupos: grupo I, comportando sete pacientes com esclerose sistêmica e osteólise mandibular (Figura 1), e grupo II, contendo oito pacientes com esclerose sistêmica sem osteólise mandibular. Os 10 indivíduos saudáveis constituíram o grupo III, controle. O estudo foi aprovado pelo Comitê de Ética em Pesquisa e todos os indivíduos consentiram em participar desta pesquisa.
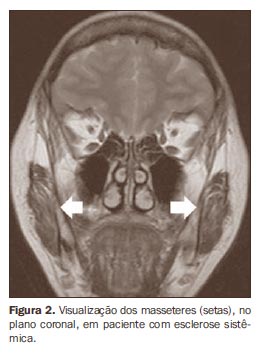
Todos os indivíduos foram submetidos a exame de RM bilateral do masseter (Figura 2), tendo sido utilizado um aparelho Sonata® (Siemens Medical Systems; Erlangen, Alemanha), com campo magnético de 1.5 T e gradiente de 40 mT. A sequência turbo spin-eco (TSE) com relaxamento em T2 foi adquirida no plano coronal, com tempo de repetição (TR) de 2.810 ms, tempo de eco (TE) de 84 ms, número de excitações (NEX) de 2, campo de visão (FOV) de 230 mm e intervalo de 5 mm; a sequência com relaxamento em T1 foi adquirida no plano axial (TR: 479 ms; TE: 13 ms; NEX: 2; FOV: 230 mm; intervalo de 5 mm) com e sem supressão de gordura (TR: 420 ms; TE: 13 ms; NEX: 2; FOV: 230 mm, intervalo de 5 mm). O tempo total de aquisição das imagens foi de 15 minutos e o tempo total de exame foi de 25 minutos.
O exame de espectroscopia por RM (ERM), com sequência PRESS, foi realizado com um único voxel posicionado tridimensionalmente. A região de interesse (ROI) foi representada por um volume cúbico que foi posicionado, visualmente, na região central do músculo, local anatomicamente de maior massa tecidual (Figura 3). Assim, a leitura das frequências foi exclusiva do masseter, não sofrendo interferência dos tecidos circunvizinhos. Nos grupos I e II, foram obtidos valores de ambos os masseteres, enquanto no grupo III a aquisição foi unilateral. Foram registrados apenas os metabólitos que se relacionam com o tecido muscular, com as respectivas escalas de frequência, em partes por milhão: creatina (3,14), colina (3,30), lactato (1,14) e lipídio (1,42). Para a análise estatística das relações entre os metabólitos creatina, colina, lipídio e lactato foi empregada a análise de variância (ANOVA), acompanhada das comparações múltiplas de Bonferroni ou de Tamhane, quando necessário, além do uso das correções de Brown-Forsyth. O nível de rejeição para hipótese de nulidade adotado foi de 0,10 (10%). Foi utilizado, para execução da análise estatística, o software SPSS 11.5.
RESULTADOS Os valores dos metabólitos puros estão relacionados na Tabela 1. A análise dos valores dos metabólitos puros, que podem ser observados na Tabela 2, revelou que não houve diferença significante, entre os três grupos, em relação à creatina e ao lipídio.
Em relação à colina, não houve diferença significante nos pacientes com ou sem osteólise. A concentração de lactato foi me-nor nos pacientes com esclerose sistêmica, com ou sem osteólise, em relação aos indivíduos normais. Os metabólitos foram agrupados em índices, tendo-se encontrado que a creatina/colina, creatina/lactato, lipídio/lactato e colina/lipídio foram diferentes entre os grupos estudados, como pode ser observado na Tabela 3.
DISCUSSÃO A ERM foi desenvolvida no início dos anos 90, como um método não invasivo de avaliação da concentração de metabólitos no interior de variados tecidos, como cérebro, coração e músculos(19). Este método veio auxiliar sobremaneira o estudo metabólico dos músculos faciais, uma vez que, pelos métodos convencionais, havia a necessidade de se realizar biópsia destas regiões, o que trazia grande limitação para este tipo de estudo(20). Optamos por escolher a ERM de hidrogênio (ERM-H), por ser este o átomo mais abundante no organismo, por apresentar maior sensibilidade, maior facilidade de execução e interpretação, e capacidade de investigar um maior número de metabólitos em relação à espectroscopia de fósforo (ERM-31P)(21,22). No presente estudo a creatina foi o componente da cadeia energética avaliado. Ela atua como substrato da creatinaquinase, que transfere o grupo fosfato da molécula de adenosina trifosfato para a creatina, para a produção da fosfocreatina. Esta, por sua vez, é o composto de armazenamento utilizado para a produção de energia durante o trabalho muscular(23). Observamos que os valores da creatina foram estatisticamente iguais nos três grupos, entretanto, um estudo prévio com ERM-H encontrou maior concentração de creatina no masseter de pacientes com disfunção temporomandibular, indicando maior intensidade e/ou frequência das reações bioquímicas necessárias para a manutenção das funções musculares(24). No tecido cerebral os valores de creatina são estáveis em várias doenças(21,23), no entanto, o mesmo não se pode afirmar em relação ao músculo esquelético, uma vez que alguns estudos sobre o metabolismo energético em doenças reumáticas demonstraram resultados variáveis. Empregando a ERM-31P em músculos dos membros inferiores, alguns estudos observaram aumento no índice fosfato inorgânico/fosfocreatina nos pacientes com esclerose sistêmica e polimiosite(15,25), o que indica a presença de doença muscular isquêmica. Por outro lado, estudos por meio da ERM-H mostraram diminuição da concentração de creatina na panturrilha de pacientes com síndrome mialgia-eosinofilia(26) e em pacientes com distrofia muscular de Duchenne(27). Em relação à presença do lactato, os pacientes com esclerose sistêmica mostraram menor concentração em relação aos indivíduos sãos. Por outro lado, em nosso estudo não houve diferença entre os pacientes com e sem osteólise. Estudo in vitro sobre o metabolismo muscular na distrofia muscular de Duchenne demonstrou diminuição do nível do lactato em relação aos indivíduos normais: a diminuição da concentração do lactato indica redução da atividade glicolítica ou mesmo diminuição da sua concentração no músculo(27). Em nosso estudo podemos interpretar este achado supondo que os fenômenos vasculares relacionados à esclerose sistêmica não estão diminuindo a capacidade aeróbica do masseter, pois não estaria havendo o recurso da glicólise anaeróbia (sistema do ácido lático), do mesmo modo que não houve alteração da demanda energética (creatina). Desse modo, esses fenômenos não atuariam significativamente no masseter, ou atuariam de forma parcial, de maneira que a extensa rede vascular do masseter estaria de certa forma suprindo suas necessidades energéticas oxidativas. Sendo assim, ambos os fatores bioquímicos não parecem ter contribuição significativa na gênese da osteólise, segundo nossas observações. O lipídio, da mesma forma que a creatina, não mostrou diferenças significantes entre os grupos estudados. O aumento da sua concentração está relacionado com processos de degradação celular e necrose(21), e seu aumento foi observado no masseter em pacientes com disfunção temporomandibular(24). A colina foi o único metabólito estudado que se mostrou aumentado nos pacientes com osteólise, em relação aos indivíduos normais. O aumento da colina reflete um processo de proliferação celular e evidência de fenômenos de síntese na membrana celular, como aqueles observados em doenças neoplásicas, estando aumentada em relação ao músculo normal(21,28). Por outro lado, sua diminuição pode demonstrar anomalias da membrana, como foi observado em pacientes com distrofia muscular de Duchenne(27). A elevação da colina pode estar relacionada à proliferação celular e/ou ao aumento da sua densidade, e além disto, processos inflamatórios podem também demonstrar picos deste metabólito, resultante da presença de uma grande população de células inflamatórias(28). Sendo assim, a maior concentração de colina nos pacientes com osteólise pode estar relacionada aos mecanismos fisiopatológicos que acometem o fibroblasto na esclerose sistêmica(29) e ao aumento do tecido conjuntivo no epimísio e no perimísio(1). Além disso, observou-se que na esclerose sistêmica a hipóxia tecidual induz à neoangiogênese e que ocorre uma intensa proliferação da camada íntima vascular(30). Portanto, a elevação da colina pode ser o produto dos fenômenos acima descritos, bem como expressar a atividade inflamatória no masseter, sendo que estes fatores poderiam ter participação na gênese da osteólise. Foram avaliados os metabólitos por intermédio de índices para verificar sua atividade em conjunto. Os índices creatina/lipídio e colina/lactato foram estatisticamente os mesmos em todos os grupos. Por outro lado, os demais índices mostraram variações que sugerem significância. Estudos prévios demonstraram que os índices colina/lipídio e creatina/lipídio estão diminuídos em pacientes com polimiosite(26), enquanto nós observamos aumento no primeiro índice e ausência de variação no segundo, nos pacientes com esclerose sistêmica. Do mesmo modo, os pacientes com esclerose sistêmica apresentaram menor índice de creatina/colina e de lipídio/lactato, em relação aos pacientes normais. Em relação ao índice creatina/lactato, apenas os pacientes sem osteólise mostraram diminuição em relação aos normais. Os achados da ERM-H devem ser interpretados com cautela, pois podem ser consequência da interação de fatores como grau de atividade da doença, grau do envolvimento muscular e mesmo sofrer influência de medicamentos usados para controle da doença, como os corticosteroides(22). Por outro lado, este exame mostra alterações bioquímicas mesmo em pacientes sem evidência clínica ou morfológica de alteração muscular(25).
CONCLUSÕES O masseter, nos pacientes com esclerose sistêmica, apresentou menor quantidade de lactato em relação aos indivíduos sadios, enquanto a colina tende a estar aumentada nos pacientes com osteólise. Os índices creatina/colina, creatina/lactato, lipídio/lactato e colina/lipídio mostraram tendência à diferença entre os grupos estudados. Mais estudos são necessários para a compreensão da participação do masseter no desenvolvimento da osteólise mandibular.
REFERÊNCIAS 1. Kayser C, Andrade LEC. Esclerose sistêmica. In: Sato E. Guias de medicina ambulatorial e hospitalar - reumatologia. São Paulo: Ed. Manole; 2004. p. 111-20. [ ] 2. Mayes MD, Lacey JV Jr, Beebe-Dimmer J, et al. Prevalence, incidence, survival, and disease characteristics of systemic sclerosis in a large US population. Arthritis Rheum. 2003;48:2246-55. [ ] 3. Badea I, Taylor M, Rosenberg A, et al. Pathogenesis and therapeutic approaches for improved topical treatment in localized scleroderma and systemic sclerosis. Rheumatology (Oxford). 2009;48:213-21. [ ] 4. Bouer M, Chammas MC, Messina MCL, et al. Correlação clínica e ultra-sonográfica na esclerodermia localizada cutânea. Radiol Bras. 2008;41: 87-91. [ ] 5. Azevedo ABC, Guimarães SMM, Tavares Jr WC, et al. Avaliação da tomografia de alta resolução versus radiografia de tórax na doença intersticial pulmonar na esclerose sistêmica. Radiol Bras. 2005;38:95-9. [ ] 6. Gasparetto EL, Pimenta R, Inoue C, et al. Esclerose sistêmica progressiva: aspectos na tomografia computadorizada de alta resolução. Radiol Bras. 2005;38:329-32. [ ] 7. Santos MK, Faria FB, Trad CS. Comprometimento pulmonar na esclerose sistêmica: revisão de casos. Radiol Bras. 2006;39:181-4. [ ] 8. Avouac J, Kowal-Bielecka O, Landewé R, et al. European League Against Rheumatism (EULAR) Scleroderma Trial and Research group (EUSTAR) recommendations for the treatment of systemic sclerosis: methods of elaboration and results of systematic literature research. Ann Rheum Dis. 2009;68:629-34. [ ] 9. Pope JE. Musculoskeletal involvement in scleroderma. Rheum Dis Clin North Am. 2003;29:391-408. [ ] 10. Bassett LW, Blocka KLN, Furst DE, et al. Skeletal findings in progressive systemic sclerosis (scleroderma). AJR Am J Roentgenol. 1981;136: 1121-6. [ ] 11. Rosa ACF, Costa EN, Machado MM, et al. Calcinose peritendínea do tendão calcâneo associada a dermatomiosite: correlação entre radiografia convencional, ultra-sonografia, ressonância magnética e macroscopia cirúrgica. Radiol Bras. 2006; 39:75-8. [ ] 12. Taveras JM. The interpretation of radiographs. In: Schwartz L, editor. Disorders of the temporomandibular joint. Philadelphia: Saunders; 1959. p. 154-62. [ ] 13. Pogrel MA. Unilateral osteolysis of the mandibular angle and coronoid process in scleroderma. Int J Oral Maxillofac Surg. 1988;17:155-6. [ ] 14. Ruprecht A, Dolan K, Lilly GE. Osteolysis of the mandible associated with progressive systemic sclerosis. Dentomaxillofac Radiol. 1990;19:31-3. [ ] 15. Ramón Y, Samra H, Oberman M. Mandibular condylosis and apertognathia as presenting symptoms in progressive systemic sclerosis (scleroderma). Pattern of mandibular bony lesions and atrophy of masticatory muscles in PSS, presumably caused by affected muscular arteries. Oral Surg Oral Med Oral Pathol. 1987;63:269-74. [ ] 16. King LE Jr, Olsen NJ, Puett D, et al. Quantitative evaluation of muscle weakness in scleroderma patients using magnetic resonance imaging and spectroscopy. Arch Dermatol. 1993;129:246-7. [ ] 17. Olsen NJ, King LE Jr, Park JH. Muscle abnormalities in scleroderma. Rheum Dis Clin North Am. 1996;22:783-96. [ ] 18. Schmidt WA, Wernicke D, Kiefer E, et al. Colour duplex sonography of finger arteries in vasculitis and in systemic sclerosis. Ann Rheum Dis. 2006;65:265-7. [ ] 19. Ross B, Kreis R, Ernst T. Clinical tools for the 90s: magnetic resonance spectroscopy and metabolite imaging. Eur J Radiol. 1992;14:128-40. [ ] 20. Al-Farra ET, Vandenborne K, Swift A, et al. Magnetic resonance spectroscopy of the masseter muscle in different facial morphological patterns. Am J Orthod Dentofacial Orthop. 2001;120:427-34. [ ] 21. Ramin SL, Tognola WA, Spotti AR. Proton magnetic resonance spectroscopy: clinical application in patients with brain lesions. São Paulo Med J. 2003;121:254-9. [ ] 22. Chung YL, Smith EC, Williams SCR, et al. In vivo proton magnetic resonance spectroscopy in polymyositis and dermatomyositis: a preliminary study. Eur J Med Res. 1997;2:483-7. [ ] 23. Miller BL. A review of chemical issues in H NMR spectroscopy: N-acetyl L-aspartate, creatine and choline. NMR Biomed. 1991;4:47-52. [ ] 24. Nasri LFG. Análise comparativa entre os achados de ressonância magnética e de eletromiografia do músculo facial masseter, em indivíduos com e sem disfunção têmporo-mandibular [tese de doutorado]. São Paulo: Universidade Federal de São Paulo; 2005. [ ] 25. Doornbos J, Luyten PR, Janssen M, et al. P-31 MR spectroscopy of skeletal and cardiac muscle metabolism in patients with systemic sclerosis: a multiple case study. J Magn Reson Imaging. 1994;4:165-8. [ ] 26. Schick F, Duda S, Dürk H, et al. Eosinophiliamyalgia syndrome: findings at MR imaging and proton spectroscopy of the lower leg. Magn Reson Imaging. 1994;12:513-22. [ ] 27. Sharma U, Atri S, Sharma MC, et al. Skeletal muscle metabolism in Duchenne muscular dystrophy (DMD): an in-vitro proton NMR spectroscopy study. Magn Reson Imaging. 2003;21:145-53. [ ] 28. Maheshwari SH, Mukherji SK, Neelon B, et al. The choline/creatine ratio in five benign neoplasms: comparison with squamous cell carcinoma by use of in vitro MR spectroscopy. AJNR Am J Neuroradiol. 2000;21:1930-5. [ ] 29. Finol HJ, Marquez A, Rivera H, et al. Ultrastructure of systemic sclerosis inflammatory myopathy. J Submicrosc Cytol Pathol. 1994;26:245-53. [ ] 30. Herron GS, Romero LI. Vascular abnormalities in scleroderma. Semin Cutan Med Surg. 1998;17: 12-7. [ ]
Recebido para publicação em 18/11/2008.
* Trabalho realizado no Departamento de Diagnóstico por Imagem da Universidade Federal de São Paulo/Escola Paulista de Medicina (Unifesp/EPM), São Paulo, SP, Brasil. |
|
Av. Paulista, 37 - 7° andar - Conj. 71 - CEP 01311-902 - São Paulo - SP - Brazil - Phone: (11) 3372-4544 - Fax: (11) 3372-4554