Radiologia Brasileira - Publicação Científica Oficial do Colégio Brasileiro de Radiologia
AMB - Associação Médica Brasileira CNA - Comissão Nacional de Acreditação
 Vol. 42 nº 2 - Mar. / Abr. of 2009
Vol. 42 nº 2 - Mar. / Abr. of 2009
|
ARTIGO ORIGINAL
|
|
|
|
|
Autho(rs): Jetro Pereira de Oliveira, Luiz Antonio Ribeiro da Rosa, Delano Valdivino Santos Batista, Lúcia Helena Bardella, Arnaldo Rangel Carvalho |
|
|
Descritores: Reto, Braquiterapia, HDR, Dosímetro termoluminescente, Câncer do colo uterino |
|
|
Resumo: VLicenciado em Eletrônica, Operador do Laboratório de Dosimetria Termoluminescente do Serviço de Física Médica em Radioterapia e Medicina Nuclear do Instituto de Radioproteção e Dosimetria (SEFME/IRD), Rio de Janeiro, RJ, Brasil
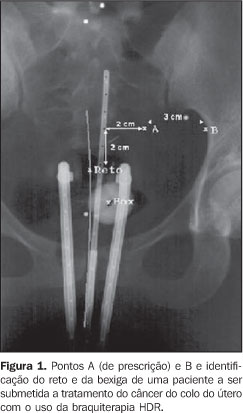
INTRODUÇÃO O colo do útero é um segmento cilíndrico do útero. Ele entra na vagina pela sua parede anterior e repousa, na maioria das vezes, perpendicular ao corpo da vagina. Mede entre 2,0 e 4,0 cm de comprimento. Junta-se com o segmento inferior do útero ao nível do istmo, e essa área é marcada por um discreto estreitamento do lúmen. O câncer do colo do útero representa um contínuo desafio à prática clínica. Segundo o Instituto Nacional de Câncer (INCA), são esperados, em 2008, 19.000 novos casos da doença no Brasil(1). Entre as mulheres brasileiras, o câncer do colo do útero é o terceiro mais comum. Sem considerar os tumores de pele não melanoma, o câncer do colo do útero é o mais incidente na região Norte. Nas regiões Sul, Centro-Oeste e Nordeste esse tipo de câncer ocupa a segunda posição em frequência, e na região Sudeste, a quarta posição(2). Com cerca de 500.000 novos casos por ano no mundo, o câncer do colo uterino é o segundo tipo de câncer mais comum entre as mulheres, sendo responsável pelo óbito de, aproximadamente, 230.000 mulheres por ano. Sua incidência é cerca de duas vezes maior em países menos desenvolvidos, se comparada à dos países mais desenvolvidos(3). Um dos métodos utilizados no combate ao câncer do colo do útero, que faz uso da radiação ionizante, é a radioterapia. A radioterapia se subdivide em teleterapia e braquiterapia. Na braquiterapia, as fontes colocadas próximas ao tumor são radioisótopos cujas radiações, ao penetrarem o tecido de interesse, liberam toda ou parte de sua energia localmente, levando à morte as células neoplásicas(4). A braquiterapia é usada, normalmente, como um tratamento complementar, após a paciente ter sido submetida a teleterapia. Em janeiro de 2001, a radioterapia nacional completou dez anos de experiência com a braquiterapia de alta taxa de dose (HDR - high-dose-rate), definida como o tratamento cuja taxa de dose é superior a 0,2 Gy/min(5). A radioterapia é, sem dúvida, uma opção eficaz para tratar o câncer do colo do útero, mas também representa um perigo aos órgãos radiossensíveis localizados próximos ao útero, como o reto e a bexiga. No caso do reto, uma dose elevada pode causar complicações, com possibilidade de variar de diarréia episódica, espasmo retal e sangramento ocasional até ulceração localizada, estenose parcial, hemorragia recorrente e abundante, com necrose e obstrução, e, finalmente, a formação de fístula retovaginal. Um planejamento adequado do tratamento pode garantir, com boa exatidão, uma alta dose de radiação no tumor e a proteção simultânea do reto e da bexiga de uma exposição a valores elevados de dose. Os sistemas de planejamento usados na braquiterapia para o tratamento do câncer do colo uterino estão baseados em modelos matemáticos, que, naturalmente, têm as suas limitações. Quando possível, são recomendáveis procedimentos para a avaliação das doses nos órgãos de risco, de modo a possibilitar a comparação desses valores de dose com aqueles oriundos do planejamento. Dessa forma, é verificada não só a correção do planejamento, mas também a dos procedimentos de irradiação da própria paciente. Isso pode ser feito adotando medidas in vivo, ou seja, avaliações de dose realizadas durante o tratamento da paciente usando dosímetros termoluminescentes (DTLs), radiofotoluminescentes (RPLGDs - radiophotoluminescent glass dosimeter), transistor de efeito de campo de semicondutor de óxido metálico (MOSFET - metal oxide semiconductor field effect transistor) ou diodos(6-9). Neste trabalho foi proposto o uso do DTL LiF:Mg,Ti,Na, na forma de pó, para medidas de doses in vivo no reto de pacientes durante o tratamento do câncer do colo do útero utilizando fonte de 192Ir em braquiterapia HDR. Critério para a limitação da dose no reto Na braquiterapia, devido à distribuição de dose não homogênea, a prescrição da dose é mais complicada do que na teleterapia. Vários sistemas foram desenvolvidos, com diferentes pontos de prescrição. O relatório nº 38 da Comissão Internacional de Unidades e Medidas da Radiação (ICRU)(10) sugere padronizar a maneira de relatar a dose e o volume do tratamento. Nele são listados itens que deveriam ser incluídos na prescrição de um tratamento intracavitário. A descrição da técnica, incluindo a dose e o fracionamento, a relação temporal com o implante, o tipo de sistema intracavitário aplicado, o isótopo empregado, a dose recebida em um número de pontos relevantes ao controle do tumor, a dose no reto e na bexiga, são alguns dos itens que deveriam ser incorporados no relato do tratamento intracavitário. Os pontos relevantes ao controle tumoral estão localizados na parede pélvica e no trapezóide linfático de Fletcher. Os pontos críticos de referência para a bexiga e o reto são definidos no trígono vesical (na superfície posterior do balão do cateter de Foley preenchido com 7 ml de contraste) e na parede anterior do reto (0,5 cm além da parede posterior da vagina, em uma linha passando pelo ponto médio das fontes dos colpostatos). O trígono vesical é a figura geométrica em forma de um triângulo invertido, cujos vértices são formados pelos locais que correspondem às desembocaduras dos ureteres na bexiga e pelo orifício da uretra, também localizado na bexiga(10). Um dos primeiros passos fundamentais para determinar as distribuições de dose na braquiterapia baseia-se na definição das posições da fonte em relação ao volume alvo e outras características anatômicas de interesse. A prescrição no ponto A, apesar de criticada por muitos autores e pelo relatório nº 38 da ICRU(10), ainda é o método de prescrição mais frequentemente utilizado. O ponto A foi originalmente descrito como estando localizado 2,0 cm superior ao fórnix vaginal e 2,0 cm lateral ao centro do canal uterino, tendo sido desenvolvido para refletir uma dose média dentro do triângulo paracervical contendo as estruturas críticas vasculares (pirâmide de tolerância). O ponto A, idealmente, representa a intersecção do ureter com a artéria uterina. O ponto B, 2,0 cm acima e 5,0 cm lateral, seguindo o mesmo sistema de origens utilizado na localização do ponto A, representa a parede pélvica e, em particular, os linfonodos, como pode ser visto na Figura 1. A dose no ponto B é normalmente um terço da dose no ponto A.
MATERIAIS E MÉTODOS O material termoluminescente utilizado em forma de pó foi o fluoreto de lítio dopado com magnésio, titânio e sódio (LiF: Mg,Ti,Na). Este composto é produzido pela companhia Philitech (Philitech; Paris, França), sob o código DTL937. É um material enriquecido com 7Li (99,994%). O tratamento térmico pré-irradiação utilizado na regeneração do material é de 450 °C durante três horas. Para esse tratamento térmico é utilizado um forno ETT (Fimel; Paris, França). O pó termoluminescente, uma vez irradiado, é avaliado em uma leitora automática PCL3. O tratamento térmico pós-irradiação é realizado no próprio leitor termoluminescente a uma temperatura de 125 °C durante cinco segundos, temperatura essa inferior à de avaliação dos DTLs, de 440 °C. O equipamento é produzido pela empresa francesa Fimel e tem capacidade para ler cerca de 34 mg do material acondicionado em pequenos recipientes confeccionados em aço inoxidável, como pode ser visto na Figura 2.
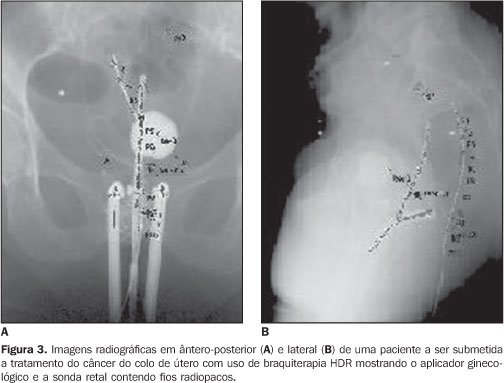
O critério de limitação de dose adotado pelo INCA foi de quatro aplicações com intervalos entre si de uma semana, sendo cada aplicação de 700 cGy (dose prescrita no ponto A), podendo chegar ao reto uma dose de, no máximo, 65% desse valor. Para a bexiga e o sigmoide, a dose está limitada, respectivamente, em 70% e 55% da dose no ponto A. Antes de se medir as doses no reto, foram avaliadas a reprodutibilidade e a linearidade do sistema dosimétrico. O experimento para a verificação da linearidade foi realizado em um simulador cúbico de acrílico cheio de água, com dimensões de 38,0 38,0 30,5 cm3. Cerca de 34 mg do pó dosimétrico foram colocados em capilares com 20,0 cm de comprimento e 3,0 mm de diâmetro. O pó foi acondicionado na parte posterior dos capilares. Estes foram posicionados a 3,0 cm da fonte de 192Ir e irradiados três vezes a diferentes níveis de dose, desde 4,9 até 902,3 cGy. Blocos de "água sólida" foram usados na calibração dos DTLs em função da dose absorvida na água. Este procedimento foi escolhido a fim de minimizar as incertezas no posicionamento dos dosímetros em relação à fonte, pois, devido à presença de elevado gradiente de dose, a precisão no posicionamento do dosímetro em relação à fonte é muito importante. O uso da água sólida no presente trabalho, em substituição à água líquida normal, baseou-se nos resultados de Meli et al.(11), que, utilizando simulação por Monte Carlo, demonstraram a adequação do material simulador para medidas com fontes de 192Ir. As amostras de pó termoluminescente foram calibradas a uma distância de 6,0 cm da fonte de 192Ir. Os valores de dose absorvida na água, nos pontos onde as amostras do material termoluminescente foram posicionadas, foram calculados utilizando o formalismo matemático desenvolvido no relatório nº 51 da Associação Americana dos Físicos em Medicina (AAPM)(12), a partir de medidas de taxa de kerma no ar a 10,0 cm da fonte usando a câmara Farmer com o fator de calibração determinado pelo método desenvolvido por Maréchal(13-15). Depois de se calibrar os DTLs para o espectro de energia da radiação gama do 192Ir, o método foi testado com pacientes sob tratamento no INCA. No procedimento ginecológico de rotina, antes de se iniciar o tratamento, uma sonda é introduzida no reto da paciente. Esta sonda é um tubo de polivinil cloreto atóxico siliconizado, esterilizado por radiação gama e descartável. Dentro deste tubo e dos aplicadores ginecológicos são colocados fios radiopacos. Antes de ser submetida à radiação terapêutica com o 192Ir, a paciente é exposta à radiação X e imagens ântero-posterior e lateral são obtidas e utilizadas no planejamento do tratamento, como podem ser observadas na Figura 3. Dessa forma, as doses administradas ao longo do reto, mais precisamente ao longo do fio radiopaco dentro da sonda retal, podem ser planejadas. Substituindo o fio radiopaco pelo capilar contendo o pó termoluminescente, antes de a paciente ser exposta ao 192Ir, é possível avaliar a dose ao longo desse órgão durante o tratamento e comparar os valores experimentais com os valores determinados pelo sistema de planejamento, possibilitando um novo planejamento para a próxima aplicação do tratamento, caso as doses medidas sejam superiores ao valor limite para o reto.
O capilar utilizado para medir doses no reto possui 20,0 cm de comprimento e 3,0 mm de diâmetro. É formado por dez pequenos compartimentos contendo, cada compartimento, 34 mg do pó dosimétrico. O capilar é introduzido na sonda retal com o máximo de cuidado, para que esta sonda se mantenha na mesma posição anterior quando continha o fio radiopaco. A Figura 4 mostra o desenho desse capilar.
Antes de contribuírem com a presente investigação, todas as pacientes foram esclarecidas quanto ao tipo do experimento a ser realizado e concordaram com a sua realização. Seis pacientes participaram da investigação.
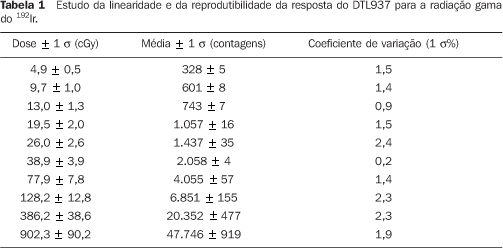
RESULTADOS A Tabela 1 apresenta os resultados do estudo da reprodutibilidade da resposta do DTL937 para a energia da radiação gama do 192Ir. Foram feitas três irradiações para cada valor de dose absorvida. A resposta termoluminescente do material dosimétrico apresenta boa reprodutibilidade, menor que 2,4% para o intervalo de dose considerado, entre 4,9 e 902,3 cGy. A média e o desvio padrão desses valores são (1,6 ± 0,7)%.
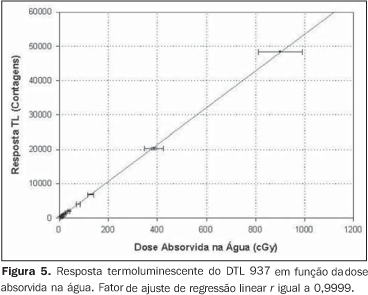
A resposta dos DTLs evidencia um comportamento linear, não havendo a necessidade da aplicação de fatores de correção de linearidade aos resultados obtidos, conforme pode ser observado na Figura 5. O fator de ajuste da regress ão linear, r, é de 0,9999.
A Tabela 2 apresenta os resultados da dosimetria no reto obtidos com as pacientes submetidas a braquiterapia HDR para o tratamento do câncer do colo do útero. São mostradas a dose limite determinada para o reto segundo o critério adotado pelo INCA, a dose máxima obtida pelo sistema de planejamento para o reto, a dose máxima medida no reto com o auxílio dos DTLs, a dose média obtida pelo sistema de planejamento para o reto e a dose média medida no reto via dosimetria termoluminescente. Embora a resposta dos DTLs apresente boa reprodutibilidade (1,6 ± 0,7)%, em média, as incertezas nas medidas experimentais e nos valores de dose obtidos pelo sistema de planejamento são da ordem de 10%. A calibração dos DTLs foi feita com base no formalismo matemático desenvolvido no relatório nº 51 da AAPM(12). O sistema de planejamento utilizado para o cálculo das doses administradas no volume alvo e no reto durante o tratamento de braquiterapia também faz uso do mesmo formalismo. No relatório nº 51 da AAPM(12), com base na propagação quadrática das incertezas envolvidas no formalismo, é estimada uma incerteza de 10% para o valor da dose calculada.
DISCUSSÃO Considerando as incertezas associadas às doses medidas e àquelas planejadas (Tabela 2), observa-se que nos seis casos estudados as doses administradas ao reto das pacientes foram, no máximo, iguais às doses limites determinadas para o órgão, segundo o critério adotado, considerando-se as incertezas estimadas. Em termos de dose média no reto, as medidas apresentaram boa concordância com os valores planejados. O mesmo pode ser verificado quanto aos valores de dose máxima. Nos casos das pacientes 1 e 2, há diferenças um pouco maiores entre os valores planejados e os medidos. Possivelmente, por causa da movimentação interna dos órgãos, o posicionamento dos DTLs não deve ter ocorrido com a mesma exatidão verificada nas demais pacientes. É importantíssimo que os dosímetros sejam posicionados no mesmo ponto adotado para o cálculo da dose pelo sistema de planejamento. As incertezas das medidas experimentais e dos valores de dose obtidos pelo sistema de planejamento são da ordem de 10%. Isto se deve à incerteza inerente do cálculo de dose com base no documento TG 43 da AAPM(12), que é de aproximadamente 10%. Lambert et al.(7) estudaram diferentes dosímetros para a aplicação em dosimetria in vivo durante tratamentos empregando braquiterapia HDR. Foram investigados detectores termoluminescentes, MOSFETs, diamante e cintiladores. Os detectores diamante apresentaram os resultados mais exatos, porém possuem dimensões grandes para medidas de dose em braquiterapia HDR, na qual os gradientes de dose são muito elevados. Os MOSFETs apresentaram erros entre 30% e 40% nas medidas realizadas a mais de 5 cm da fonte, embora para avaliações de dose realizadas entre 2 e 5 cm os erros tenham sido da ordem de 5%. O cintilador apresentou exatidão dosimétrica de 3% para dosimetrias realizadas a distâncias entre 1 e 10 cm da fonte de braquiterapia. A crítica dos autores aos DTLs foi a sua incapacidade de realizar medidas em tempo real, embora o seu desempenho dosimétrico tenha sido bem melhor que aquele dos MOSFETs. É importante frisar que detectores diamante e cintilador não são de uso comum em serviços de radioterapia e que os dosímetros de uso mais comum em física médica para medidas in vivo são os termoluminescentes, os diodos e os MOSFETs(16). Sakata et al.(6) mediram doses no reto utilizando dosímetros semicondutores durante procedimentos de braquiterapia intracavitária para tratamento do câncer ginecológico. Foram pesquisadas 105 pacientes. Seus resultados indicaram diferenças entre as doses planejadas e as medidas de até 5% para 30,8% das pacientes tratadas. Essa diferença pode chegar a 10% para 56% das pacientes e a 20% para 85% das pacientes. Para 15% das pacientes as diferenças entre as doses medidas e planejadas foram superiores a 20%. Waldhäusl et al.(9), utilizando diodos, mediram a dose no reto em 55 aplicações de braquiterapia HDR em pacientes com câncer ginecológico. Foram encontradas diferenças de -31% até +90% entre os valores medidos e os calculados para a dose administrada ao órgão durante o tratamento do câncer uterino. A principal razão das diferenças elevadas deveu-se à incerteza no posicionamento dos detectores. Ao contrário dos resultados encontrados por Waldhäusl et al.(9) e Sakata et al.(6), no presente trabalho as diferenças entre os valores de dose planejados e os valores de dose medidos foram sempre inferiores a 8%, sendo que muitos valores foram inferiores a 3,5%. Quarenta e quatro por cento das diferenças entre os valores de dose calculados e os medidos no reto por Sakata et al.(6) foram maiores que 10%, sendo que 15% destes foram maiores que 20%. Waldhäusl et al.(9) encontraram diferenças que variaram de -31% até +90% entre as doses calculadas e as medidas no reto de pacientes submetidas a braquiterapia HDR. É importante ressaltar que Sakata et al.(6) trabalharam com 105 pacientes e que os resultados de Waldhäusl et al.(9) foram obtidos com 55 aplicações de braquiterapia HDR. No presente trabalho, só se teve acesso a seis pacientes e, portanto, a sua estatística é muito pobre quando comparada às utilizadas na bibliografia mencionada(6,9). Dessa forma, com base nos presentes resultados, não se pode afirmar que o procedimento aqui descrito seja superior aos utilizados pelos autores mencionados(6,9), no entanto, o método mostra-se adequado à avaliação da dose no reto, podendo indicar uma necessidade de reavaliação do planejamento do tratamento no caso da detecção de doses no reto bem superiores (> 10%) às planejadas. Sakata et al.(6) e Waldhäusl et al.(9) utilizaram diodos em seus trabalhos. É importante dizer que, segundo Lambert et al.(7), os diodos são menos exatos que os DTLs nas avaliações das doses in vivo. No presente trabalho, a técnica utilizada foi a dosimetria termoluminescente. Os DTLs apresentam o inconveniente de não permitirem a avaliação da dose em tempo real, o que pode ser obtido com o uso de diodos ou MOSFETs. Entretanto, por não utilizarem cabos e não necessitarem do uso de um eletrômetro durante a medida, eles são mais adaptáveis às medidas in vivo, molestando menos as pacientes. Também têm dimensões menores que os diodos, o que é também uma vantagem para um dosímetro a ser aplicado nas avaliações de dose in vivo. Os MOSFETs podem ter dimensões também muito pequenas, os micro-MOSFETs. Os DTLs são, ainda, bem menos dependentes das variações de temperatura da paciente quando comparados aos diodos(17). O procedimento dosimétrico descrito no presente trabalho permite avaliar as doses administradas ao reto decorrentes do tratamento do câncer do colo do útero com o uso de braquiterapia HDR. Essa avaliação possibilita a tomada de decisões por parte da equipe médica quanto à melhor maneira de continuar o tratamento administrado à paciente, quando da constatação que as doses medidas são superiores às planejadas, visando à proteção do órgão, o que contribui para minimizar as complicações que podem ter lugar quando o reto é exposto a doses elevadas de radiação.
CONCLUSÃO O sistema de dosimetria termoluminescente utilizado no presente trabalho, simples e de fácil utilização quando comparado a outras possíveis técnicas dosimétricas aplicáveis à dosimetria in vivo no reto, mostrou-se eficiente na avaliação da dose no reto de pacientes submetidas a braquiterapia HDR para o tratamento do câncer de colo uterino, possibilitando a reavaliação do planejamento do tratamento entre a primeira e a segunda aplicação semanal, quando doses superiores às limites (> 10%) forem medidas no órgão a ser protegido. Agradecimentos À Comissão Nacional de Energia Nuclear (CNEN), pelo suporte financeiro recebido, ao Dr. Andrés Reinaldo Rodrigues Papa, primeiro Coordenador da Comissão de Pós-Graduação do Instituto de Radioproteção e Dosimetria (CPG/IRD), pelo apoio durante o curso de mestrado do primeiro autor, à equipe de braquiterapia do INCA, pelo apoio constante durante todo o período de medidas, e a todas as pessoas que de alguma forma auxiliaram na concepção e desenvolvimento do trabalho.
REFERÊNCIAS 1. Instituto Nacional de Câncer. Estimativa 2008: incidência de câncer no Brasil. Rio de Janeiro: INCA; 2007. p. 24. [ ] 2. Instituto Nacional de Câncer. Estimativa 2008: incidência de câncer no Brasil. Rio de Janeiro: INCA; 2007. p. 32. [ ] 3. Salvajoli JV, Souhami L, Faria LS. Radioterapia em oncologia. 1ª ed. Rio de Janeiro: Editora Médica e Científica; 1999. [ ] 4. Calcina CSG, Almeida A, Rocha JRO. Análises de protocolos de braquiterapia, por alta taxa de dose, do controle de qualidade de alguns serviços locais, baseados no TG40, TG56 e ARCAL XXX. Radiol Bras. 2001;34:225-32. [ ] 5. Esteves SCB, Oliveira ACZ, Feijó LFA. Braquiterapia de alta taxa de dose no Brasil. Radiol Bras. 2004;37:337-41. [ ] 6. Sakata K, Nagakura H, Oouchi A, et al. High-dose-rate intracavitary brachytherapy: results of analyses of late rectal complications. Int J Radiat Oncol Biol Phys. 2002;54:1369-76. [ ] 7. Lambert J, Nakano T, Law S, et al. In vivo dosimeters for HDR brachytherapy: a comparison of a diamond detector, MOSFET, TLD, and scintillation detector. Med Phys. 2007;34:1759-65. [ ] 8. Nose T, Koizumi M, Yoshida K, et al. In vivo dosimetry of high-dose-rate interstitial brachyther-apy in the pelvic region: use of radiophotolumi-nescence glass dosimeter for measurement of 1004 points in 66 patients with pelvic malignancy. Int J Radiat Oncol Biol Phys. 2008;70: 626-33. [ ] 9. Waldhäusl C, Wambersie A, Pötter R, et al. In-vivo dosimetry for gynaecological brachytherapy: physical and clinical considerations. Radiother Oncol. 2005;77:310-7. [ ] 10. International Commission on Radiation Units and Measurements. Dose and volume specification for reporting intracavitary therapy in gynaecology. ICRU Report 38. Bethesda: ICRU; 1985. p. 1-16. [ ] 11. Meli J, Meigooni A, Nath R. On the choice of phantom material for the dosimetry of 192Ir sources. Int J Radiat Oncol Biol Phys. 1988;14: 587-94. [ ] 12. American Association of Physicists in Medicine. Dosimetry of interstitial brachytherapy sources: recommendations of the AAPM Radiation Therapy Committee Task Group No. 43. AAPM Report No. 51. Woodbury: American Institute of Physics; 1995. [Reprinted from Med Phys. 1995;22:209-34] [ ]. 13. Maréchal MH. Recomendações para calibração de fontes de 192Ir de alta taxa de dose [tese de doutorado]. Rio de Janeiro: Universidade do Estado do Rio de Janeiro; 2000. [ ] 14. Ferreira IH, Almeida CE, Marre D, et al. Monte Carlo calculations of the ionization chamber wall correction factors for 192Ir and 60Co gamma rays and 250 kV x-rays for use in calibration of 192Ir HDR brachytherapy sources. Phys Med Biol. 1999;44:1897-904. [ ] 15. Maréchal MH, Almeida CE, Ferreira IH, et al. Experimental derivation of wall correction factors for ionization chambers used in high dose rate 192Ir source calibration. Med Phys. 2002;29:1-5. [ ] 16. Kron T. Applications of thermoluminescence dosimetry in medicine. Radiat Prot Dosimetry. 1999;85:333-40. [ ] 17. Mayles WPM, Heisig S, Mayles HMO. Treatment verification and in vivo dosimetry. In: Williams JR, Thwaites DI, editors. Radiotherapy physics in practice. 2nd ed. New York: Oxford University Press, Inc.; 2000. p. 220-46. [ ]
Recebido para publicação em 14/9/2007
* Trabalho realizado no Instituto Nacional de Câncer (INCA), Rio de Janeiro, RJ, Brasil. |
|
Av. Paulista, 37 - 7° andar - Conj. 71 - CEP 01311-902 - São Paulo - SP - Brazil - Phone: (11) 3372-4544 - Fax: (11) 3372-4554