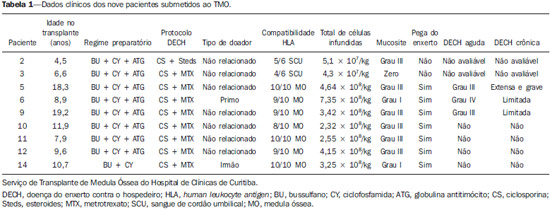
Radiologia Brasileira - Publicação Científica Oficial do Colégio Brasileiro de Radiologia
AMB - Associação Médica Brasileira CNA - Comissão Nacional de Acreditação
 Vol. 47 nº 6 - Nov. / Dez. of 2014
Vol. 47 nº 6 - Nov. / Dez. of 2014
|
ARTIGO ORIGINAL
|
|
|
|
|
Autho(rs): Sergio Eiji Ono1; Arnolfo de Carvalho Neto2; Emerson Leandro Gasparetto3; Luiz Otávio de Mattos Coelho4; Dante Luiz Escuissato2; Carmem Maria Sales Bonfim5; Lisandro Lima Ribeiro6 |
|
|
Descritores: Adrenoleucodistrofia ligada ao X; Ressonância magnética; Tensor de difusão; Escore de Loes. |
|
|
Resumo: INTRODUÇÃO
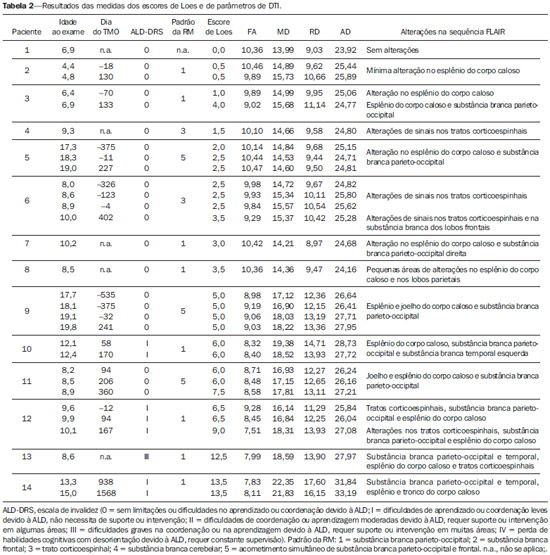
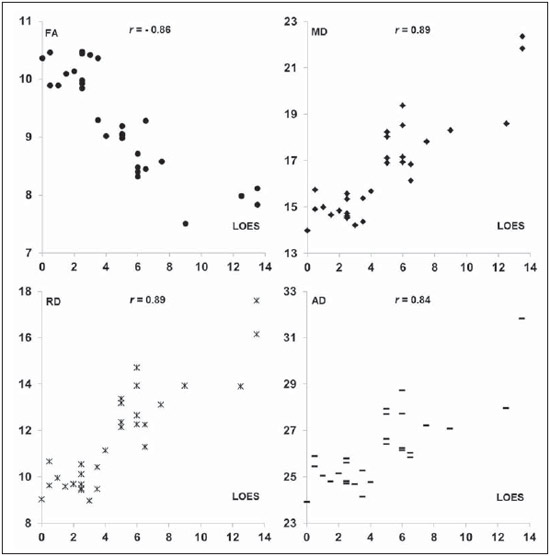
A adrenoleucodistrofia ligada ao X (ALD-X), registrada na biblioteca OMIM® (Online Mendelian Inheritance in Man®) da Universidade de Johns Hopkins, com a referência #300100, é uma doença secundária a mutação no gene ABCD1 e resulta no defeito da beta oxidação peroxissomal e acúmulo de ácidos graxos saturados de cadeia muito longa (VLCFA) em todos os tecidos do corpo. É determinada geneticamente como herança recessiva ligada ao cromossomo X. As manifestações da doença ocorrem primariamente no córtex adrenal, na mielina do sistema nervoso central e nas células de Leydig nos testículos. O teste diagnóstico mais comumente utilizado é a demonstração do excesso dos VLCFAs no plasma. É importante avaliar com cuidado o fenótipo do paciente, que frequentemente muda com o tempo(1). Cerca de 50% dos pacientes com o defeito genético da ALD-X desenvolvem a forma cerebral inflamatória em algum estágio da vida, mais comumente na infância, entre 4 e 8 anos de vida. O desenvolvimento neurológico e a função cognitiva no início são normais. Alterações na ressonância magnética (RM) do encéfalo antecedem os sintomas(2), com relatos de alterações na espectroscopia de prótons da RM (MRS) antecedendo alterações na RM convencional(3,4). Em aproximadamente 80% a 85% destes pacientes as lesões iniciais e mais graves envolvem as regiões parieto-occipitais. O acúmulo anormal de VLCFA na substância branca tem papel importante na cascata de destruição da mielina e do axônio que ocorre neste fenótipo. O padrão ouro para avaliar a progressão da doença na ALD-X foi proposto por Loes em 1994(5), em uma escala de gravidade na RM de 34 pontos usando um sistema de pontuação baseado na localização e extensão do envolvimento e avaliação de presença de atrofia local ou global. As localizações selecionadas para o escore de gravidade são as substâncias brancas parieto-occipital, temporal anterior e frontal, corpo caloso, vias visuais e auditivas, fibras de projeção, cerebelo e núcleos da base. O escore de gravidade auxilia na determinação da extensão do dano na mielina no encéfalo. Considera-se um estágio bastante precoce se os escores forem menores que 4, um estágio precoce é considerado com escores entre 4 e 8, um estágio tardio é entre 9 e 13 e um estágio muito tardio se os escores forem maiores que 13. O escore de Loes é um dos parâmetros usados no seguimento e orienta decisões terapêuticas para o transplante de células hematopoiéticas (TMO). A progressão das alterações na RM na ALD-X depende da idade do paciente, escore inicial ao diagnóstico e localização anatômica das lesões (padrão da RM). Quando estes dados são interpretados em conjunto, auxiliam a predizer o curso da doença e a seleção de candidatos para o TMO(6). Peters et al.(7) sugerem que o paciente com escore de Loes menor que 9 pode se beneficiar do TMO, mas opiniões mais recentes sinalizam que até mesmo escores menores (< 4) podem ser melhores na seleção de candidatos para o TMO(8). O TMO não pode ser justificado na ausência de evidências de desmielinização (i.e., escore de Loes igual a zero), porque 60% a 85% dos meninos não desenvolverão a doença cerebral durante a infância(7). O TMO é o único tratamento que pode interromper o processo de desmielinização de pacientes com ALD-X e resultar em uma boa qualidade de vida em longo prazo, desde que o procedimento seja feito no estágio inicial da doença(9), mostrando uma sobrevida de 5 anos de 89% a 95% contra uma probabilidade de sobrevida de 45% a 54% em pacientes não tratados com o TMO(7,10,11), mas uma cura definitiva ainda não existe(12). Considerando que o diagnóstico precoce e o transplante no momento certo são essenciais para que os resultados sejam otimizados, nós esperamos que o uso das técnicas avançadas de RM possa auxiliar nas decisões terapêuticas. A difusão anisotrópica da água nas fibras nervosas é a base da utilização do tensor de difusão (DTI diffusion tensor imaging) para estabelecer o trajeto das fibras nervosas. O fato de a difusão da água ser sensível à microestrutura do tecido subjacente fornece um método para avaliar a orientação e integridade destas fibras nervosas, que pode ser útil na avaliação de várias doenças neurológicas(13). O uso do DTI tem várias aplicações, e a alteração da anisotropia em doenças desmielinizantes, principalmente na esclerose múltipla, tem sido demonstrada por vários grupos(14-17). Outros artigos mostraram que os parâmetros de imagem da RM correlacionam com parâmetros histopatológicos na substância branca de forma confiável usando medidas do DTI(18,19). Os parâmetros do DTI avaliados no presente estudo foram a fração de anisotropia (FA) e as difusibilidades média, radial e axial (MD, RD e AD). O DTI é um modelo matemático representado por uma matriz de vetores, sendo que os três eixos do DTI são chamados de eingenvectors, cujas magnitudes são os eingenvalues. O maior vetor corresponde à difusibilidade longitudinal ou axial (AD) e a média dos demais vetores corresponde à RD. A média dos três eingenvalues é a MD. A FA mede o "grau de direcionalidade" da difusibilidade intravoxel, com valores variando de zero, no caso de difusão isotrópica, a 1, indicando difusão perfeitamente linear(20). Para o estudo da ALD, Ito et al.(21) avaliaram 11 pacientes masculinos e mediram a FA em áreas com alterações de sinais, mostrando a redução deste valor comparado a áreas aparentemente normais. Um artigo de Schneider et al., de 2003(22), avaliou a FA em três pacientes e observou a redução da FA comparada a sete controles, sugerindo este parâmetro como indicador de desmielinização em áreas consideradas normais no exame de RM convencional. Em razão do pequeno número de observações, sugeriram-se avaliações em séries maiores. Alterações de aumento da DR estão relacionadas a dano na mielina e danos no axônio estariam relacionados ao aumento do valor da DA(23). Não há na literatura estudos que avaliem a ALD pelo método e pelos escores propostos no presente trabalho. MATERIAIS E MÉTODOS O estudo foi aprovado pelo Comitê de Ética em Pesquisa em Seres Humanos do Hospital de Clínicas de Curitiba da Universidade Federal do Paraná (HC-UFPR), credenciado na Comissão Nacional de Ética em Pesquisa do Ministério da Saúde. Foram avaliados exames de RM de 14 pacientes masculinos com diagnóstico de ALD, com idades entre 4 e 20 anos, 9 deles submetidos a TMO (Tabela 1). Os exames abrangem um período de 5 anos e 3 meses, entre março de 2007 e junho de 2012. O trabalho é retrospectivo, avaliando o DTI de exames de rotina de RM de pacientes acompanhados pelo Serviço de Transplante de Medula Óssea do HC-UFPR. Foram realizadas medidas dos parâmetros de DTI em um grupo controle formado por 28 pacientes masculinos, com idades entre 4 e 20 anos, que tinham queixas clínicas não atribuídas a doenças de substância branca (investigação de cefaleias, doenças dos ouvidos internos, regiões das órbitas e sela turca e estudo de lesões extra-axiais cisto de aracnoide) e com resultados normais no estudo de RM convencional. Os exames dos pacientes com ALD foram realizados em aparelho de RM de alto campo magnético, de 1,5 tesla (Magnetom® Avanto; Siemens AG, Erlangen, Alemanha), com os seguintes parâmetros: sequência FLAIR (imagens no plano sagital, TR de 7.000 ms, TE de 384 ms, TI de 2.500 ms, espessura de corte de 1 mm, matriz 424 × 512, FOV de 230 × 280 mm) para avaliação convencional das alterações morfológicas e de sinais das lesões, determinando-se o escore de Loes, e o DTI (plano axial, TR de 4.900 ms, TE de 103 ms, espessura de corte de 3 mm, matriz 192 × 192, FOV de 230 × 230 mm, 12 direções). Os exames do grupo controle foram realizados no mesmo aparelho, com parâmetros do DTI ajustados para exames clínicos: TR de 3.100 ms, TE de 95 ms, espessura de corte de 5 mm, matriz 148 × 148, FOV de 230 × 230 mm, 12 direções. Dois radiologistas com mais de cinco anos de experiência em neurorradiologia (observador 1: Ono SE; observador 2: Coelho LOM) fizeram a interpretação das imagens convencionais (FLAIR) para o escore de Loes e as leituras dos parâmetros do DTI. A interpretação das imagens FLAIR foi de forma independente, e no caso de discrepâncias o escore de Loes foi definido por consenso. As leituras dos parâmetros DTI foram obtidas de forma independente para avaliação de concordância intra e interobservador. A leitura, a interpretação e o cálculo do escore de Loes foram obtidos de forma direta, por análise das imagens da sequência FLAIR, utilizando-se visualizador de arquivos DICOM (Kodak Care-stream PACS Client Suite). Já o processamento do DTI deriva várias medidas, sendo que as de interesse são FA, MD, RD e AD, obtidas com o software de uso público DTI-Studio, versão 3.0.3 (https://www.mristudio.org). Com os mapas dos parâmetros de DTI, fizeram-se as medidas de FA, trace e RD em regiões de interesse (ROIs) predeterminadas, tendo como referência os locais do estudo de Schneider et al.(22). As medidas dos parâmetros de DTI foram realizadas em 9 locais bilateralmente, totalizando 18 medidas, nas seguintes localizações: braços anterior e posterior da cápsula interna, centro semioval, substância branca parietal, substância branca occipital, substância branca temporal anterior, substância branca frontal e joelho e esplênio do corpo caloso. A Figura 1 mostra estes locais em um exame padrão e a Figura 2 mostra exemplo de mensuração em um dos pacientes dos valores de FA, traço do tensor (trace), RD e do eingenvalue principal (corresponde à AD). Para esta leitura foi utilizado o próprio DTI-Studio. A medida do parâmetro MD foi derivada da medida trace (MD = trace/3). O parâmetro AD foi obtido usando-se a fórmula: AD = trace 2 × RD. Ao final, as 18 medidas de cada parâmetro foram somadas para se obter um valor único que pudesse ser correlacionado ao escore de Loes. Para medidas de FA espera-se uma correlação negativa, com diminuição da FA, e para medidas de MD, RD e AD espera-se uma correlação positiva dos valores. 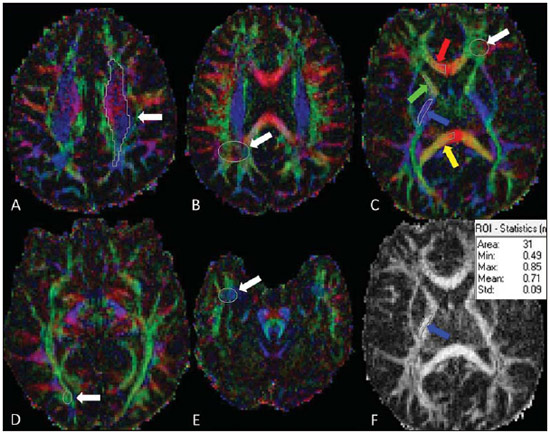 Figura 1. ROIs propostas nos mapas de FA. A: Centro semioval (esquerdo). B: Substância branca no lobo parietal (direito). C: Substância branca no lobo frontal (esquerdo), joelho do corpo caloso (porção direita), braço anterior da cápsula interna (direita), braço posterior da cápsula interna (direita), esplênio do corpo caloso (porção direita). D: Substância branca no lobo occipital (direito). E: Lobo temporal (direito). F: Exemplo de medida de FA, correspondente ao mapa de FA colorido na ilustração C. A seta aponta a ROI no braço posterior da cápsula interna direita e o quadro mostra valores obtidos na leitura desta ROI, com média de 0,71. 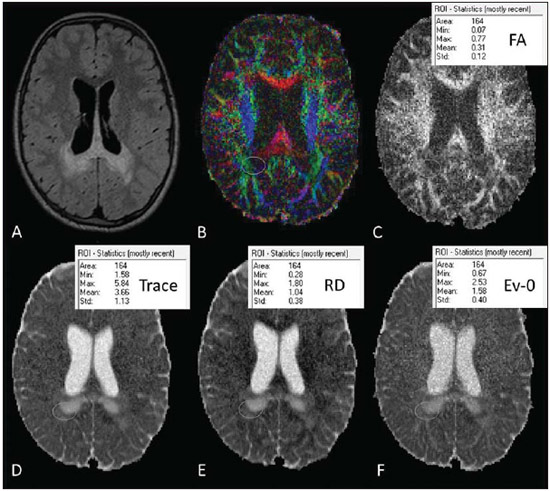 Figura 2. Ilustração da mensuração com ROIs em um dos pacientes, sendo exemplificado na substância branca do lobo parietal direito. A: Corte axial FLAIR. B: Mapa de FA colorido. C: Medida de FA. D: Medida trace do tensor. E: Difusibilidade radial. F: Eingenvalue 0 (difusibilidade axial). RESULTADOS A análise estatística dos dados coletados foi baseada nos coeficientes de correlação de Pearson (r), com nível de significância estatística dependente do tamanho dos grupos comparados. Valores de p menores que 0,05 indicam significância estatística. Correlação forte foi considerada para valores de coeficientes (r) acima de 0,7. A análise das medidas de DTI de pacientes do grupo controle (pareados por idade) foi feita para obter parâmetros do DTI estimados com valores médios e desvios-padrão de FA, MD, RD e AD. A análise intraobservador foi feita com dados coletados pelo observador 1 com os dados dos pacientes com ALD, com medidas dos parâmetros de DTI tomadas com uma semana de intervalo. A análise interobservador de dados dos pacientes com ALD comparou resultados do observador 1 (média das duas medidas usadas na análise intraobservador) e medidas do observador 2 (medida única). A análise interobservador dos dados do grupo controle comparou dados coletados pelos observadores 1 e 2. As medidas de DTI usadas para correlação com o escore de Loes foram a média dos resultados obtidos pelo observador 1 (média de duas medidas) e pelo observador 2 (medida única). Os resultados dos 30 exames dos 14 pacientes com ALD estão tabulados na Tabela 2. A análise estatística intraobservador dos escores de DTI dos exames dos pacientes com ALD mostrou coeficientes de Pearson de 0,96, 0,96, 0,95 e 0,80 para os escores de FA, MD, RD e AD, respectivamente, todos com nível de significância p < 0,01. A análise estatística interobservador com dados de pacientes com ALD apresentou coeficientes de Pearson de 0,97 para escores de FA, MD e RD e 0,94 para escore de AD (p < 0,01). As medidas dos parâmetros de DTI do grupo controle sugerem que mudanças decorrentes do desenvolvimento ainda ocorrem na faixa etária dos 4 aos 20 anos de idade. Linhas de tendência mostram diminuição dos escores de MD, RD e AD e aumento do escore de FA. Considerando que o grupo controle é pequeno e que o coeficiente de correlação de Pearson em relação à idade mostra nenhuma a pouca correlação, a amostra de 28 pacientes do grupo controle foi usada para obter os valores de médias e desvios-padrão para esta faixa etária (FA = 10,23 ± 0,48; MD = 14,20 ± 0,63; RD = 8,84 ± 0,76 e AD = 24,91 ± 0,57). A análise estatística da correlação entre as medidas de DTI e escores de Loes nos pacientes com ALD obteve coeficientes de correlação de 0,86, 0,89, 0,89 e 0,84 para medidas de FA, MD, RD e AD, todos com p < 0,01 (Figura 3). DISCUSSÃO A RM do encéfalo de pacientes com ALD-X é importante para mostrar a progressão de lesões(24). O exame convencional de RM tem alta sensibilidade para a detecção de anormalidades na substância branca, mas baixa especificidade. Achados patológicos relacionados com estas alterações de sinais são altamente variáveis e incluem hipomielinização, desmielinização, perda axonal, gliose, edema intersticial e degeneração cística da substância branca(18). Técnicas avançadas de RM, como espectroscopia de prótons e em particular imagens ponderadas em difusão, parecem melhorar a sensibilidade e especificidade da avaliação pela RM, mediante identificação e diferenciação mais precisa destes processos patológicos(25,26). A hipótese é que os parâmetros de DTI correlacionam-se com o grau de desmielinização e gravidade da doença. A análise estatística mostrou forte correlação entre parâmetros de DTI e os escores de Loes, com coeficientes de correlação de Pearson acima de 0,84, em valores absolutos (p < 0,01). Para avaliar as medidas dos parâmetros de DTI não há dados na literatura, e foi necessário obter valores de referência (controles) pareados com os casos do estudo. Os parâmetros de DTI são considerados relativamente estáveis após os 24 meses de vida(27), mas mudanças ainda ocorrem após este período, durante o desenvolvimento cerebral(28). Isto foi observado no grupo controle, com medidas de DTI indicando uma tendência de aumento da FA e diminuição nas medidas de MD, RD e AD, considerando as contribuições totais da substância branca amostradas, apesar de nenhuma a pouca correlação em relação à idade. Este fato foi considerado para obter os valores médios e desvios-padrão dos valores de DTI na faixa etária dos controles. Apesar de o escore de Loes permitir avaliar várias possíveis alterações, com escores entre 0 e 34 pontos, o artigo original mostrou que o grupo estudado tinha uma média de escores de 9 pontos, com valores entre 0,5 e 25, em uma amostra de 83 pacientes(5). Nossa amostra tem pacientes com escores de Loes variando de 0 a 13,5 (incluindo pacientes nos estágios muito precoce, precoce e tardio), sendo uma limitação relativa considerando o objetivo de correlacionar escores, mas na realidade avaliando escores na faixa de interesse para a decisão de TMO, pois valores de escores mais altos (estágio muito tardio) não são considerados para este procedimento. Outra limitação está relacionada aos parâmetros de aquisição, com foco na redução do tempo de aquisição para minimizar artefatos de movimento. A aquisição do DTI usou 12 direções, enquanto estudos de simulação indicam que pelo menos 20 direções são necessárias para uma estimativa robusta da anisotropia e pelo menos 30 direções para uma estimativa robusta do tensor(29). Outro problema é a seleção da ROI, que é observador dependente. As localizações das ROIs propostas são fixas, porém podem não incluir regiões com alterações, e no caso áreas com substância branca com aspecto aparentemente normal e áreas alteradas, podendo causar dificuldades na seleção dos limites da ROI. Uma observação importante sobre a escala de gravidade proposta por Loes é que mudanças sutis na RM convencional podem não ser refletidas em um aumento do escore, dando alguma incerteza na progressão da doença considerando a interpretação das imagens convencionais. Considerando que o paciente pode se beneficiar do TMO antes que os déficits neurológicos se tornem evidentes, é importante identificar a desmielinização precoce. Analisando as medidas de DTI dos pacientes 1 a 8 (Tabela 2), notamos algumas tendências que já foram sugeridas por Schneider et al.(22). O paciente 2 demonstrou alterações nas medidas de MD e RD, apesar de baixos escores de Loes. O paciente 3 tinha medidas de MD e RD alteradas (mais de um desvio-padrão) com escore de Loes de 1, e na sequência foi observada mudança significativa nestas medidas (mais de dois desvios-padrão) e uma mudança súbita no escore de Loes. O paciente 5 mostrou doença estável após o TMO e as medidas de DTI apresentaram poucas mudanças. O paciente 6 mostrou alterações progressivas nas medidas de DTI, apesar de escores de Loes sem alterações no pré-TMO. Estes pacientes não apresentaram mudanças significativas nas medidas de FA. Isto está, de certa forma, de acordo com o que Schneider et al. observaram no estudo deles, sendo que valores de MD mostraram alterações patológicas mais pronunciadas do que os valores de FA na substância branca aparentemente normal(22). O número pequeno de pacientes limita a análise estatística, mas nós consideramos importante a observação de tendência de alterações nas medidas de DTI, apesar de escores de Loes sem alterações, particularmente na faixa de escores entre 0 e 4, que é considerada a faixa de interesse na qual os pacientes com ALD teriam maior benefício. Apenas o transplante de células hematopoiéticas alogênico pode levar à estabilização da doença em longo prazo e aumentar a sobrevida(11). O TMO é recomendado no estágio inicial da ALD, necessitando parâmetros clínicos e exames complementares confiáveis para aumentar a chance de um resultado positivo, e o estudo tem a intenção de fornecer um método adicional para auxiliar o seguimento de pacientes com ALD. Uma análise mais detalhada nas medidas de DTI na faixa de escore de gravidade de 0 a 4 mostrou uma tendência de mudança nos parâmetros de DTI, apesar de não mostrar alterações no escore de Loes, indicando que medidas de MD e RD podem potencialmente ser úteis nos estágios muito precoce e precoce da doença, e poderiam ser utilizados como parâmetros de seguimento como adjunto ao escore de Loes, porém, investigações adicionais com séries maiores de pacientes são necessárias para validar o método proposto para uso clínico. Sugere-se também que a avaliação do tensor possa ser mais precisa com o uso de técnicas avaliando os parâmetros do DTI de forma global, com processamento estatístico baseado em tractos, por exemplo, o Tract-Based Spatial Statistics (TBSS)(30), em vez de baseado em ROIs. CONCLUSÃO A avaliação dos parâmetros de DTI nos exames de seguimento de pacientes com ALD-X mostrou correlação com os escores de Loes e em estágios precoces da doença poderia auxiliar com informações adicionais em relação ao exame convencional, sendo que alterações foram percebidas nas medidas de MD e RD. No entanto, considerando-se o tamanho da amostra e as limitações do estudo, sugere-se que estudos adicionais sejam feitos com um número maior de pacientes, para melhor demonstração das correlações observadas no presente estudo. REFERÊNCIAS 1. Moser HW. Therapy of X-linked adrenoleukodystrophy. NeuroRx. 2006;3:246-53. 2. Moser HW, Barker PB. Magnetic resonance spectroscopy: a new guide for the therapy of adrenoleukodystrophy. Neurology. 2005;64:406-7. 3. Pouwels PJ, Kruse B, Korenke GC, et al. Quantitative proton magnetic resonance spectroscopy of childhood adrenoleukodystrophy. Neuropediatrics. 1998;29:254-64. 4. Eichler FS, Itoh R, Barker PB, et al. Proton MR spectroscopic and diffusion tensor brain MR imaging in X-linked adrenoleukodystrophy: initial experience. Radiology. 2002;225:245-52. 5. Loes DJ, Hite S, Moser H, et al. Adrenoleukodystrophy: a scoring method for brain MR observations. AJNR Am J Neuroradiol. 1994;15:1761-6. 6. Loes DJ, Fatemi A, Melhem ER, et al. Analysis of MRI patterns aids prediction of progression in X-linked adrenoleukodystrophy. Neurology. 2003;61:369-74. 7. Peters C, Charnas LR, Tan Y, et al. Cerebral X-linked adrenoleukodystrophy: the international hematopoietic cell transplantation experience from 1982 to 1999. Blood. 2004;104:881-8. 8. Warren DJ, Connolly DJA, Wilkinson ID, et al. Magnetic resonance spectroscopy changes following haemopoietic stem cell transplantation in children with cerebral adrenoleukodystrophy. Dev Med Child Neurol. 2007;49:135-9. 9. Cartier N, Aubourg P. Hematopoietic stem cell transplantation and hematopoietic stem cell gene therapy in X-linked adrenoleukodystrophy. Brain Pathol. 2010;20:857-62. 10. Mahmood A, Raymond GV, Dubey P, et al. Survival analysis of haematopoietic cell transplantation for childhood cerebral X-linked adrenoleukodystrophy: a comparison study. Lancet Neurol. 2007;6:687-92. 11. Miller WP, Rothman SM, Nascene D, et al. Outcomes after allogeneic hematopoietic cell transplantation for childhood cerebral adrenoleukodystrophy: the largest single-institution cohort report. Blood. 2011;118:1971-8. 12. Moser HW, Raymond GV, Dubey P. Adrenoleukodystrophy: new approaches to a neurodegenerative disease. JAMA. 2005;294:3131-4. 13. Beaulieu C. The basis of anisotropic water diffusion in the nervous system - a technical review. NMR Biomed. 2002;15:435-55. 14. Filippi M, Cercignani M, Inglese M, et al. Diffusion tensor magnetic resonance imaging in multiple sclerosis. Neurology. 2001;56:304-11. 15. Nucifora PGP, Verma R, Lee SK, et al. Diffusion-tensor MR imaging and tractography: exploring brain microstructure and connectivity. Radiology. 2007;245:367-84. 16. Castriota-Scanderbeg A, Fasano F, Hagberg G, et al. Coefficient D(av) is more sensitive than fractional anisotropy in monitoring progression of irreversible tissue damage in focal nonactive multiple sclerosis lesions. AJNR Am J Neuroradiol. 2003;24:663-70. 17. Roychowdhury S, Maldjian JA, Grossman RI. Multiple sclerosis: comparison of trace apparent diffusion coefficients with MR enhancement pattern of lesions. AJNR Am J Neuroradiol. 2000;21:869-74. 18. van der Voorn JP, Pouwels PJW, Powers JM, et al. Correlating quantitative MR imaging with histopathology in X-linked adrenoleukodystrophy. AJNR Am J Neuroradiol. 2011;32:481-9. 19. Seewann A, Vrenken H, van der Valk P, et al. Diffusely abnormal white matter in chronic multiple sclerosis: imaging and histopathologic analysis. Arch Neurol. 2009;66:601-9. 20. Mukherjee P, Berman JI, Chung SW, et al. Diffusion tensor MR imaging and fiber tractography: theoretic underpinnings. AJNR Am J Neuroradiol. 2008;29:632-41. 21. Ito R, Melhem ER, Mori S, et al. Diffusion tensor brain MR imaging in X-linked cerebral adrenoleukodystrophy. Neurology. 2001;56:544-7. 22. Schneider JFL, Il'yasov KA, Boltshauser E, et al. Diffusion tensor imaging in cases of adrenoleukodystrophy: preliminary experience as a marker for early demyelination? AJNR Am J Neuroradiol. 2003;24:819-24. 23. Song SK, Sun SW, Ju WK, et al. Diffusion tensor imaging detects and differentiates axon and myelin degeneration in mouse optic nerve after retinal ischemia. Neuroimage. 2003;20:1714-22. 24. Gasparetto EL, Rosa JM, Davaus T, et al. Cerebral X-linked adrenoleukodystrophy: follow-up with magnetic resonance imaging. Arq Neuropsiquiatr. 2006;64:1033-5. 25. Patay Z. Diffusion-weighted MR imaging in leukodystrophies. Eur Radiol. 2005;15:2284-303. 26. Bizzi A, Castelli G, Bugiani M, et al. Classification of childhood white matter disorders using proton MR spectroscopic imaging. AJNR Am J Neuroradiol. 2008;29:1270-5. 27. Hermoye L, Saint-Martin C, Cosnard G, et al. Pediatric diffusion tensor imaging: normal database and observation of the white matter maturation in early childhood. Neuroimage. 2006;29:493-504. 28. Kumar R, Nguyen HD, Macey PM, et al. Regional brain axial and radial diffusivity changes during development. J Neurosci Res. 2012;90:346-55. 29. Mukherjee P, Chung SW, Berman JI, et al. Diffusion tensor MR imaging and fiber tractography: technical considerations. AJNR Am J Neuroradiol. 2008;29:843-52. 30. Smith SM, Jenkinson M, Johansen-Berg H, et al. Tract-based spatial statistics: voxelwise analysis of multi-subject diffusion data. Neuroimage. 2006;31:1487-505. 1. Mestre, Médico Radiologista da Clínica DAPI Diagnóstico Avançado por Imagem, Curitiba, PR, Brasil 2. Doutores, Professores Adjuntos da Universidade Federal do Paraná (UFPR), Radiologistas da Clínica DAPI Diagnóstico Avançado por Imagem, Curitiba, PR, Brasil 3. Doutor, Bolsista de Produtividade em Pesquisa do Conselho Nacional de Desenvolvimento Científico e Tecnológico (CNPq), Curso de Pós Graduação em Medicina (Radiologia), Departamento de Radiologia da Universidade Federal do Rio de Janeiro (UFRJ), Rio de Janeiro, RJ, Brasil 4. Membro Titular do Colégio Brasileiro de Radiologia e Diagnóstico por Imagem (CBR), Médico Radiologista da Clínica DAPI Diagnóstico Avançado por Imagem, Curitiba, PR, Brasil 5. Médica Hematologista, Coordenadora do Programa de Transplante de Medula Óssea (TMO) Pediátrico do Hospital de Clínicas da Universidade Federal do Paraná (HC-UFPR), Curitiba, PR, Brasil 6. Médico Hematologista do Ambulatório de Anemia de Fanconi do Serviço de Transplante de Medulo Óssea (TMO) do Hospital de Clínicas da Universidade Federal do Paraná (HC-UFPR), Curitiba, PR, Brasil Endereço para correspondência: Dr. Sergio Eiji Ono DAPI Diagnóstico Avançado por Imagem Rua Brigadeiro Franco, 122, Mercês Curitiba, PR, Brasil, 80430-210 E-mail: ono.sergio@gmail.com Recebido para publicação em 18/8/2013. Aceito, após revisão, em 29/4/2014. Trabalho realizado no Hospital de Clínicas da Universidade Federal do Paraná (HC-UFPR) e na Clínica DAPI Diagnóstico Avançado por Imagem, Curitiba, PR, Brasil. |
|
Av. Paulista, 37 - 7° andar - Conj. 71 - CEP 01311-902 - São Paulo - SP - Brazil - Phone: (11) 3372-4544 - Fax: (11) 3372-4554