Radiologia Brasileira - Publicação Científica Oficial do Colégio Brasileiro de Radiologia
AMB - Associação Médica Brasileira CNA - Comissão Nacional de Acreditação
 Vol. 46 nº 3 - Maio / Jun. of 2013
Vol. 46 nº 3 - Maio / Jun. of 2013
|
QUAL É O SEU DIAGNÓSTICO?
|
|
|
|
|
Autho(rs): Vitor Frauches Souza1; Renato Testahy Chaves1; Victor Spinelli Balieiro1; Caroline Bastida de Paula2; Alair Augusto Sarmet Moreira Damas dos Santos3; Marcelo Souto Nacif4 |
|
|
Paciente de 58 anos de idade, do sexo feminino, com quadro clínico de dores musculares em membros superiores e inferiores associadas a dispneia leve e estertoração bibasal. Foi encaminhada ao Centro de Imagem do Hospital de Clínicas de Niterói para realização de tomografia computadorizada de alta resolução (TCAR) (Figuras 1, 2 e 3).
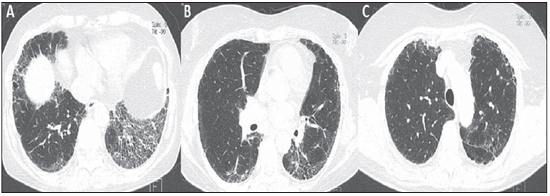 Figura 1. TCAR nos terços inferior (A), médio (B) e superior (C). 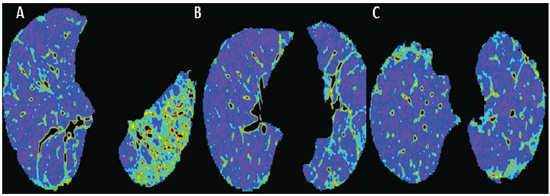 Figura 2. Mapa colorido em reformatação axial nos terços inferior (A), médio (B) e superior (C). 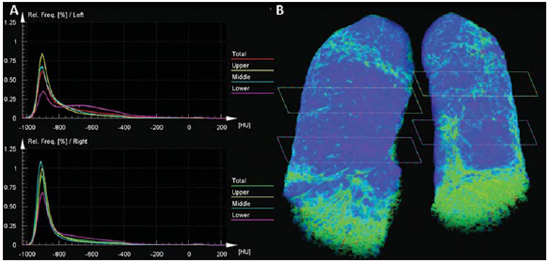 Figura 3. Gráfico de avaliação das densidades pulmonares nos terços superiores, médios e inferiores (A) e reformatação 3D dos pulmões com mapa colorido demonstrando as densidades relativas e os planos dos terços superior, médio e inferior (B). DESCRIÇÃO DAS IMAGENS Figura 1. TCAR nos terços inferior (A), médio (B) e superior (C) mostra discreta distorção da arquitetura pulmonar, com reticulado e sinais de fibrose (faveolamento) periféricos, entremeados a áreas de atenuação em vidro fosco e parênquima pulmonar relativamente normal. Notar o maior comprometimento das bases pulmonares, onde se observam bronquiolectasias de tração. Figura 2. Mapa colorido em reformatação axial nos terços inferior (A), médio (B) e superior (C) utilizando os algoritmos do software Syngo InSpace Lung Parenchyma Analysis da Siemens, em que a análise qualitativa (visual) realizada nas regiões de maior densidade, com aumento do espaço morto, estão representadas pelas cores amarelo/verde. Os tons de azul escuro representam áreas de parênquima normal com troca gasosa ainda preservada. Figura 3. Gráfico de avaliação das densidades pulmonares nos terços superiores, médios e inferiores (A) para análise quantitativa. Reformatação 3D dos pulmões com mapa colorido mostra as densidades relativas e os planos dos terços superior, médio e inferior (B). O software Syngo InSpace Lung Parenchyma Analysis da Siemens primeiramente facilita análise quantitativa pelo gráfico, em que a região basal inferior esquerda possui 50% menos parênquima preservado em relação à região superior do mesmo lado. Também é possível, através da reformatação 3D, realizar análise qualitativa. Notar que o pulmão direito mostra ser menos acometido pela doença e está mais expandido. Diagnóstico: Avaliação qualitativa e quantitativa da densidade pulmonar em paciente com polimiosite e fibrose pulmonar. COMENTÁRIOS A polimiosite é definida como uma miopatia idiopática que evolui durante semanas a meses e tem como característica principal o desenvolvimento de processo inflamatório não supurativo na musculatura esquelética, o qual se manifesta clinicamente por fraqueza muscular proximal e simétrica. Tem incidência de aproximadamente um caso a cada 100 mil habitantes, com predomínio em mulheres(1,2). A polimiosite pode ocorrer isoladamente ou estar associada a doenças sistêmicas autoimunes e infecções virais, a exemplo de lúpus, artrite reumatoide, doença de Crohn, infecções por HIV e HTLV(3,4). Nos adultos, o pico de incidência ocorre entre 40 e 50 anos, embora qualquer faixa etária possa ser afetada(5). Em 1975, Bohan e Peter formularam critérios de classificação, que incluem(5,6): fraqueza muscular proximal e simétrica, elevação sérica de enzimas musculares, eletromiografia com alterações miopáticas e alterações características na biópsia muscular com ausência de sinais histológicos de outras miopatias. O diagnóstico definitivo de polimiosite é estabelecido quando estão presentes os quatro critérios citados acima. Estão descritas três categorias de autoanticorpos miosite-específicos. Destes, os anticorpos antissinteta-se e anti-Jo-1 são os que estão fortemente associados a doença intersticial pulmonar. O envolvimento pulmonar e consequente comprometimento respiratório apresentamse em apenas 10% dos pacientes, podendo ocorrer de duas formas principais: na forma de doença intersticial pulmonar ou por fraqueza dos músculos respiratórios(6,7). A TCAR proporcionou grande avanço para o diagnóstico e acompanhamento destas situações clínicas. Os achados tomográficos incluem os decorrentes da pneumonia intersticial, que podem estar relacionados a doença fibrosante com reticulado periférico, bronquiectasias e bronquiolectasias de tração, faveolamento e mínimo vidro fosco, os quais usualmente possuem predomínio periférico, basal e posterior. Todavia, alguns casos evoluem com padrão de dano alveolar agudo, como no lúpus eritematoso sistêmico, em que se pode encontrar opacidades em vidro fosco difusas, pavimentação em mosaico e até consolidação, bilaterais(7). A TC pode demonstrar outros achados, geralmente relacionados a desmotilidade esofágica, que pode ser suspeitada quando existe dilatação ou hipotonia do esôfago com nódulos centrolobulares e consolidação predominando nas regiões pulmonares dependentes. Por outro lado, a elevação do diafragma com perda de volume pulmonar ocorre no envolvimento do músculo diafragmático(7). A análise qualitativa e quantitativa da densidade pulmonar por softwares dedicados pode auxiliar no diagnóstico e principalmente no acompanhamento de longo prazo dos pacientes com doença pulmonar crônica. Estes softwares poderão criar padrões de comparação individual, isto é, um primeiro exame pode ser utilizado como base comparativa para avaliação ao longo do tratamento ou de grupos, que poderá facilitar a definição de padrões da doença e critérios de classificação para a gravidade, de acordo com o percentual de densidade do parênquima pulmonar. No presente caso demonstramos que os resultados podem ser estratificados por terços (superior, médio e inferior) para caracterização da distribuição da doença. O software utilizado facilita a análise automática e tridimensional para quantificação da densidade pulmonar média, máxima e mínima, do volume pulmonar total e do volume percentual relativo. CONSIDERAÇÕES FINAIS Os avanços da TCAR e dos softwares de avaliação quantitativa e qualitativa facilitam a pesquisa clínica e acadêmica, pois são de fácil utilização e alta reprodutibilidade. A possibilidade da utilização de softwares de quantificação da densidade pulmonar poderá transformar os paradigmas do acompanhamento de pacientes com doença intersticial pulmonar. REFERÊNCIAS 1. Dalakas MC, Hohlfeld R. Polymyositis and dermatomyositis. Lancet. 2003;362:971-82. 2. Yazici Y, Kagen LJ. Clinical presentation of the idiopathic inflammatory myopathies. Rheum Dis Clin North Am. 2002;28:823-32. 3. Stefanidis I, Giannopoulou M, Liakopoulos V, et al. A case of membranous nephropathy associated with Sjögren syndrome, polymyositis and autoimmune hepatitis. Clin Nephrol. 2008;70:245-50. 4. Robert WJ, William PA. Renal disorders associated with systemic sclerosis, rheumatoid arthritis, Sjögren's syndrome and polymyositis-dermatomyositis. In: Schrier RW, editor. Diseases of the kidney & urinary tract. 8th ed. Philadelphia, PA: Lippincott, Williams & Wilkins; 2007. p. 1713-4. 5. Miller ML. Clinical manifestations and diagnosis of adult dermatomyositis and polymyositis. UpToDate, 2008. 6. Betteridge Z, Gunawardena H, North J, et al. Antisynthetase syndrome: a new autoantibody to phenylalanyl transfer RNA synthetase (anti-Zo) associated with polymyositis and interstitial pneumonia. Rheumatology. 2007;46:1005-8. 7. Silva CIS, Müller NL. Manifestações intratorácicas das doenças do colágeno na tomografia computadorizada de alta resolução do tórax. Radiol Bras. 2008;41:189-97. 1. Especializandos em Radiologia e Diagnóstico por Imagem pelo Instituto de Pós-Graduação Médica Carlos Chagas (IPGMCC), Rio de Janeiro, RJ, Brasil. 2. Application Specialist Siemens Healthcare, São Paulo, SP, Brasil. 3. Professor Titular do Curso de Radiologia e Diagnóstico por Imagem do Instituto de Pós-Graduação Médica Carlos Chagas (IPGMCC), Rio de Janeiro, RJ, Coordenador do Centro de Imagem do Hospital de Clínicas de Niterói (HCN), Niterói, RJ, Brasil. 4. Médico Radiologista do Hospital de Clínicas de Niterói (HCN), Professor Adjunto do Departamento de Radiologia da Faculdade de Medicina da Universidade Federal Fluminense (UFF), Niterói, RJ, Brasil. Endereço para correspondência: Dr. Vitor Frauches Souza Rua Humberto de Campos, 746/301, Leblon Rio de Janeiro, RJ, Brasil, 22430-190 E-mail: drvitorfrauches@gmail.com Trabalho realizado no Hospital de Clínicas de Niterói (HCN), Niterói, RJ, Brasil. |
|
GN1© Copyright 2025 - All rights reserved to Colégio Brasileiro de Radiologia e Diagnóstico por Imagem
Av. Paulista, 37 - 7° andar - Conj. 71 - CEP 01311-902 - São Paulo - SP - Brazil - Phone: (11) 3372-4544 - Fax: (11) 3372-4554
Av. Paulista, 37 - 7° andar - Conj. 71 - CEP 01311-902 - São Paulo - SP - Brazil - Phone: (11) 3372-4544 - Fax: (11) 3372-4554