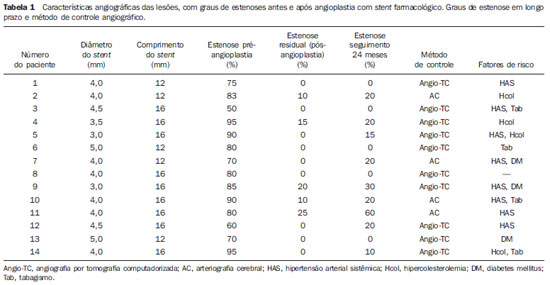
INTRODUÇÃO
Aproximadamente 25% dos acidentes vasculares cerebrais isquêmicos envolvem a circulação posterior, sendo a estenose da artéria vertebral responsável por até 20% destes(1,2). Em muitos pacientes esta isquemia é relacionada a alterações hemodinâmicas decorrentes de obstrução proximal da artéria vertebral. Em pacientes sintomáticos e que não respondem a terapia medicamentosa com dupla antiagregação, a angioplastia com balão tem sido relatada ser benéfica. Até o momento, o tratamento da estenose da artéria vertebral com colocação de
stent tem sido quase sempre realizado com próteses vasculares coronarianas convencionais(3,4) e associado a taxas de reestenose que variam de 9,6% até 66,7% (Tabela 1)(1,3,49). O conceito para a utilização de um
stent farmacológico é baseado no uso de revestimentos com drogas citotóxicas sobre o
stent (plataforma) para inibir a ocorrência de reestenose vascular devido a hiperplasia intimal. Estudos clínicos de tratamento da estenose das artérias coronárias têm demonstrado superioridade dos
stents farmacológicos quando comparados com os
stents convencionais(8,10).
Nesta série são relatados nossos resultados no tratamento de 14 pacientes consecutivos com isquemia do território vertebrobasilar consequente a estenose da artéria vertebral extracraniana e que foram tratados com implante de
stent farmacológico com paclitaxel.
MATERIAIS E MÉTODOS
Foram revisados os prontuários e estudos angiográficos de 14 pacientes referidos para a equipe de neurorradiologia intervencionista do Hospital Universitário Clementino Fraga Filho da Universidade Federal do Rio de Janeiro, para o tratamento de lesões vasculares que envolvem as artérias vertebrais e que foram tratados com
stents revestidos com paclitaxel, no período de junho de 2008 a abril de 2011. Os critérios de inclusão foram os seguintes: a) pacientes com evidência angiográfica de estenose da artéria vertebral
> 50%; b) sintomas de isquemia vertebrobasilar refratária a tratamento medicamentoso caracterizada por acidente vascular cerebral ou ataque isquêmico transitório, durante o uso de medicação antiplaquetária e com controle de fatores de risco; c) consentimento informado assinado.
Inicialmente, os pacientes eram selecionados através de um estudo por angiotomografia ou angiorressonância magnética. Quando selecionados, a angiografia digital era realizada apenas no momento do tratamento, para confirmação dos achados e do grau de estenose.
Os pacientes do estudo apresentavam sintomas relacionados a isquemia da circulação posterior, refratários ao tratamento clínico, incluindo o uso de antiplaquetário oral. Os estudos de angiografia foram reavaliados para análise quantitativa das lesões, a qual foi realizada por meio de análise computadorizada através de
software próprio integrado ao sistema de angiografia (Quantcor; Siemens Medical Solutions, Forchheim, Alemanha).
O estudo angiográfico por cateter era realizado, incluindo as artérias subclávias, vertebrais e carótidas, também para determinar a extensão da doença vascular e avaliar a presença de circulação colateral através das artérias comunicantes posteriores. O tempo de coagulação ativado (TCA) era obtido antes do início do procedimento angiográfico. Após punção arterial, era feito
bolus de heparina intravenosa 80 U/kg de peso corporal, com o propósito de elevar a duas vezes e meia o valor basal do TCA, ou > 250 segundos. Os pacientes, em seguida, eram submetidos ao procedimento sob sedação consciente. O acesso vascular era obtido mediante punção da artéria femoral, com utilização de bainha 6 ou 7 Fr. Um cateter-guia Guider Soft Tip 6 ou 7 Fr (Boston Scientific; Natick, MA, EUA) era então cuidadosamente posicionado proximalmente à lesão a ser tratada. A lesão era então ultrapassada com fio-guia 0,014 Transend EX (Boston Scientific; Irvine, CA, EUA), por vezes em combinação de um microcateter 1,7 Fr SL10 (Boston Scientific; Irvine, CA, EUA). Quando necessário, era utilizado um microguia de troca Transend Platinum 300 cm (Boston Scientific; Irvine, CA, EUA) para colocação do
stent. No caso de estenose severa (> 80%), era utilizada angioplastia com cateter balão para pré-dilatação da lesão, a fim de permitir posterior passagem do
stent. O procedimento terapêutico foi realizado em todos os casos com o uso do
stent Taxus Express Monorail (Boston Scientific; Irvine, CA, EUA) coronário, com plataforma de liberação de paclitaxel. Não foi utilizado filtro de proteção cerebral. Após a inserção do
stent e antes de sua liberação, uma aquisição angiográfica era realizada para determinar a localização exata do
stent na lesão. Nos casos de lesão ostial, o
stent era colocado de modo que um segmento curto de cerca de 2 mm ficasse saliente para a porção mais inferior do óstio da artéria vertebral, para cobrir completamente a placa aterosclerótica. O
stent era implantado por meio de lenta inflação controlada do balão de angioplastia. A administração de heparina era interrompida no final do processo, sem reversão. Os pacientes foram mantidos em um regime oral de ticlopidina (500 mg/dia) ou clopidogrel (75 mg via oral/dia) por três meses e por tempo indeterminado com aspirina (200 mg/dia). Além disso, eram controlados os fatores de risco associados ao paciente, com controle estrito da hipercolesterolemia e da hiperglicemia, além de tratamento adjuvante para o tabagismo nos pacientes com adesão ao tratamento. Os pacientes eram posteriormente acompanhados com Doppler, angiografia digital ou angiografia por tomografia computadorizada até 24 meses da colocação do
stent.
RESULTADOS
Foram incluídos no estudo 14 pacientes, sendo 5 do sexo feminino e 9 do sexo masculino, com idade média de 67,2 anos (variando de 49 a 87 anos). Entre as comorbidades relacionadas, 8 dos 14 pacientes (57,1%) apresentavam hipertensão arterial, 4 (28,6%) tinham hipercolesterolemia, 3 (21,4%) eram portadores de diabetes mellitus, 3 (21,4%) tinham doença coronariana e 4 (28,6%) eram tabagistas. Cinco dos 14 pacientes (35,7%) apresentaram infarto encefálico de evolução aguda ou subaguda no território da circulação posterior, evidenciado por tomografia computadorizada ou por ressonância magnética.
Características das lesões avaliadas nas imagens angiográficas obtidas logo antes do implante de
stent evidenciaram um grau inicial de estenose variando de 50% a 95% (média de 78,8%). O comprimento do segmento estenótico variou de 1,4 a 25,7 mm (média de 5,2 mm).
As medições de diâmetro, incluindo o local da estenose mais severa, foram obtidas diretamente da angiografia na posição de trabalho pré-angioplastia. Em relação à distribuição das lesões na artéria vertebral, a maioria (57,14%) estava localizada no óstio arterial, 14,2% no segmento V2, 7,1% no segmento V3 e 21,4% no segmento V4. A doença aterosclerótica ostial, em geral, se devia a uma extensão de uma placa aterosclerótica da artéria subclávia. O grau de estenose arterial antes e imediatamente após a colocação do
stent, tal como aos 24 meses de seguimento, além dos diâmetros e comprimentos dos
stents utilizados e a avaliação do grau de reestenose intra-
stent, estão disponíveis na Tabela 1.
Os procedimentos de angioplastia e implante de
stent foram tecnicamente bem sucedidos em todos os pacientes. Em todos os casos foi utilizado o
stent Taxus Express Monorail (Boston Scientific; Irvine, CA, EUA) revestido com paclitaxel. Não ocorreram complicações permanentes relacionadas ao procedimento. O grau de estenose residual medido nas imagens angiográficas obtidas imediatamente após a colocação do
stent variou de 0% a 20% (média de 5,7%), sendo que nenhum paciente apresentou estenose residual maior que 25% do lúmen arterial. Tanto a morbidade neurológica permanente quanto a mortalidade relacionadas ao procedimento em 30 dias de seguimento foram de 0%. Apenas um paciente (7,1%) apresentou ataque isquêmico transitório dentro de 24 horas do procedimento (paciente 11). Não houve acidente vascular cerebral relacionado ao território tratado durante o procedimento (0%). Em apenas um caso foi observada dissecção intimal decorrente de angioplastia (paciente 4), que foi tratada com o implante de
stent adicional.
Imediatamente após o procedimento era realizada avaliação neurológica, que era repetida aos 15 e 30 dias e no máximo de seguimento (média de 24 meses). A maioria dos pacientes (71,4%) era sintomática antes do procedimento e apresentou melhora dos seus sintomas relacionados ao hipofluxo encefálico. Também não foram detectados novos episódios isquêmicos após o procedimento.
Seguimento angiográfico durante longo prazo foi obtido em todos os 14 pacientes. Antes da colocação do
stent, todos os pacientes tinham estenose de pelo menos 50%. Imediatamente após a colocação do
stent, nenhum paciente apresentou estenose residual de 50% ou mais. A estenose residual média imediatamente após o procedimento foi de 5,7%. Aos 24 meses de seguimento, esta taxa de estenose média se elevou para 12,5%, porém, apenas um paciente se mostrou com estenose hemodinamicamente significativa, maior que 50%. Esta incidência de reestenose significativa aos 24 meses de seguimento foi de 7,1%, embora este paciente também não apresentasse recorrência dos sintomas vertebrobasilares.
Casos ilustrativos
Paciente 4 Homem de 63 anos, com antecedentes de hipertensão e hiperlipidemia, apresentou episódios de ataques isquêmicos transitórios manifestos por deficiências do campo visual. Ele foi tratado de forma conservadora com dupla antiagregação plaquetária, mas desenvolveu um acidente vascular cerebral acometendo o hemisfério cerebelar e o lobo occipital esquerdos dois meses mais tarde, que o deixou com uma quadrantanopia residual (Figura 1A). O paciente foi submetido a angiorressonância magnética, que revelou presença de uma lesão na artéria vertebral esquerda. A angiografia digital pré-angioplastia evidenciou uma placa ateromatosa excêntrica e irregular que determinava estenose de cerca de 95% (Figura 1B). Para a terapêutica, um cateter-guia 6F foi posicionado na artéria subclávia, e um
stent Taxus 3,5 × 16 mm (Boston Scientific; Irvine, CA, EUA) foi implantado sobre a lesão. A angiografia revelou melhora acentuada do fluxo para a artéria vertebral distal e para a circulação posterior, sem estenose residual (Figura 1C). O paciente recebeu alta hospitalar em terapia antiplaquetária e manteve-se assintomático em 26 meses de acompanhamento neurológico.
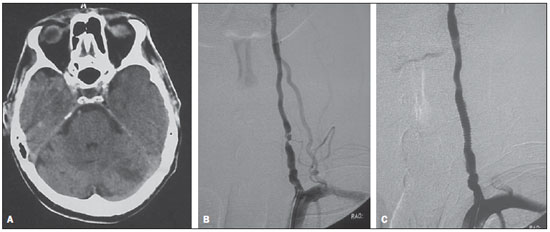
Figura 1. A: Tomografia computadorizada de crânio demonstrando lesões hipodensas em ambos os hemisférios cerebelares, a maior no hemisfério esquerdo. B: Angiografia digital vertebral esquerda demonstrando uma lesão aterosclerótica em seu segmento V2, estimada em 95%. C: Angiografia digital vertebral esquerda pós-angioplastia, sem estenose residual.
Homem de 54 anos, com doença arterial coronariana, se apresentou ao setor de emergência do hospital com síndrome vertiginosa associada a vômitos. A ressonância magnética do crânio revelou lesões isquêmicas puntiformes em ambos os hemisférios cerebelares, sugerindo a origem embólica das lesões (Figura 2A). O estudo por Doppler das artérias carótidas e vertebrais sugeriu uma estenose severa, maior que 90%, na artéria vertebral direita. Os achados da angiografia digital realizada antes da angioplastia corroboraram este diagnóstico (Figura 2B), evidenciando uma lesão ateromatosa extensa e que determinava estenose de 90% do óstio da artéria vertebral esquerda. Foi realizada angioplastia com implante de
stent Taxus 3,0 × 16 mm (Boston Scientific; Irvine, CA, EUA), com excelente resultado angiográfico e sem evidência de lesão residual pós-angioplastia (Figura 2C). O estudo de controle por angiotomografia computadorizada aos 12 meses revelou mínima estenose intra-
stent, estimada em 15%, assintomática.
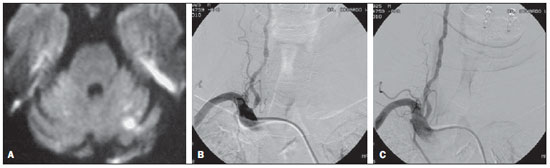
Figura 2. A: Ressonância magnética, com sequência ponderada em difusão (DW), demonstrando foco isquêmico agudo no cerebelo. B: Angiografia digital préangioplastia revelando lesões nos segmentos V1 e V2 da artéria vertebral direita. C: Angiografia digital revelando aspecto angiográfico final após a angioplastia.
Homem de 62 anos, tabagista de 50 maços-ano e com antecedentes de hipertensão arterial sistêmica, diabetes mellitus e doença vascular periférica, apresentou ataques isquêmicos transitórios manifestos com síndrome vertiginosa e diplopia. O paciente foi submetido a angiografia digital diagnóstica, que revelou lesão de 95% do óstio da artéria vertebral esquerda associada a 85% de estenose da artéria subclávia proximal à origem da artéria vertebral (Figura 3A). A artéria vertebral esquerda era a dominante. Foi realizado cateterismo da artéria subclávia esquerda e implantado um
stent Taxus 4 × 16 mm (Boston Scientific; Irvine, CA, EUA) no óstio da artéria vertebral esquerda. Posteriormente, foi realizada angioplastia da artéria subclávia com balão Powerflex 7 × 20 mm (Cordis; Warren, NJ, EUA). A angiografia pós-angioplastia mostrou resolução da estenose na origem da artéria vertebral subclávia esquerda, com excelente fluxo anterógrado nesta e estenose residual na artéria subclávia (Figura 3B). O paciente anotou melhora imediata em seus sintomas após o procedimento e manteve-se assintomático em 18 meses de acompanhamento, com mínima estenose intra-
stent, estimada em 10%.
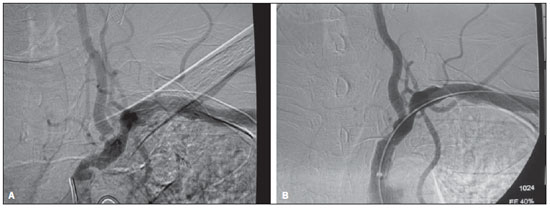
Figura 3. A: Angiografia digital subclávia esquerda revelando lesão ostial estimada em 95% na artéria vertebral esquerda associada a lesão obstrutiva da artéria subclávia. B: Aspecto angiográfico final após angioplastias do óstio da artéria vertebral e da artéria subclávia.
A análise de nossa população identifica a hipertensão como fator de risco mais comum de acometimento aterosclerótico severo do sistema vertebrobasilar, seguido pelo tabagismo e pela hipercolesterolemia.
O mecanismo da isquemia vertebrobasilar pode ser embólico ou hemodinâmico. Causas embólicas de isquemia vertebrobasilar são embolização distal de placas ou lesões das artérias subclávia, vertebral e/ou basilar(3,7,11). Para sintomas hemodinâmicos ocorrerem, doença substancial deve estar presente em ambas as artérias vertebrais, e o polígono de Willis deve estar incompleto. Embora esse mecanismo ainda não esteja completamente elucidado, a análise de microêmbolos na circulação posterior revela que a maioria é o resultado de doença cardíaca coexistente, sem correlação com distúrbio do sistema vertebrobasilar(2). Além disso, a maioria das causas relacionadas com a isquemia da circulação posterior é relacionada ao comprometimento hemodinâmico, em contraste com a doença carotídea, em que os êmbolos são a principal fonte de acidente vascular cerebral na circulação anterior. Alternativamente, pode ocorrer isquemia hemodinâmica com estenose da artéria subclávia proximal, levando a uma síndrome do roubo da subclávia. Alguns estudos questionam os benefícios do tratamento endovascular da estenose da artéria vertebral quando comparado com a terapia medicamentosa(12). Na prática clínica, a reconstrução vascular por meio cirúrgico ou endovascular já foi considerada uma opção razoável para melhorar o aporte sanguíneo em pacientes com insuficiência vertebrobasilar. Porém, atualmente, para pacientes com estenose vertebral sintomática refratária ao tratamento medicamentoso não há nenhuma boa razão para recusar o procedimento minimamente invasivo.
Nosso estudo mostra que o uso de
stents farmacológicos em pacientes com estenose da artéria vertebral é viável e benéfico na prevenção da isquemia vertebrobasilar recorrente e da reestenose vascular. A avaliação do valor clínico da angioplastia e colocação de
stent no tratamento da estenose da artéria vertebral exigiria comparação com o tratamento medicamentoso em um maior estudo controlado randomizado. A experiência atual com angioplastia e colocação de
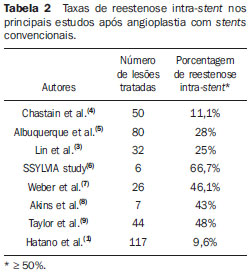
stent no tratamento da estenose vertebral é atualmente quase que exclusivamente com base no uso do
stents convencionais(1,39) (Tabela 2). A reestenose do vaso em que o
stent foi colocado, no seguimento angiográfico, é geralmente definida como um grau de estreitamento luminal de pelo menos 50%(13).
Em um estudo retrospectivo de Gupta et al.(14) foi relatado o uso de
stents farmacológicos no tratamento endovascular de 27 lesões da artéria vertebral. Dois tipos de
stents foram usados: Cypher
®(Cordis; Miami, FL, EUA) e Taxus Express
®(Boston Scientific; Irvine, CA, EUA). Depois de um período de acompanhamento de quatro meses, 7% das lesões tinham reestenose de pelo menos 50%(14). No presente estudo, a taxa de reestenose vascular significativa foi de 7,1% aos 24 meses de seguimento clínico e angiográfico. Estes resultados aparentemente foram bastante superiores aos resultados que seriam obtidos caso
stents convencionais tivessem sido utilizados.
Indubitavelmente, os
stents farmacológicos foram considerados um grande avanço para a prática médica. Os medicamentos liberados por esses
stents reduzem o risco de reestenose, inibindo o acúmulo de macrófagos e a proliferação de células musculares lisas ao redor do stent. No entanto, como tais ações também inibem a reendotelização da superfície do stent(15,16), era temido que estes efeitos aumentassem o risco de trombose tardia do
stent, porém o tratamento com antiagregantes plaquetários parece desempenhar um grande papel na redução do risco desta trombose(17,18). Além disso, estudos sobre os resultados clínicos em longo prazo dos pacientes contribuíram para confirmar os benefícios na sobrevida de
stents coronários farmacológicos quando comparados aos
stents convencionais em até cinco anos de seguimento e não mostraram diferença no risco de trombose tardia do
stent(1720).
É sabido que fatores morfológicos das lesões da artéria vertebral podem afetar o resultado da terapia de angioplastia com
stent. Por exemplo, a extensão da lesão afeta a taxa de reestenose(3,21) e uma tortuosidade vascular excessiva pode impedir o implante do
stent. Em nosso estudo, qualquer comprimento de lesão era incluído e tortuosidade vascular não era considerada critério de exclusão.
Nosso estudo apresenta algumas limitações, principalmente quanto ao pequeno número de pacientes incluídos, entretanto, é suficiente como um estudo de viabilidade. Uma taxa maior de reestenose tardia ocorreu principalmente quando se detectava estenose residual ao término do procedimento. Desta forma, a estenose residual imediatamente após o implante de
stent em estenose da artéria vertebral parece ser um preditor de reestenose no seguimento, embora a importância deste achado sobre o desfecho clínico ainda deva ser esclarecida.
Embora a dose do fármaco liberado na circulação seja pequena e não haja evidências de neurotoxicidade induzida por paclitaxel, o risco potencial de neurotoxicidade que resulta da colocação de um
stent com paclitaxel em um território neurovascular continua sendo uma preocupação que precisa ser avaliada cautelosamente(2224).
A doença extracraniana da artéria vertebral é difícil de diagnosticar e acompanhar com técnicas não invasivas como ultrassonografia com Doppler, e seu tratamento não é tão bem definido quanto a doença vascular carotídea. Para avaliação inicial, portanto, utilizou-se a angiografia por tomografia computadorizada ou ressonância magnética para triagem, antes de realizar a angiografia digital, de modo a evitar o gasto desnecessário e expor os pacientes aos riscos da angiografia. Entretanto, o uso da angiografia por tomografia computadorizada não seria suscetível de resultar em viés de seleção dos pacientes, porque existe uma tendência para este método de exagerar o grau de estenose vascular(25). Embora o uso de clopidogrel por um ano inteiro tenha sido recomendado em doentes com doença coronária após implante de
stent farmacológico, tem sido prática comum em nossa instituição administrar a aspirina e clopidogrel por seis meses e aspirina sozinha ininterruptamente em pacientes que recebem
stents em artéria carótida vertebral, ou em localização intracraniana.
A correção cirúrgica das lesões na origem da artéria vertebral e da artéria subclávia, com endarterectomia vertebral ostial, endarterectomia de subclávia, ou reimplante da artéria vertebral na artéria subclávia ou da artéria carótida, é tecnicamente difícil. Em sua série de 325 lesões tratadas cirurgicamente em 290 pacientes, Thevenet et al.(26) relataram baixa taxa de mortalidade, de apenas 0,6%, porém taxa relativamente alta de síndrome de Horner pós-operatória (28%), uma complicação inexistente na terapia percutânea. Embora tenham sido relatados bons resultados em longo prazo, eles são associados a uma taxa relativamente alta de morbidade peroperatória(3,26).
CONCLUSÕES
Os resultados da presente série clínica retrospectiva sugerem que a angioplastia e colocação de
stents farmacológicos com paclitaxel em pacientes sintomáticos portadores de estenose da artéria vertebral é viável e promissora em termos de potencial de segurança e eficácia na prevenção da isquemia recorrente e da reestenose. Embora um seguimento clínico e angiográfico em longo prazo seja necessário para avaliar a durabilidade da permeabilidade do
stent, a evolução clínica neste grupo de doentes sugere um benefício contínuo do processo. Para tal, seria necessária a realização de um maior estudo randomizado e controlado.
REFERÊNCIAS
1. Hatano T, Tsukahara T, Miyakoshi A, et al. Stent placement for atherosclerotic stenosis of the vertebral artery ostium: angiographic and clinical outcomes in 117 consecutive patients. Neurosurgery. 2011;68:10816.
2. Caplan LR, Amarenco P, Rosengart A, et al. Embolism from vertebral artery origin occlusive disease. Neurology. 1992;42:150512.
3. Lin YH, Juang JM, Jeng JS, et al. Symptomatic ostial vertebral artery stenosis treated with tubular coronary
stents: clinical results and restenosis analysis. J Endovasc Ther. 2004;11:71926.
4. Chastain HD 2nd, Campbell MS, Iyer S, et al. Extracranial vertebral artery stent placement: in-hospital and follow-up results. J Neurosurg. 1999;91:54752.
5. Albuquerque FC, Fiorella D, Han P, et al. A reappraisal of angioplasty and stenting for the treatment of vertebral origin stenosis. Neurosurgery. 2003;53:60716.
6. SSYLVIA Study Investigators. Stenting of Symptomatic Atherosclerotic Lesions in the Vertebral or Intracranial Arteries (SSYLVIA): study results. Stroke. 2004;35:138892.
7. Weber W, Mayer TE, Henkes H, et al. Efficacy of stent angioplasty for symptomatic stenoses of the proximal vertebral artery. Eur J Radiol. 2005;56:2407.
8. Akins PT, Kerber CW, Pakbaz RS. Stenting of vertebral artery origin atherosclerosis in high-risk patients: bare or coated? A single-center consecutive case series. J Invasive Cardiol. 2008;20:1420.
9. Taylor RA, Siddiq F, Suri MF, et al. Risk factors for in-stent restenosis after vertebral ostium stenting. J Endovasc Ther. 2008;15:20312.
10. Virmani R, Guagliumi G, Farb A, et al. Localized hypersensitivity and late coronary thrombosis secondary to a sirolimus-eluting stent: should we be cautious? Circulation. 2004;109:7015.
11. Burnay J, Pietri J. Vertebral and subclavian reimplantation into the common carotid artery with widening angioplasty on the vertebral ostium. Presse Med. 1986;15:580.
12. Wehman JC, Hanel RA, Guidot CA, et al. Atherosclerotic occlusive extracranial vertebral artery disease: indications for intervention, endovascular techniques, short-term and long-term results. J Interv Cardiol. 2004;17:21932.
13. Biria M, Tadros P, Gupta K. Subclavian-vertebral artery bifurcation stenting using drug-eluting
stents: a report of two cases using different techniques. J Invasive Cardiol. 2007;19:E1569.
14. Gupta R, Al-Ali F, Thomas AJ, et al. Safety, feasibility, and short-term follow-up of drug-eluting stent placement in the intracranial and extracranial circulation. Stroke. 2006;37:25626.
15. Vajda Z, Miloslavski E, Güthe T, et al. Treatment of stenoses of vertebral artery origin using short drug-eluting coronary stents: improved follow-up results. AJNR Am J Neuroradiol. 2009;30:16536.
16. Yu SC, Leung TW, Lam JS, et al. Symptomatic ostial vertebral artery stenosis: treatment with drug-eluting stentsclinical and angiographic results at 1-year follow-up. Radiology. 2009;251:22432.
17. Regar E, Serruys PW. The Ravel trial. Zero percent restenosis: a cardiologists dream comes true! Rev Esp Cardiol. 2002;55:45962.
18. Dabus G, Gerstle RJ, Derdeyn CP, et al. Endovascular treatment of the vertebral artery origin in patients with symptoms of vertebrobasilar ischemia. Neuroradiology. 2006;48:91723.
19. Du B, Wong EH, Jiang WJ. Long-term outcome of tandem stenting for stenoses of the intracranial vertebrobasilar artery and vertebral ostium. AJNR Am J Neuroradiol. 2009;30:8404.
20. Morice MC, Serruys PW, Barragan P, et al. Long-term clinical outcomes with sirolimus-eluting coronary stents: five-year results of the RAVEL trial. J Am Coll Cardiol. 2007;50:1299304.
21. Zhou Z, Yin Q, Xu G, et al. Influence of vessel size and tortuosity on in-stent restenosis after stent implantation in the vertebral artery ostium. Cardiovasc Intervent Radiol. 2011;34:4817.
22. Pace A, Bove L, Aloe A, et al. Paclitaxel neurotoxicity: clinical and neurophysiological study of 23 patients. Ital J Neurol Sci. 1997;18:739.
23. Pace A, Nisticò C, Cuppone F, et al. Peripheral neurotoxicity of weekly paclitaxel chemotherapy: a schedule or a dose issue? Clin Breast Cancer. 2007;7:5504.
24. van Gerven JM, Moll JW, van den Bent MJ, et al. Paclitaxel (Taxol) induces cumulative mild neurotoxicity. Eur J Cancer. 1994;30A:10747.
25. Yoo WJ, Lim YS, Ahn KJ, et al. Assessment of vertebral artery stents using 16-slice multi-detector row CT angiography in vivo evaluation: comparison of a medium-smooth kernel and a sharp kernel. Eur J Radiol. 2009;70:3628.
26. Thevenet A, Ruotolo C. Surgical repair of vertebral artery stenoses. J Cardiovasc Surg (Torino). 1984;25:10110.
1. Mestre, Médico Neurorradiologista do Hospital Universitário Clementino Fraga Filho da Universidade Federal do Rio de Janeiro (UFRJ), Rio de Janeiro, RJ, Brasil.
2. Mestre, Médico Neurologista do Hospital Universitário Antônio Pedro da Universidade Federal Fluminense (UFF), Niterói, RJ, Brasil.
3. Doutor, Professor Assistente da Faculdade de Medicina de Ribeirão Preto da Universidade de São Paulo (FMRPUSP), Ribeirão Preto, SP, Brasil.
Endereço para correspondência:
Dr. Eduardo Wajnberg
Rua Nina Rodrigues, 72/102, Jardim Botânico
Rio de Janeiro, RJ, Brasil, 22461-100
E-mail: eduardowj@gmail.com
Recebido para publicação em 1/8/2011.
Aceito, após revisão, em 10/10/2011.
* Trabalho realizado no Hospital Universitário Clementino Fraga Filho da Universidade Federal do Rio de Janeiro (UFRJ), Rio de Janeiro, RJ, Brasil.
 Vol. 44 nº 6 - Nov. / Dez. of 2011
Vol. 44 nº 6 - Nov. / Dez. of 2011