Paciente de 16 anos de idade, do sexo masculino, assintomático, apresentou sopro na ausculta cardíaca que na avaliação pelo ecocardiograma demonstrou estar relacionado a alteração morfofuncional no aparelho valvar do coração direito. O paciente foi encaminhado para a realização de ressonância magnética do coração (RMC).
Descrição das imagens
Figura 1. Aquisições acopladas ao eletrocardiograma (ECG), em cine-RM (SSFP), no eixo longo quatro câmaras. (
A) diástole, (
B) sístole e (
C) diástole média. Observar o deslocamento para o interior do ventrículo direito do aparelho valvar tricúspide, com aumento do volume do átrio direito e fusão parcial dos folhetos ao músculo cardíaco septal. Isso provoca uma deformidade no ápice do ventrículo esquerdo.
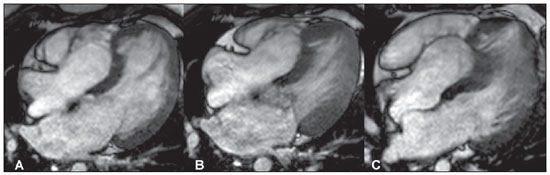
Figura 1. Aquisições acopladas ao eletrocardiograma (ECG), em cine-RM (SSFP), no eixo longo quatro câmaras. (A) diástole, (B) sístole e (C) diástole média.
Aquisições acopladas ao ECG. Realce tardio nos eixos longo quatro câmaras. (
A) e (
B) diferentes planos. Observar o realce tardio positivo no septo interventricular junto à porção média.
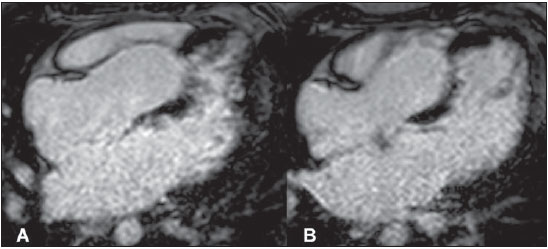
Figura 2. Aquisições acopladas ao ECG. Realce tardio nos eixos longo quatro câmaras. (A) e (B), diferentes planos.
Anomalia de Ebstein com fibrose septal.
COMENTÁRIOS
Há mais de 20 anos a RMC vem sendo utilizada como método de referência no estudo de cardiopatias congênitas, principalmente do ventrículo direito. A capacidade de se obter um estudo funcional com medidas de fluxo e gradiente associado a um estudo anatômico do coração e dos grandes vasos possibilita uma avaliação quase completa para o planejamento cirúrgico e acompanhamento dos pacientes(1,2).
A anomalia de Ebstein é uma cardiopatia congênita rara encontrada em apenas 0,51% dos casos em autópsias e pode causar cianose ao nascimento. Esta anomalia é marcada pela malformação da valva tricúspide associada ao deslocamento desta em direção ao ápice do ventrículo direito (atrialização)(1,2).
A evolução do quadro clínico é variada e dependente do grau de disfunção e malformação valvar. Usualmente, no período neonatal a causa mais comum de morte é por insuficiência cardíaca grave. Após o período neonatal, os achados mais frequentes são fadiga e arritmias. As arritmias tendem a ter uma incidência maior por anomalias no sistema de condução elétrico cardíaco, gerando com certa frequência casos de Wolff-Parkinson-White, batimentos prematuros ventricular ou atrial, ou presença de
flutter/fibrilação atrial. Apesar do padrão de acometimento do ventrículo direito, o lado esquerdo também pode ser acometido. Isto ocorre principalmente por anormalidades da valva mitral e de contratilidade do ventrículo esquerdo(2,3).
A possibilidade de coexistência com outras cardiopatias congênitas, que podem afetar o esqueleto cardíaco ou a mecânica funcional do coração, como a comunicação interatrial, a estenose da valva pulmonar, a atresia pulmonar ou a não compactação miocárdica, entre outras, faz da RMC o método não invasivo de diagnóstico a ser realizado antes de qualquer procedimento terapêutico(1,4,5).
O estudo volumétrico das câmaras cardíacas deve ser feito por um método reprodutível, com baixa variabilidade entre observadores e sem riscos para os pacientes, principalmente exposição à radiação, pois muitos necessitarão de estudos de controle ao longo da vida(1).
O estudo do realce tardio miocárdico pela RMC possibilita a detecção de áreas de fibrose no tecido miocárdico. Recentemente, Nakamura et al.(5) relataram a presença de fibrose miocárdica na porção atrializada do ventrículo direito em um paciente de 69 anos. No presente caso, foi identificado o mesmo achado porém em um paciente com 16 anos de idade. Entretanto, não se sabe a implicação clínica relacionada à sobrevida de pacientes com anomalia de Ebstein que apresentem fibrose quando crianças ou jovens.
Nos casos em que o diagnóstico é realizado tardiamente, o achado de imagem mais característico é a desproporção entre as cavidades direita e esquerda (Figura 3).
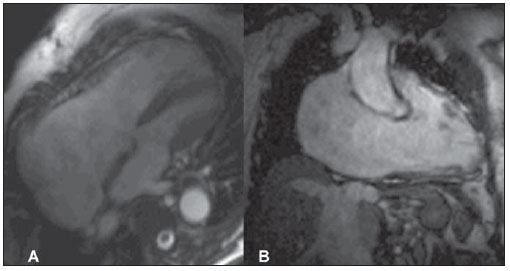
Figura 3. Aquisições acopladas ao ECG, em cine-RM (SSFP), no eixo longo quatro câmaras (A) e eixo longo duas câmaras do ventrículo direito (B). Observar a grande dilatação do átrio e ventrículo direitos. Exame realizado no Hospital Pro-Cardíaco, Rio de Janeiro, RJ, Brasil.
Existem diversas formas de tratamento da anomalia de Ebstein. No período neonatal, quando a anomalia é muito severa e o paciente permanece cianótico mesmo com terapia medicamentosa e ventilatória agressiva, o transplante é a melhor opção. No entanto, este tem sido realizado com pouco sucesso em razão do reduzido tamanho dos pulmões. Uma vez fora do período neonatal, as opções de tratamento aumentam. Por muitos anos o tratamento de escolha era apenas a troca da valva tricúspide associada à redução da porção atrializada do ventrículo direito. Recentemente, a técnica do cone tem sido mais utilizada. Para este procedimento é criada uma estrutura tipo túnel com a valva tricúspide, para ajudar a minimizar a regurgitação pós-procedimento. O defeito do septo interatrial, se presente, é fechado e o tamanho do átrio direito é reduzido. Durante o ato cirúrgico, torna-se necessário reduzir o número de prováveis circuitos patológicos de condução elétrica(2,612).
Considerações finais
O tratamento cirúrgico tem sido proposto em inúmeros casos(6,7,911), porém evidências clínicas associadas à utilização da RMC na estratificação pré-cirúrgica irão facilitar o entendimento do desfecho clínico dos pacientes com anomalia de Ebstein.
A RMC é um exame fundamental, impactando no diagnóstico não invasivo préintervenção e auxiliando no acompanhamento pós-intervenção. Acreditamos que sua utilização influenciará a sobrevida, principalmente dos pacientes que se submeterão a intervenções eletrofisiológicas.
REFERÊNCIAS
1. Yalonetsky S, Tobler D, Greutmann M, et al. Cardiac magnetic resonance imaging and the assessment of ebstein anomaly in adults. Am J Cardiol. 2011;107:76773.
2. Link KM, Herrera MA, DSouza VJ, et al. MR imaging of Ebstein anomaly: results in four cases. AJR Am J Roentgenol. 1988;150:3637.
3. Beerepoot JP, Woodard PK. Case 71: Ebstein anomaly. Radiology. 2004;231:74751.
4. Bagur RH, Lederlin M, Montaudon M, et al. Images in cardiovascular medicine. Ebstein anomaly associated with left ventricular noncompaction. Circulation. 2008;118:e6624.
5. Nakamura I, Kotooka N, Komori Y, et al. Ebstein anomaly by cardiac magnetic resonance imaging. J Am Coll Cardiol. 2009;53:1568.
6. Brown ML, Dearani JA, Danielson GK, et al. Functional status after operation for Ebstein anomaly: the Mayo Clinic experience. J Am Coll Cardiol. 2008;52:4606.
7. Brown ML, Dearani JA, Danielson GK, et al. The outcomes of operations for 539 patients with Ebstein anomaly. J Thorac Cardiovasc Surg. 2008;135:112036,36 e17.
8. Nakata T, Fujimoto Y, Hirose K, et al. Norwood procedure combined with the Starnes procedure. Ann Thorac Surg. 2008;86:137880.
9. Van Arsdell G. Can we modify late functional outcome in Ebstein anomaly by altering surgical strategy? J Am Coll Cardiol. 2008;52:4679.
10. Brown ML, Dearani JA, Danielson GK, et al. Comparison of the outcome of porcine bioprosthetic versus mechanical prosthetic replacement of the tricuspid valve in the Ebstein anomaly. Am J Cardiol. 2009;103:55561.
11. Boston US, Goldberg SP, Ward KE, et al. Complete repair of Ebstein anomaly in neonates and young infants: a 16-year follow-up. J Thorac Cardiovasc Surg. 2011;141:11639.
12. Liu J, Qiu L, Zhu Z, et al. Cone reconstruction of the tricuspid valve in Ebstein anomaly with or without one and a half ventricle repair. J Thorac Cardiovasc Surg. 2011;141:117883.
1. Doutor, Professor da Universidade Federal Fluminense (UFF), Niterói, RJ, Consultor em Imagem Cardíaca da Plani Diagnósticos Médicos por Imagem, São José dos Campos,SP, Brasil.
2. Médico Radiologista, Coordenador do Grupo de Medicina Interna da Plani Diagnósticos Médicos por Imagem, São José dos Campos, SP, Brasil.
3. Diretor Médico da Plani Diagnósticos Médicos por Imagem, São José dos Campos, SP, Brasil.
Endereço para correspondência:
Dr. Marcelo Souto Nacif
4853 Cordell Avenue, 419
Bethesda, MD, USA
E-mail: msnacif@yahoo.com.br
Trabalho realizado na Plani Diagnósticos Médicos por Imagem, São José dos Campos, SP, Brasil.
 Vol. 44 nº 5 - Set. / Out. of 2011
Vol. 44 nº 5 - Set. / Out. of 2011


