Radiologia Brasileira - Publicação Científica Oficial do Colégio Brasileiro de Radiologia
AMB - Associação Médica Brasileira CNA - Comissão Nacional de Acreditação
 Vol. 42 nº 5 - Set. / Out. of 2009
Vol. 42 nº 5 - Set. / Out. of 2009
|
ARTIGO ORIGINAL
|
|
|
|
|
Autho(rs): Kátia Elisa Prus Pinho, Pedro Miguel Gewehr, Caroline Werner Pereira da Silva, Andersson Barison, João Gilberto Tilly Júnior, Danyel Scheidegger Soboll |
|
|
Descritores: Diagnóstico por imagem, Meios de contraste, Radiação ionizante, Espectroscopia de ressonância magnética nuclear, Raios X, Raios gama |
|
|
Resumo: VFísico Responsável pela Radiologia Geral do Hospital de Clínicas da Universidade Federal do Paraná (UFPR), Curitiba, PR, Brasil
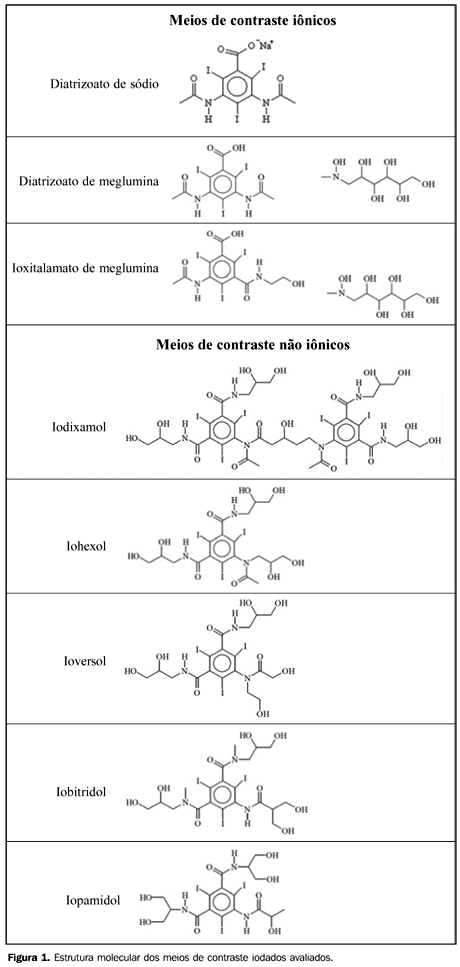
INTRODUÇÃO Os meios de contraste radiológicos são compostos introduzidos no organismo por diferentes vias, que permitem aumentar a definição das imagens radiográficas, graças ao aumento de contraste provocado por eles, possibilitando, desse modo, a obtenção de imagens de alta definição e, com isso, maior precisão em exames de diagnóstico por imagem(1,2). A utilização de compostos com a finalidade de melhorar a qualidade das imagens radiológicas é bastante antiga, cerca de mais de meio século(3). Desde então, reações adversas resultantes da introdução de uma substância estranha ao corpo humano, administrada via oral ou intravenosa, têm sido relatadas, uma vez que nem sempre estas substâncias são inofensivas e algumas vezes podem alterar a circulação sanguínea causando reações inesperadas(4,5). Partindo deste princípio, diversas precauções devem ser tomadas tanto com os pacientes, como no preparo e armazenamento dos meios de contraste(6,7). Todos os meios de contraste iodados usados atualmente são derivados do ácido 2,4,6-triiodobenzoico (Figura 1). São classificados com base nas suas características físico-químicas, incluindo sua estrutura química, osmolalidade, viscosidade, quantidade de átomos de iodo na estrutura, propriedades biológicas, capacidade de ionização em solução, hidrossolubilidade, lipofilia e toxicidade(6). Os meios de contraste iônicos são aqueles capazes de se dissociar em soluções aquosas formando íons cátions e ânions, enquanto os não iônicos não se dissociam (Figura 1), porém interagem com moléculas de água por meio de interações intermoleculares(5). Alguns cuidados no armazenamento e assepsia dos meios de contraste são imprescindíveis, incluindo armazená-los ao abrigo de luz, uma vez que são fotossensíveis, e distantes da incidência de raios X, pela possibilidade da radiação ionizante causar a degradação das moléculas, alterando assim a estrutura do meio de contraste e, com isso, suas propriedades de contraste nas imagens radiológicas. Além disso, é importante mantê-los na temperatura de 15 a 25ºC, uma vez que em baixas temperaturas pode ocorrer a formação de cristais, verificar prazos de validade e não utilizar os frascos e ampolas abertos por mais de 24 horas, devido ao risco de contaminação por microorganismos(8).
No presente trabalho foi investigada a influência da radiação ionizante de raios X e gama sobre a estabilidade da estrutura molecular de diversos meios de contraste comerciais amplamente usados na radiologia em exames de diagnóstico por imagem de raios X e tomografia computadorizada, por meio da espectroscopia de ressonância magnética nuclear (RMN) de 1H e 13C. Buscou-se avaliar possíveis alterações nas estruturas moleculares dos meios de contraste, pela incidência da radiação, o que poderia causar mudanças nas suas propriedades físico-químicas e biológicas, bem como na toxicidade, comprovando assim os resultados presentes da literatura(8).
MATERIAIS E MÉTODOS Amostras Oito diferentes meios de contraste iodados, sendo três iônicos e cinco não iônicos (Figura 1), foram cedidos por quatro fabricantes que os disponibilizam no Brasil. Os contrastes, e respectivos fabricantes, são: Iopamiron 300 e Pielograf 76% (Bayer Schering Pharma; Berlim, Alemanha), Ominipaque e Visipaque (Farmasa; São Paulo, Brasil), Henetix e Telebrix (Guerbet; Paris, França), Optiray 320 e Optiray 350 (Mallinckrodt; Saint Louis, EUA). De cada meio de contraste, oito alíquotas foram tomadas, das quais quatro foram submetidas à radiação por raios X, duas à radiação por raios gama e duas foram mantidas para controle, não sendo expostas a nenhuma radiação. Para proceder a irradiação dos meios de contraste, estes foram dispostos em tubos de microcentrífuga contendo 1,7 ml de cada meio, identificados por letras, para evitar que o operador dos instrumentos soubesse a origem deles. O preparo das amostras foi realizado no Laboratório de Química da Universidade Tecnológica Federal do Paraná (UTFPR), seguindo normas de assepsia para cada frasco aberto e aspirado(9). Irradiação por raios X A irradiação das amostras por raios X foi realizada no Setor de Radioterapia do Hospital Erasto Gaertner, Curitiba, PR, utilizando-se um monitor de radiação Radcal 9010 (Radcal Corp.; Monrovia, EUA) e uma câmara de ionização Radcal 10X5-6 (Radcal Corp.; Monrovia, EUA), com volume sensível de 6 cm3 calibrados para faixa de energia de radiodiagnóstico, determinando-se a radiação exata que as amostras estavam recebendo. Como fonte de radiação foi utilizado tubo de raios X de um simulador de tratamentos de radioterapia RMX 625 R (Raytheon Medical Systems; Melrose Park, EUA), de filtração inerente equivalente a 0,5 mm de alumínio. As amostras foram expostas a diferentes doses de radiação por raios X, variando-se de 9,85 a 10.200 mR (Tabela 1), a uma distância de 50 cm da fonte e tensão de 90 kV(10).
Irradiação por raios gama A irradiação das amostras por raios gama foi realizada utilizando-se a energia média de 1,25 MeV, proveniente de uma fonte de cobalto-60 instalada em uma máquina de teleterapia Theratron 780 C (MDS Nordion; Ontário, Canadá), empregando bolus de 0,5 cm de espessura de gel sobre as amostras. A distância fonte–superfície adotada foi de 50 cm e o rendimento a esta distância foi de 5 Gy/min. As amostras foram expostas a duas doses de radiação: 0,1 e 10 Gy(10). Em ambos os equipamentos as amostras foram irradiadas em um campo de 8 × 8 cm2. Análises de RMN Os espectros de RMN de 1H e 13C{1H} foram adquiridos em um espectrômetro Bruker Avance 400 (Bruker; Karlsruhe, Alemanha) de campo magnético de 9,4 tesla, instalado no Laboratório de RMN da Universidade Federal do Paraná, observando-se os núcleos de 1H e 13C a 400,13 e 100,62 MHz, respectivamente, em D2O (água deuterada) à temperatura ambiente de aproximadamente 22ºC em uma sonda multinuclear de observação direta de 5 mm. Para isso, alíquotas de 0,2 ml de cada meio de contraste foram filtradas em algodão diretamente para tubos de RMN de 5 mm, com auxílio de pipetas Pasteur, os quais foram completados com 0,4 ml de D2O contendo 2,2,3,3-tetradeutério-3-trimetilsililpropionato (TMSP-d4 – referência interna)(11). Os espectros de RMN de 1H foram adquiridos com a sequência de pulsos zg, acumulando-se quatro varreduras, 64 K pontos (1 K = 1.024) e janela espectral de ~13 ppm(11,12). Em algumas amostras foi necessária a pré--saturação do sinal da água, utilizando-se a sequência de pulsos zgpr. Por sua vez, os espectros de RMN de 13C{1H} foram adquiridos com a sequência de pulsos zgpg30, acumulando-se 1.024 varreduras, 32 K pontos e janela espectral de ~255 ppm. Ambos os espectros de RMN de 1H e 13C{1H} foram processados com auxílio do programa TopSpin (Bruker; Karlsruhe, Alemanha), aplicando-se multiplicações exponenciais dos free induction decays (FIDs) por fatores de 0,3 e 3,0 Hz para a construção dos espectros de RMN de 1H e 13C com 64 K e 32 K pontos, respectivamente. Os deslocamentos químicos em ambos os espectros de RMN de 1H e 13C{1H} foram calibrados em relação ao sinal do TMSP-d4 em 0,0 ppm(11).
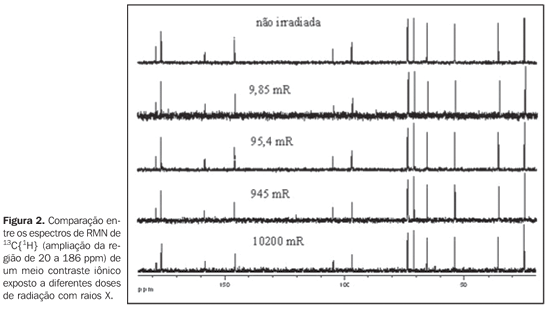
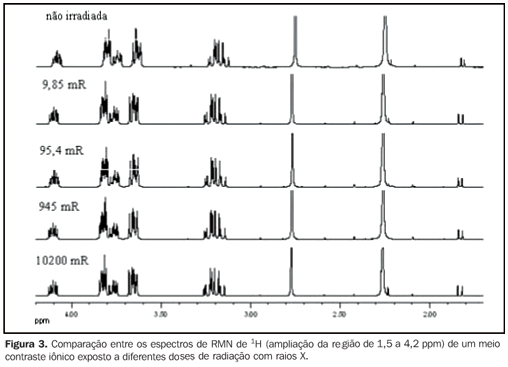
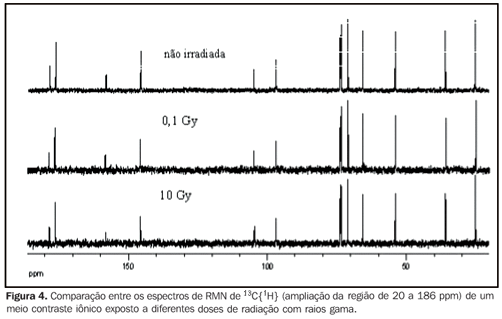
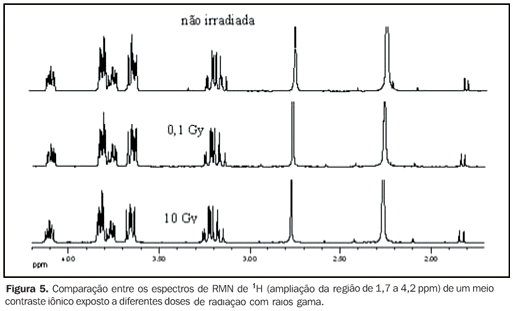
RESULTADOS Com o objetivo de avaliar o efeito da aplicação de radiações ionizantes sobre os meios de contraste empregados em radiologia, espectros de RMN de 13C{1H} e 1H foram obtidos das amostras após sofrerem irradiações por raios X ou raios gama. Da mesma forma, espectros de RMN de 13C{1H} e 1H foram adquiridos de amostras dos mesmos meios de contraste, porém sem sofrer irradiação alguma, os quais foram utilizados como referência para comparação com os espectros de RMN das amostras irradiadas. As Figuras 2 e 3 mostram a comparação entre os espectros de RMN de 13C{1H} e 1H, respectivamente, de uma amostra de meio de contraste iônico exposta a diferentes doses de radiação com raios X, enquanto as Figuras 4 e 5 mostram a comparação entre os espectros de RMN de 13C{1H} e 1H, respectivamente, de uma amostra de meio de contraste iônico que sofreu diferentes doses de radiação com raios gama.
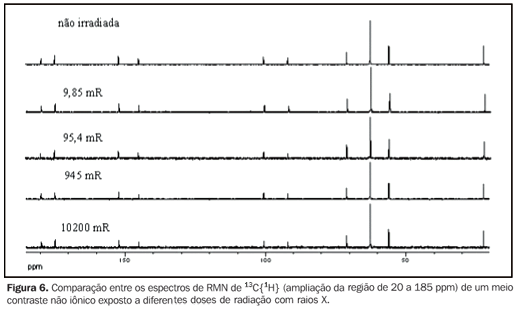
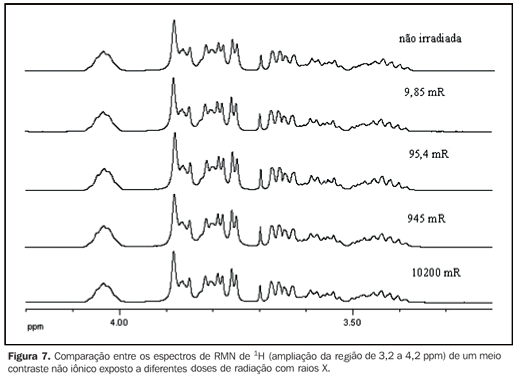
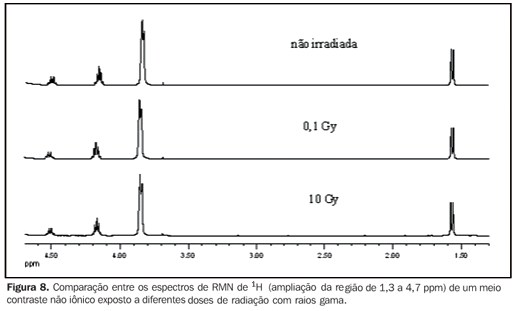
As Figuras 6 e 7 mostram a comparação entre os espectros de RMN de 13C{1H} e 1H, respectivamente, de uma amostra de meio de contraste não iônico exposta a diferentes doses de radiação com raios X, enquanto a Figura 8 mostra a comparação entre os espectros de RMN de 1H de uma amostra de meio de contraste não iônico que sofreu diferentes doses de radiação com raios gama.
DISCUSSÃO Os espectros de RMN de 13C{1H} de ambos os meios de contraste, iônicos e não iônicos, irradiados por raios X ou raios gama mostraram que os níveis de energia utilizados não causaram alterações nas estruturas moleculares dos meios de contraste investigados, como se observa nas Figuras 2, 4 e 6 para um determinado meio de contraste. Da mesma forma, os espectros de RMN de 1H, que apresentam sensibilidade muito superior aos de 13C{1H}(11) , também mostraram não haver nenhuma modificação química dos meios de contraste analisados, como observado nas Figuras 3, 5, 7 e 8. Ou seja, não houve degradação dos meios de contraste analisados, pois não há evidências do surgimento de novos sinais nos espectros RMN, o que seria um indicativo da decomposição dos meios de contraste, com a consequente formação de novos compostos. Isto fica claro ao se comparar os espectros de RMN das amostras mantidas para controle, as quais não sofreram radiação com as amostras irradiadas, seja por raios X ou raios gama, uma vez que todas as amostras apresentam mesmo perfil espectral nas análises de RMN de 1H e 13C{1H} (Figuras 2 a 8). Sendo assim, garante-se a integridade molecular dos meios de contraste estudados, ou seja, de que eles não são alterados quando irradiados com raios X ou raios gama e, portanto, não há problemas em armazenar as amostras nas salas, ou próximo aos equipamentos em que são realizados os exames. Enfatiza-se que a radiação recebida pelas amostras durante os ensaios foi direta, enquanto em um exame real a radiação é indireta e, portanto, os níveis de radiações nestes casos são diferentes daqueles empregados neste estudo. Apesar de alguns fabricantes de meios de contraste recomendarem que estes não sejam mantidos na presença de radiações ionizantes dispersas, este estudo não detectou nenhuma influência da radiação ionizante por raios X ou raios gama na estrutura molecular dos meios de contraste iodados avaliados nas condições utilizadas. Provavelmente, essa observação dos fabricantes deve-se a uma precaução geral no sentido de se preservar e manipular apenas quantidades suficientes de meio de contraste para os exames diários, uma vez que quantidades maiores poderiam, em alguns casos, serem armazenadas na sala de exame, acarretando uma exposição desnecessária e tornando uma prática constante nas unidades de diagnóstico por imagem.
CONCLUSÃO As investigações mostraram que as radiações ionizantes utilizadas na radiologia em exames de diagnósticos por imagem de raios X e tomografia computadorizada não provocam alterações na estrutura molecular (degradação) dos meios de contraste atualmente utilizados, independentemente dos níveis de exposição à irradiação por raios X ou raios gama a que os meios de contraste são submetidos, viabilizando assim o uso clínico desses contrastes. Agradecimentos Às empresas Bayer Schering Pharma, Farmasa, Guerbet e Mallinckrodt, que gentilmente cederam amostras de meios de contraste e tornaram possível a realização deste estudo. Aos Laboratórios de Química da UTFPR e UFPR e ao Hospital Erasto Gaertner, por disponibilizarem os equipamentos para a realização deste trabalho.
REFERÊNCIAS 1. Falgas BJ, Hurlé ADG, Lecumberri VN, et al. Farmacia hospitalaria. Madrid: Sociedad Española de Farmacia Hospitalar; 2002. [ ] 2. Bontrager LK. Tratado de técnica radiológica e base anatômica. Rio de Janeiro: Guanabara Koogan; 1999. [ ] 3. Bettmann MA. Frequently asked questions: iodinated contrast agents. Radiographics. 2004;24 Suppl 1:S3–10. [ ] 4. Asociación Argentina de Alergia e Imunología Clínica. Reacciones adversas a medios de contraste radiológicos: criterios y conductas. AAAelC y SAR. 2001;32:101–5. [ ] 5. Schild H. Todo sobre medios de contraste: ver o no ver. España: Schering AG; 1995. [ ] 6. Pinho KEP. Avaliação de fatores de riscos na utilização de contrastes iodados em exames de urografia excretora [dissertação de mestrado]. Curitiba: CPGEI/UTFPR; 2006. [ ] 7. Colégio Brasileiro de Radiologia. Assistência à vida em radiologia. São Paulo: CBR; 2000. [ ] 8. Sugawara AM, Daros KAC. Manual de meios de contraste em raios X. São Paulo: São Camilo; 2004. [ ] 9. Nischimura L, Potenza M, Cesaretti I. Enfermagem nas unidades de diagnóstico por imagem. São Paulo: Atheneu; 1999. [ ] 10. Stanton R, Stinson D. Applied physics for radiation oncology. Madison: Medical Physics Pub; 1996. [ ] 11. Günter H. NMR spectroscopy: basic principles, concepts, and applications in chemistry. Chichester: John Wiley & Sons; 1995. [ ] 12. Willard HH, Merritt LL Jr, Dean JA, et al. Instrumental methods of analysis. Belmont: Wadsworth Pub; 1988. [ ]
Recebido para publicação em 21/5/2009. Aceito, após revisão, em 21/8/2009.
* Trabalho realizado na Universidade Tecnológica Federal do Paraná (UTFPR), em parceria com o Laboratório de Ressonância Magnética Nuclear do Departamento de Química da Universidade Federal do Paraná (UFPR) e o Departamento de Radioterapia do Hospital Erasto Gaertner, Curitiba, PR, Brasil. |
|
Av. Paulista, 37 - 7° andar - Conj. 71 - CEP 01311-902 - São Paulo - SP - Brazil - Phone: (11) 3372-4544 - Fax: (11) 3372-4554