Radiologia Brasileira - Publicação Científica Oficial do Colégio Brasileiro de Radiologia
AMB - Associação Médica Brasileira CNA - Comissão Nacional de Acreditação
 Vol. 55 nº 3 - Maio / Jun. of 2022
Vol. 55 nº 3 - Maio / Jun. of 2022
|
ARTIGO ORIGINAL
|
|
|
|
|
Autho(rs): Raquel Rodrigues Borges1,a; Tiago Nóbrega Morato2,3,b; Alexandre Sérgio de Araujo Bezerra1,3,c; Bruna Arrais Dias1,d; Juliana Cavalcanti de Freitas Reinaux1,e; Guilherme Urpia Monte4,f; Luciano Farage2,3,4,5,g |
|
|
Descritores: Débito cardíaco; Meios de contraste; Angiografia por tomografia computadorizada. |
|
|
Resumo: INTRODUÇÃO
A tomografia computadorizada do tórax com injeção intravenosa de meio de contraste iodado é amplamente utilizada para avaliação de pacientes com doenças cardíacas e respiratórias. Em virtude de sua alta resolução espacial, permite avaliação morfológica detalhada. Entretanto, a despeito de sua resolução temporal, a tomografia computadorizada tem sido subutilizada para a avaliação de parâmetros funcionais, que nas mais diversas situações clínicas fornecem informações fundamentais para a tomada de decisão terapêutica. Um parâmetro funcional passível de estudo pelo método é a avaliação da função cardíaca. A aquisição de imagens pode ser sincronizada com o eletrocardiograma, permitindo, posteriormente, processar imagens cardíacas na sístole e diástole. Por meio da técnica de Simpson(1), possibilita a avaliação dos volumes sistólicos e diastólicos biventriculares e, dessa forma, o cálculo da fração de ejeção ventricular e do débito cardíaco(2,3). Essa técnica é conhecida como técnica geométrica de avaliação da função cardíaca. Contudo, a avaliação sincronizada ao eletrocardiograma implica a utilização de maior dose de radiação, maior tempo de aquisição e maior número de imagens para pós-processamento, aumentando o tempo de avaliação pelo radiologista. Há ainda necessidade de pós-processamento e análise de imagem com software dedicado. Atualmente, a técnica com maior reprodutibilidade para avaliação não invasiva de avaliação dos volumes ventriculares e fração de ejeção é a ressonância magnética cardíaca(4,5). Assim como na tomografia, o método de medida dos volumes é o método de Simpson, e a correlação entre os métodos é considerada muito boa (r = 0,97)(6). Outra forma de avaliação da função cardíaca, amplamente utilizada desde o começo de século XX, é a avaliação do débito cardíaco por meio de curva de concentração de marcador(7). O método se baseia na detecção da curva de concentração de um marcador em um ponto distante do local de injeção. O contraste iodado pode ser utilizado como marcador, e as medidas de densidade da tomografia mostram relação linear com a concentração de contraste no sangue(810). Dessa forma, uma aquisição dinâmica no nível dos grandes vasos permite a medida seriada da concentração de contraste, com posterior estimativa do débito cardíaco por meio da equação de Stewart-Hamilton. Conceitualmente, a técnica é semelhante à medida do débito cardíaco pelo método de Fick. Uma forma simplificada de avaliação global da função cardíaca é a mensuração do tempo entre a injeção do agente de contraste até a chegada deste em estruturas vasculares torácicas. O pressuposto é que o tempo que o agente de contraste leva para circular está diretamente relacionado ao débito cardíaco e à extensão do território vascular a ser percorrido, sendo este, por sua vez, proporcional ao peso e à altura do paciente(1115). Modelos matemáticos experimentais demonstram a variação dos tempos até a chegada do contraste no tronco arterial pulmonar e na aorta após alterações no débito cardíaco(12,13). Vanhoenacker et al.(16) sugerem uma forma simplificada de estimar a função ventricular por meio da medida do tempo de trânsito do meio de contraste entre os ventrículos direito e esquerdo, relacionada ao tempo de trânsito do agente de contraste na circulação pulmonar. Os resultados obtidos foram promissores, com boa correlação com a medida de função cardíaca pela ressonância magnética. O uso dessa técnica é atrativo por ser simples, correlacionar-se com o débito cardíaco pela ressonância magnética, e dispensar software específico para análise ou calibragem do aparelho. Uma desvantagem da proposta do autor, no entanto, é a posição da medida realizada. Na prática clínica não se realiza avaliação da chegada do agente de contraste no nível dos ventrículos, e sim, na altura do tronco arterial pulmonar, limitando a utilização rotineira do método. Utilizando o mesmo arrazoado teórico de Vanhoenacker et al.(16) e Shors et al.(17), o qual permite a estimativa da função cardíaca, pode ser possível estimar o tempo de circulação venosa periférica, medida entre o sítio da injeção intravenosa do meio de contraste e a chegada deste na veia cava superior, bem como o tempo de circulação vascular pulmonar, pela medida do tempo de trânsito de contraste (TTC) entre o tronco arterial pulmonar e a chegada do contraste na aorta. O uso de tal técnica seria vantajoso por sua simplicidade na aquisição dos tempos de circulação, não necessitando de sequência tomográfica com uso de alta dose de radiação ou calibragem do aparelho de tomografia. Neste caso, são utilizadas as imagens adquiridas na fase inicial do exame a fase de monitoração da chegada do meio de contraste no vaso alvo (bolus tracking). Além de estar relacionada diretamente ao débito cardíaco, a avaliação dos tempos para a chegada do meio de contraste até a veia cava superior e da cava superior até o tronco arterial pulmonar pode, potencialmente, estar relacionada a alterações na resistência da circulação pulmonar e vem sendo ativamente estudada em pacientes com hipertensão pulmonar(1820). Há estudos que correlacionam o TTC, medido entre o sítio da injeção e o tronco arterial pulmonar, e a presença de disfunção ventricular direita, sugerindo que o método pode ser utilizado como adjunto na avaliação de hipertensão arterial pulmonar, como no estudo retrospectivo de pacientes com hipertensão pulmonar definida. Davarpanah et al.(18) e Swift et al.(21) também avaliaram o TTC entre o tronco arterial pulmonar e o átrio esquerdo, em exames de ressonância magnética dinâmica da circulação pulmonar de pacientes com hipertensão arterial pulmonar, encontrando diferença significativa entre o TTC no grupo que apresentou desfecho fatal no acompanhamento, evidenciando a potencialidade de uso do método para avaliação da hipertensão arterial pulmonar(22). Todavia, há grande lacuna na literatura a respeito dos valores normais de TTCs na circulação periférica e na circulação pulmonar. Essa carência de dados inviabiliza o emprego da técnica em larga escala. Este estudo buscou medir os TTCs entre o sítio de injeção (fossa antecubital do membro superior) e a veia cava superior, tronco arterial pulmonar e aorta ascendente em pacientes submetidos a tomografia computadorizada coronariana contrastada, definindo padrões de normalidade para esses tempos de circulação, sendo o débito cardíaco desses pacientes calculado pelo amplamente estabelecido método de Simpson (volumetria). MATERIAIS E MÉTODOS Este é um estudo retrospectivo com grupo de pacientes ambulatoriais adultos submetidos a angiotomografia computadorizada coronariana, no período de dezembro de 2017 a abril de 2019, aprovado pelo Comitê de Ética em Pesquisa do Hospital Santa Marta, Brasília, DF. Os critérios de inclusão aplicados foram: idade superior a 18 anos e ausência de história de insuficiência cardíaca, doença valvar ou doença pulmonar conhecida e ausência de contraindicações ao uso de agente de contraste. Foram excluídos da análise os pacientes com fração de ejeção menor que 55% e volumes diastólico e sistólico finais indexados do ventrículo esquerdo maiores que 100 mL/m2 e 50 mL/m2, respectivamente. Aquisição das imagens Os exames foram realizados em tomógrafo Philips Brilliance (Philips Medical Systems, Best, Holanda) com 64 fileiras de detectores. As imagens utilizadas para o cálculo dos tempos de circulação periférica e pulmonar foram obtidas de acordo com o protocolo padrão de exame, sem acréscimo no volume injetado de meio de contraste ou na dose de radiação. A injeção intravenosa do meio de contraste iodado iônico ioversol (Optiray 350; Mallinckrodt, St. Louis, MO, EUA) foi realizada em veia da prega cubital do membro superior direito, por intermédio de cateter com calibre de 18-G, com fluxo monofásico na velocidade de infusão de 4 mL/s, seguida por 30 mL de soro fisiológico, também administrado a 4 mL/s. O volume administrado foi calculado com base na massa corporal do paciente (1,5 mL/kg). Utilizou-se a técnica conhecida como bolus tracking, em que era posicionada uma região de interesse (ROI) na aorta descendente, ao nível do tronco arterial pulmonar, com o equipamento medindo, a cada segundo, a atenuação no interior do vaso alvo. A aquisição das imagens das artérias coronárias era feita de forma automática quando a atenuação no interior do vaso atingia o limiar de 150 unidades Hounsfield (UH). As imagens adquiridas a cada segundo para monitorar a atenuação na aorta descendente foram reconstruídas em uma nova série, para análise dos tempos de chegada do agente de contraste na veia cava superior, tronco arterial pulmonar e aorta ascendente (todas essas estruturas visíveis no corte utilizado para monitorar a aorta descendente como demonstrado na Figura 1). 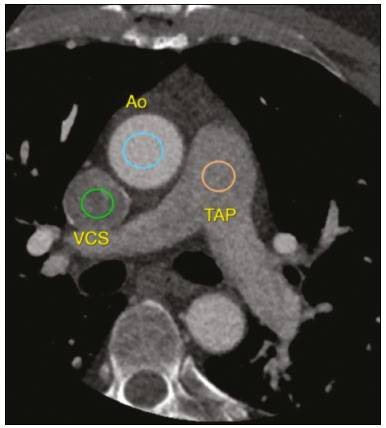 Figura 1. Locais de monitoração da atenuação no interior da veia cava superior (VCS), tronco arterial pulmonar (TAP) e aorta ascendente (Ao). Análise das imagens As imagens para o cálculo dos tempos de trânsito vascular foram reconstruídas com intervalos de 1s e a série resultante foi processada em estação de trabalho Philips Intellispace Portal (Philips Medical Systems), para o cálculo dos tempos de circulação. Tempo de circulação venosa periférica Intervalo de tempo entre o início da injeção intravenosa do meio de contraste em veia na prega cubital até a detecção do aumento da atenuação relacionado à chegada do agente de contraste em ROI posicionada na porção distal da veia cava superior, momento em que a atenuação do sangue junto ao meio de contraste aumenta em 50 UH em relação à imagem sem contraste. Tempo de circulação entre veia cava superior e tronco arterial pulmonar Intervalo de tempo entre a detecção do aumento da atenuação relacionado à chegada do agente de contraste em ROI na veia cava superior e a detecção do aumento da atenuação relacionado à chegada do agente de contraste em ROI no tronco arterial pulmonar (momento em que a atenuação do sangue junto ao meio de contraste aumenta em 50 UH em relação à imagem sem contraste). Tempo de circulação vascular pulmonar Intervalo entre a detecção do aumento da atenuação relacionado à chegada do agente de contraste em ROI no tronco arterial pulmonar (momento em que a atenuação do sangue junto ao meio de contraste aumenta em 50 UH em relação à imagem sem contraste) e a detecção do aumento da atenuação relacionado à chegada do agente de contraste em ROI na aorta ascendente, momento em que a atenuação do sangue junto ao meio de contraste aumenta em 50 UH em relação à imagem sem contraste. Análise geométrica A série pós-administração do agente de contraste (angiográfica) foi reconstruída em dez fases ao longo do ciclo cardíaco. Os volumes sistólico final, diastólico final e volume ejetado do ventrículo esquerdo, assim como a fração de ejeção, o débito cardíaco e o índice cardíaco, foram calculados a partir das imagens da fase pós-contraste de forma semiautomatizada na estação de trabalho Philips Intellispace Portal. Análise estatística Para a avaliação da distribuição da normalidade dos tempos de trânsito foi aplicado o método de DAgostino e Pearson. A correlação entre os valores do TTC com o débito cardíaco e índice cardíaco foi realizada por meio do teste de Pearson. O processamento dos dados e suas correlações foram conduzidos com o uso do software Prism 7 (GraphPad Software Inc., San Diego, CA, EUA). RESULTADOS Foram incluídos no estudo 43 pacientes. O principal motivo de encaminhamento foi rastreamento para doença arterial coronariana. A média de idade da amostra foi de 56,2 anos, variando de 30 a 78 anos, sendo 51,2% do sexo masculino. A Tabela 1 detalha os principais dados demográficos da população estudada. A dose de radiação recebida variou entre 30 mSv e 48 mSv em função do biotipo dos pacientes. 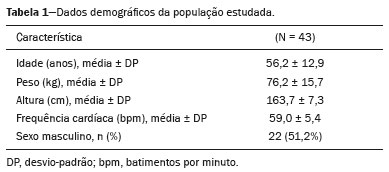 A fração de ejeção estimada pelo método geométrico variou de 56% a 77%, sendo a fração de ejeção média de 63%. O valor médio do índice cardíaco foi de 2,6 ± 0,46 L/min/m2 e variou de 2,0 a 3,9 L/min/m2. Os resultados da análise geométrica estão registrados na Tabela 2. 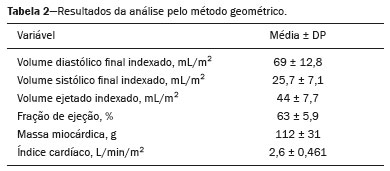 O tempo médio entre a injeção periférica do agente de contraste e a chegada na veia cava superior foi de 3,0 ± 2,4 s e entre a veia cava superior e o tronco arterial pulmonar foi de 2,9 ± 1,4 s. O tempo médio de circulação entre o tronco arterial pulmonar e a aorta ascendente foi de 7,2 ± 2,2 s. Dessa forma, o tempo entre a injeção periférica do agente de contraste e a chegada na aorta ascendente foi de 13 ± 2,56 s. A distribuição do tempo de circulação entre o tronco arterial pulmonar e aorta ascendente foi normal pelo teste de DAgostino e Pearson. Houve tendência a correlação significativa entre o tempo de circulação entre o tronco arterial pulmonar e a aorta ascendente com o índice cardíaco (p = 0,055). Observou-se correlação estatisticamente significante entre este mesmo tempo e a frequência cardíaca, fração de ejeção do ventrículo esquerdo e o volume ejetado por batimento cardíaco pelo ventrículo esquerdo, com valores demonstrados na Tabela 3. O tempo de trânsito do agente de contraste apresentou correlação significativa e inversa com o índice cardíaco, com valor de r de 0,29, demonstrado na Figura 2.  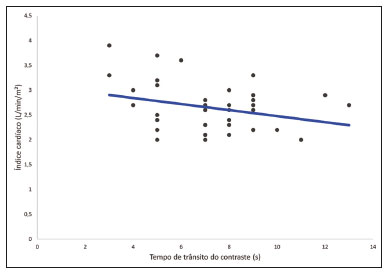 Figura 2. Gráfico de correlação entre o tempo de trânsito do contraste e o índice cardíaco. O valor de r foi 0,29. DISCUSSÃO A investigação de tempos de trânsito de marcadores como forma de avaliação cardiovascular é antiga. No final do século XX e nas primeiras décadas do século XXI, observam-se publicações de trabalhos investigando os tempos de trânsito circulatórios, avaliados por meio de métodos de imagem modernos, notadamente ressonância magnética, tomografia computadorizada e ultrassonografia(8,10,17,18,2325). A avaliação dos TTCs nas séries de bolus tracking apresenta relação direta com a função cardíaca. Não há necessidade de injeção adicional de meio de contraste, nem dose extra de radiação. O pós-processamento é mínimo, precisando de apenas alguns segundos para contar nas imagens-fontes o tempo que o meio de contraste leva para circular entre duas estruturas de interesse. Davarpanah et al.(18) investigaram o TTC, medido entre o sítio de injeção e o tronco arterial pulmonar, em pacientes com hipertensão pulmonar. Identificou-se diferença significativa entre o TTC do grupo controle e o grupo de pacientes com hipertensão pulmonar, definida como pressão sistólica estimada do ventrículo direito maior que 40 mmHg. Houve ainda diferença significativa entre o grupo com sinais de disfunção ventricular direita e sem sinais ao ecocardiograma. Além do valor diagnóstico associado à avaliação dos TTCs, o estudo da dinâmica do meio de contraste permite prever de forma mais consistente os tempos de aquisição de imagens(1114,24). Apesar de alguns resultados publicados sobre o tema em populações de pacientes com hipertensão arterial pulmonar e insuficiência cardíaca, não se identifica, em revisão de literatura em bases de dados indexadas, estudo populacional para determinação do valor de normalidade do tempo de trânsito. Tendo em vista essa lacuna, o objetivo do presente estudo foi a determinação de valor de referência populacional utilizando a medida do tempo entre o tronco arterial pulmonar e a aorta ascendente, por simular de maneira mais fidedigna o posicionamento do corte de monitoração para realização de diversas angiotomografias torácicas, incluindo angiotomografias das artérias pulmonares, artérias coronárias e da aorta. Tal fato torna as medidas diretamente aplicáveis na prática clínica. Não se espera diferença significativa entre as medidas descritas nos estudos prévios, dada a equidistância dos pontos de observação propostos por nosso grupo dos pontos utilizados por outros grupos(17,18,22). O tempo médio de trânsito foi de 7,2 s, estando próximo do tempo obtido em grupos controles de estudos que realizaram a medida, como nos estudos de Davarpanah et al.(18), em que o tempo médio de trânsito foi de 6,6 s no grupo controle, e no de Skrok et al.(22), em que tempo médio foi de 6,4 s. Uma das preocupações atuais da prática radiológica é a dose de radiação, por isso um dos pontos fortes da técnica proposta é não implicar dose significativamente mais alta de radiação do que a utilizada de rotina. A aplicação da monitoração desde o momento inicial da injeção do agente de contraste determinou aquisição de cerca de 60 imagens adicionais do tórax, com a utilização de baixa corrente e voltagem (em geral, 100 kVp e 50 mAs). Alguns estudos vasculares poderiam ser realizados sem a monitoração da chegada do meio de contraste na estrutura alvo desde o início da injeção, como em angiotomografias de aorta. Nesses casos, em geral o tomógrafo é programado para iniciar a monitoração somente após um intervalo fixo, em geral 10 a 15 s, economizando dose de radiação e impedindo a análise dos tempos de trânsito. A dose adicional de radiação estimada para a monitoração proposta é por volta de 0,07 mSv, que pode ser considerada muito baixa (a exposição anual da população geral é da ordem de 2 mSv). A maior parte dos trabalhos utilizou como referência o tempo de circulação entre o ventrículo direito e o ventrículo esquerdo(9,10,1618). Para realizar esta medida, torna- se necessário realizar uma sequência adicional, com uso de injeção de teste de meio de contraste ou modificação do protocolo padrão de aquisição das angiotomografias. A amostra do presente trabalho foi suficiente para estudar os TTCs médios, notando-se distribuição normal do tempo de circulação entre o tronco arterial pulmonar e a aorta ascendente pelo teste de DAgostino e Person, portanto, os dados podem ser reproduzidos em amostras maiores de pacientes. O tempo de trânsito do agente de contraste apresentou correlação significativa e inversa com o débito cardíaco. Neste estudo, o valor de r foi baixo, próximo de 0,3, e isso provavelmente está relacionado à seleção de pacientes sem alterações cardiovasculares e ao tamanho da nossa amostra. O objetivo inicial do trabalho não era comprovar essa correlação, já previamente conhecida com base em estudos de dinâmica do agente de contaste e de estudos com termodiluição(7,911), mas sim estabelecer o valor médio de normalidade do tempo de trânsito. Acreditamos que uma vez estabelecido o valor de normalidade, este dado possa ser usado como critério de triagem. A identificação de pacientes com tempos de trânsito alterados merece atenção clínica e complementação diagnóstica com métodos específicos como quantificação do pró-peptídeo natriurético tipo-B e ecocardiograma. CONCLUSÃO O valor de normalidade dos TTCs entre o tronco arterial pulmonar e a aorta ascendente foi estabelecido, servindo de base para avaliação clínica. O uso dessa técnica pode permitir aos radiologistas sugerir ou excluir doenças cardíacas com mais confiança nos pacientes encaminhados para as principais aplicações de tomografia computadorizada. REFERÊNCIAS 1. Thiele H, Paetsch I, Schnackenburg B, et al. Improved accuracy of quantitative assessment of left ventricular volume and ejection fraction by geometric models with steady-state free precession. J Cardiovasc Magn Reson. 2002;4:32739. 2. Coche E, Vlassenbroek A, Roelants V, et al. Evaluation of biventricular ejection fraction with ECG-gated 16-slice CT: preliminary findings in acute pulmonary embolism in comparison with radionuclide ventriculography. Eur Radiol. 2005;15:143240. 3. Scheffel H, Stolzmann P, Leschka S, et al. Ventricular short-axis measurements in patients with pulmonary embolism: effect of ECG-gating on variability, accuracy, and risk prediction. Eur J Radiol. 2012;81:2195202. 4. Grothues F, Braun-Dullaeus R. Serial assessment of ventricular morphology and function. Heart Fail Clin. 2009;5:30114, v. 5. American College of Cardiology Foundation Task Force on Expert Consensus Documents; Hundley WG, Bluemke DA, Finn JP, et al. ACCF/ACR/AHA/NASCI/SCMR 2010 expert consensus document on cardiovascular magnetic resonance: a report of the American College of Cardiology Foundation Task Force on Expert Consensus Documents. J Am Coll Cardiol. 2010;55:261462. 6. Raman SV, Shah M, McCarthy B, et al. Multi-detector row cardiac computed tomography accurately quantifies right and left ventricular size and function compared with cardiac magnetic resonance. Am Heart J. 2006;151:73644. 7. Morris LE, Blumgart HL. Velocity of blood flow in health and disease. Circulation. 1957;15:44860. 8. Garrett JS, Lanzer P, Jaschke W, et al. Measurement of cardiac output by cine computed tomography. Am J Cardiol. 1985;56:65761. 9. Ludman PF, Coats AJ, Poole-Wilson PA, et al. Measurement accuracy of cardiac output in humans: indicator-dilution technique versus geometric analysis by ultrafast computed tomography. J Am Coll Cardiol. 1993;21:14829. 10. Mahnken AH, Klotz E, Hennemuth A, et al. Measurement of cardiac output from a test-bolus injection in multislice computed tomography. Eur Radiol. 2003;13:2498504. 11. Bae KT. Peak contrast enhancement in CT and MR angiography: when does it occur and why? Pharmacokinetic study in a porcine model. Radiology. 2003;227:80916. 12. Bae KT. Optimization of contrast enhancement in thoracic MDCT. Radiol Clin North Am. 2010;48:929. 13. Bae KT, Heiken JP, Brink JA. Aortic and hepatic contrast medium enhancement at CT. Part I. Prediction with a computer model. Radiology. 1998;207:64755. 14. Bae KT, Heiken JP, Brink JA. Aortic and hepatic contrast medium enhancement at CT. Part II. Effect of reduced cardiac output in a porcine model. Radiology. 1998;207:65762. 15. Bae KT, Tran HQ, Heiken JP. Multiphasic injection method for uniform prolonged vascular enhancement at CT angiography: pharmacokinetic analysis and experimental porcine model. Radiology. 2000;216:87280. 16. Vanhoenacker PK, Van Hoe LR. A simple method to estimate cardiac function during routine multi-row detector CT exams. Eur Radiol. 2007;17:284551. 17. Shors SM, Cotts WG, Pavlovic-Surjancev B, et al. Heart failure: evaluation of cardiopulmonary transit times with time-resolved MR angiography. Radiology. 2003;229:7438. 18. Davarpanah AH, Hodnett PA, Farrelly CT, et al. MDCT bolus tracking data as an adjunct for predicting the diagnosis of pulmonary hypertension and concomitant right-heart failure. AJR Am J Roentgenol. 2011;197:106472. 19. Swift AJ, Telfer A, Rajaram S, et al. Dynamic contrast-enhanced magnetic resonance imaging in patients with pulmonary arterial hypertension. Pulm Circ. 2014;4:6170. 20. Swift AJ, Wild JM, Nagle SK, et al. Quantitative magnetic resonance imaging of pulmonary hypertension: a practical approach to the current state of the art. J Thorac Imaging. 2014;29:6879. 21. Swift AJ, Rajaram S, Hurdman J, et al. Noninvasive estimation of PA pressure, flow, and resistance with CMR imaging: derivation and prospective validation study from the ASPIRE registry. JACC Cardiovasc Imaging. 2013;6:103647. 22. Skrok J, Shehata ML, Mathai S, et al. Pulmonary arterial hypertension: MR imaging-derived first-pass bolus kinetic parameters are biomarkers for pulmonary hemodynamics, cardiac function, and ventricular remodeling. Radiology. 2012;263:67887. 23. Müller HM, Rehak PH, Puchinger M, et al. Measurement of cardiac output and pulmonary transit time for assessment of pulmonary vascular resistance in domestic piglets. Exp Physiol. 2009; 94:65964. 24. Francois CJ, Shors SM, Bonow RO, et al. Analysis of cardiopulmonary transit times at contrast material-enhanced MR imaging in patients with heart disease. Radiology. 2003;227:44752. 25. Choi BG, Sanai R, Yang B, et al. Estimation of cardiac output and pulmonary vascular resistance by contrast echocardiography transit time measurement: a prospective pilot study. Cardiovasc Ultrasound. 2014;12:44. 1. Hospital Santa Marta, Brasília, DF, Brasil 2. Radiolinea Centro de Imagens, Brasília, DF, Brasil 3. Universidade de Brasília (UnB), Brasília, DF, Brasil 4. Instituto de Cardiologia do Distrito Federal (ICDF), Brasília, DF, Brasil 5. Centro Universitário Euroamericano (Unieuro), Brasília, DF, Brasil a. https://orcid.org/0000-0002-9734-5157 b. https://orcid.org/0000-0002-5829-5548 c. https://orcid.org/0000-0001-6385-2954 d. https://orcid.org/0000-0002-7737-8031 e. https://orcid.org/0000-0003-0290-8963 f. https://orcid.org/0000-0003-0744-1709 g. https://orcid.org/0000-0002-2293-3771 Correspondência: Dr. Alexandre Sérgio de Araujo Bezerra QSE 11, Área Especial 01 e 17, Setor E Sul, Taguatinga Brasília, DF, Brasil, 72025-110 E-mail: alexbezerra@gmail.com Recebido para publicação em 14/4/2021 Aceito, após revisão, em 8/7/2021 Data de publicação: 04/11/2021 |
|
Av. Paulista, 37 - 7° andar - Conj. 71 - CEP 01311-902 - São Paulo - SP - Brazil - Phone: (11) 3372-4544 - Fax: (11) 3372-4554