Radiologia Brasileira - Publicação Científica Oficial do Colégio Brasileiro de Radiologia
AMB - Associação Médica Brasileira CNA - Comissão Nacional de Acreditação
 Vol. 54 nº 2 - Mar. / Abr. of 2021
Vol. 54 nº 2 - Mar. / Abr. of 2021
|
ENSAIO PICTÓRICO
|
|
|
|
|
Autho(rs): Heloisa Sisconeto Bisinottoa; Vinicius Menezes Jarryb; Fabiano Reisc |
|
|
Descritores: Lobo temporal/diagnóstico por imagem; Tomografia computadorizada; Ressonância magnética. |
|
|
Resumo: INTRODUÇÃO
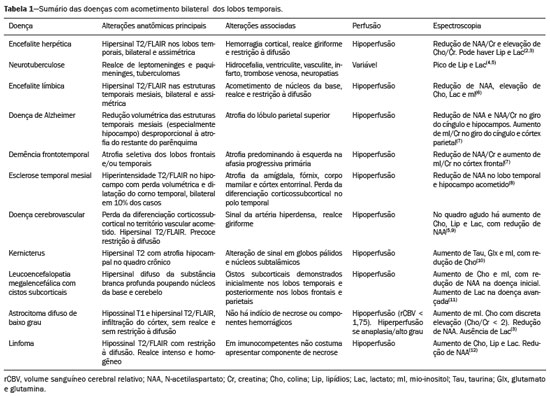
O lobo temporal pode ser dividido em neocórtex e lobo temporal mesial. O primeiro corresponde à superfície lateral e inferior e está relacionado aos processos de visão, audição e fala. O segundo, situado medialmente, é parte do sistema límbico exercendo papel no controle das emoções, comportamento e memória, além de função neuroendócrina e autonômica (Figura 1). Estruturas como a comissura anterior, o corpo caloso e a comissura hipocampal são responsáveis por interligarem os lobos temporais, favorecendo envolvimento bilateral em diversos contextos clínicos(1). 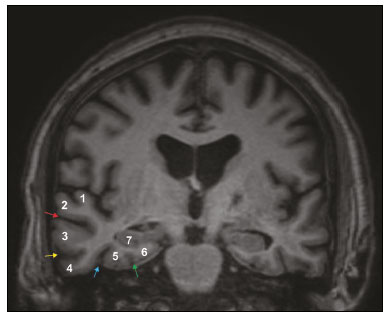 Figura 1. Coronal T1 demonstrando a anatomia normal do lobo temporal. 1, giro temporal transverso; 2, giro temporal superior; 3, giro temporal médio; 4, giro temporal inferior; 5, giro occipitotemporal lateral; 6, giro para-hipocampal/occipitotemporal medial; 7, hipocampo. Seta vermelha, sulco temporal superior; seta amarela, sulco temporal inferior; seta azul, sulco occipitotemporal; seta verde, sulco colateral. Os pacientes com lesões no lobo temporal podem apresentar confusão mental/rebaixamento do nível de consciência, sendo os exames de imagem fundamentais para adequada avaliação e diagnóstico etiológico precoce. O uso de sequências avançadas de ressonância magnética (RM), como a espectroscopia de prótons de hidrogênio, e de perfusão, permite contribuir no diagnóstico diferencial das lesões mencionadas (Tabela 1)(212). Algumas das doenças que acometem os lobos temporais serão detalhadas a seguir, com ênfase nos achados neurorradiológicos, a fim de enfatizar a importância da neuroimagem no diagnóstico diferencial. ETIOLOGIA INFECCIOSA A encefalite infecciosa aguda é condição grave causada por inúmeros patógenos, sendo a encefalite herpética a etiologia mais comum. Os vírus herpes simples tipo 2 e citomegalovírus são classicamente associados a encefalite neonatal. Após esse período, a maioria dos casos decorre de reativação do herpes simples tipo 1(13). O herpes simples tipo 8 pode ter apresentação semelhante ao herpes simples tipo 1 em paciente imunossuprimido. A tomografia computadorizada (TC) do crânio possui baixa sensibilidade nos estádios iniciais e quando alterada está associada a dano cerebral grave e pior prognóstico. A RM é o método de escolha. O hipersinal em T2/FLAIR corticossubcortical dos lobos temporais é achado característico da encefalite herpética. Inicialmente, pode ser unilateral, mas evolui para acometimento bilateral assimétrico (Figura 2). O envolvimento isolado do hipocampo não é achado habitual, devendo-se suspeitar de diagnósticos diferenciais, como encefalite límbica e status pós-convulsivo. Focos de sangramento cortical, áreas de restrição à difusão e realce giriforme podem ser observados(1,13,14). 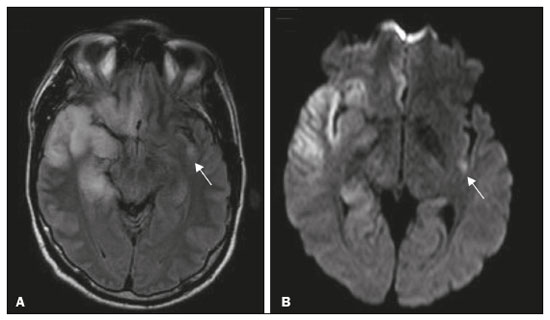 Figura 2. Paciente do sexo masculino, 46 anos, com cefaleia, febre e confusão mental. A: Axial FLAIR demonstrando hiperintensidade de sinal em ambos os lobos temporais (seta), mais evidente à direita. B: DWI com restrição à difusão bilateral (seta). PCR positivo para herpes simples tipo 1 no líquor. A tuberculose também pode envolver o sistema nervoso central por disseminação hematogênica, o que é visto em até 5% dos pacientes, com incidência maior em imunossuprimidos. A leptomeningite tuberculosa é a apresentação mais frequente, contudo, pode haver também envolvimento parenquimatoso concomitante (meningoencefalite) ou isolado (tuberculoma, abscesso cerebral e encefalite)(15). A paquimeningite tuberculosa também pode ocorrer, observando-se baixo sinal em T2 e realce difuso da paquimeninge(4) (Figura 3). 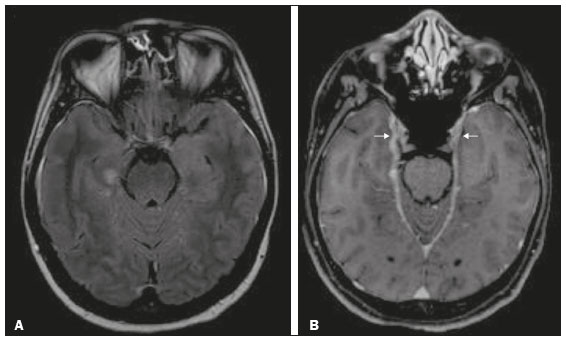 Figura 3. Paciente do sexo feminino, 35 anos, sorologia positiva para HIV, com febre e cefaleia frontoparietal esquerda há sete dias. Líquor com hiperproteinorraquia, leucocitose com predomínio de linfócitos, glicose reduzida e elevação de adenosina deaminase, favorecendo o diagnóstico de neurotuberculose. Axial FLAIR (A) e axial T1 pós-contraste (B) demonstrando espessamento paquimeníngeo (setas) com maior conspicuidade temporal à direita, local em que também se observa alteração de sinal dos lobos temporais na ponderação FLAIR. A paciente apresentou melhora dos sintomas, com resolução do quadro radiológico no exame de controle realizado um ano após o início dos sintomas (imagens não mostradas). ETIOLOGIA IMUNOMEDIADA As encefalites autoimunes ou encefalites límbicas são condições inflamatórias raras, com características clinicorradiológicas semelhantes, diferenciando-se pelo subtipo específico de anticorpo envolvido na lesão neuronal. Podem ser classificadas em paraneoplásica e não paraneoplásica. No caso de neoplasia oculta, é recomendado manter rastreamento por até quatro anos após o diagnóstico da encefalite autoimune. Independentemente da etiologia, o acometimento do sistema límbico é o achado mais característico, com hipersinal corticossubcortical em T2/FLAIR, bilateral e assimétrico na maioria dos casos (Figura 4). Diferentemente da encefalite herpética, os núcleos da base são frequentemente envolvidos, enquanto o lobo temporal lateral e a ínsula geralmente são poupados. Restrição à difusão e hemorragia não são achados frequentes. Pode evoluir com atrofia temporal mesial, sendo associada a epilepsia do lobo temporal(1,16). 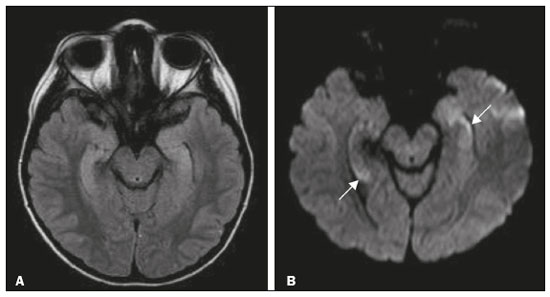 Figura 4. Paciente do sexo feminino, 9 anos, com alteração comportamental, inversão do ciclo sono-vigília e convulsões. Investigação negativa para causas infecciosas e metabólicas. Pesquisa de autoanticorpos no líquor positiva para anticorpos anti-GAD. PET/CT com FDG18F sem alterações hipermetabólicas sugestivas de acometimento neoplásico. Axial FLAIR (A) e DWI (B) demonstrando hipersinal nas regiões temporais mesiais com focos de restrição à difusão (setas). Controle evolutivo após um ano com marcada redução volumétrica das formações A B hipocampais (imagem não mostrada). ETIOLOGIA NEURODEGENERATIVA A doença de Alzheimer é o subtipo mais comum de demência, responsável por dois terços dos casos. O comprometimento da memória é o sintoma inicial mais comum, associado ou não a disfunção executiva e visuoespacial. Os depósitos de peptídio beta-amiloide e proteína tau resultam em perda neuronal seletiva nos hipocampos e giros para-hipocampais. Como consequência, há redução volumétrica do lobo temporal mesial desproporcional à atrofia do restante do parênquima cerebral, sendo este o achado mais característico da doença de Alzheimer (Figura 5). O escore MTA, uma escala visual capaz de quantificar o grau de atrofia hipocampal, possui alta sensibilidade para o diagnóstico da demência de Alzheimer, porém, não é específico(17). 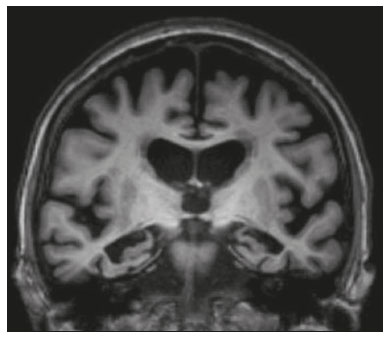 Figura 5. Paciente do sexo feminino, 77 anos, apresentando esquecimento para fatos recentes e redução da atenção. Coronal T1 demonstrando alargamento dos cornos temporais e redução volumétrica dos hipocampos. A demência frontotemporal é uma das causas mais comuns de demência pré-senil. Caracteriza-se por distúrbio de comportamento, personalidade e linguagem, com degeneração seletiva dos lobos frontal e/ou temporal. Duas variantes principais foram descritas: a comportamental e a afasia progressiva primária. A atrofia preferencial e geralmente assimétrica do lobo temporal esquerdo (bem como da porção posterior do lobo frontal e ínsula à esquerda) é observada na variante semântica da afasia progressiva primária(1) (Figura 6). 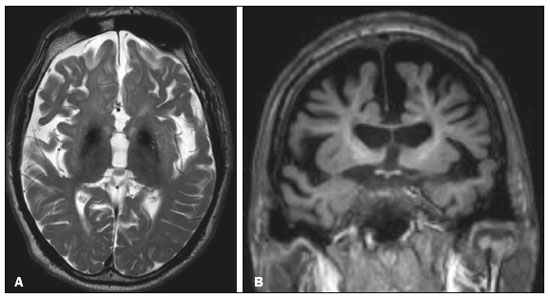 Figura 6. Paciente do sexo masculino, 37 anos, com involução neurológica progressiva. Axial T2 (A) e coronal T1 (B) demonstrando redução volumétrica do encéfalo acima do esperado para a faixa etária, com predomínio frontotemporal bilateral e preservação das regiões corticais posteriores (imagem A). SÍNDROME EPILÉPTICA A esclerose temporal mesial é a causa mais comum das epilepsias do lobo temporal. A maior parte dos pacientes apresenta crises parciais complexas de difícil controle. Já foram descritas associações com fatores genéticos e antecedentes de convulsão febril, infecções do sistema nervoso central e encefalite límbica. Há perda neuronal e gliose envolvendo predominantemente as regiões hipocampais. Os achados de RM incluem perda volumétrica do hipocampo, com dilatação do corno temporal e aumento de sinal nas sequências T2/FLAIR. O acometimento bilateral ocorre em 10% dos casos (Figura 7). 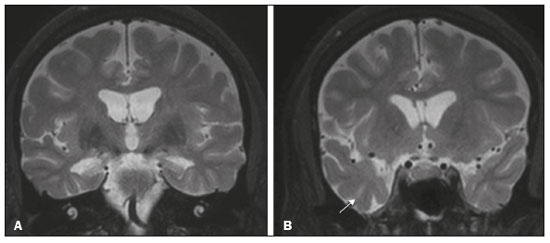 Figura 7. Paciente do sexo masculino, 62 anos, com crises convulsivas de difícil controle. Coronal T2 demonstrando redução volumétrica de ambos os hipocampos, com hipersinal e perda das rugosidades do contorno superior (alteração citoarquitetural). No polo temporal direito existe borramento da transição entre as substâncias branca e cinzenta (seta). Lesões associadas são descritas em até 20% dos pacientes, entre elas atrofia da amígdala, do fórnix, do corpo mamilar e do córtex entorrinal, além de perda da diferenciação corticossubcortical do polo temporal(1,13,18). ETIOLOGIA CEREBROVASCULAR O suprimento arterial dos lobos temporais é dependente tanto da circulação anterior quanto da posterior. Oclusões do topo da artéria basilar ou das artérias cerebrais posteriores podem evoluir com isquemia dos lobos temporais mediais, lobos occipitais, mesencéfalo e tálamo. Na TC, nos quadros agudos pode-se observar o trombo intravascular (sinal da artéria hiperdensa), hipoatenuação com perda da diferenciação corticossubcortical no território vascular correspondente e edema citotóxico com efeito expansivo local (Figura 8)(8,19). 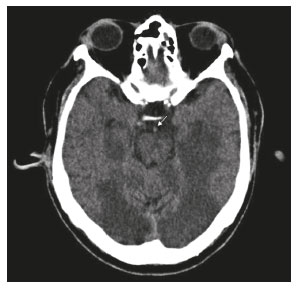 Figura 8. Paciente do sexo masculino, 67 anos, apresentou cefaleia súbita, turvação visual e rebaixamento do nível de consciência. TC no plano axial mostrando hipoatenuação corticossubcortical envolvendo lobos temporais mediais e occipitais, além do mesencéfalo e cerebelo. Nota-se sinal da artéria basilar hiperdensa compatível com trombo agudo (seta). A RM permite avaliar com maior precisão a temporalidade do insulto isquêmico. Há evidência de restrição à difusão em estádio bem precoce. O acometimento exclusivo do hipocampo é raro, devendo-se considerar diagnósticos diferenciais, como status pós-convulsivo. ETIOLOGIA METABÓLICA Kernicterus é uma condição rara em que há acometimento neurológico secundário a hiperbilirrubinemia (bilirrubina sérica acima de 20 mg/dL), com acúmulo de bilirrubina indireta nos globos pálidos, núcleos subtalâmicos, hipocampo, putâmen, tálamo e nervos cranianos (notadamente III, IV e V). Os achados de RM incluem hipersinal em sequências ponderadas em T1 nos globos pálidos e núcleos subtalâmicos, com progressão para hipersinal T2/FLAIR nessas estruturas e podendo evoluir com atrofia hipocampal (Figura 9)(2022). 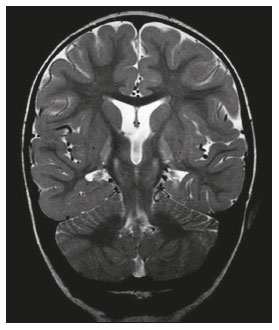 Figura 9. Paciente do sexo feminino, 4 anos, com antecedente de hiperbilirrubinemia neonatal. Coronal T2 com hiperintensidade de sinal em globos pálidos, regiões subtalâmicas/subtálamo/mesencéfalo e em hipocampos (estes de dimensões reduzidas). LEUCOENCEFALOPATIA A leucoencefalopatia megalencefálica com cistos subcorticais é doença de herança autossômica recessiva caracterizada por extensa vacuolização nas camadas externas da bainha de mielina. O quadro clínico geralmente se inicia na infância com macrocefalia associada a deterioração motora lenta e progressiva. O diagnóstico pode ser estabelecido em pacientes com quadro clínico e achados de imagens típicos (Figura 10). Na RM nota-se hipersinal difuso e confluente da substância branca afetada, poupando os núcleos da base e a substância branca cerebelar. Os cistos subcorticais são demonstrados inicialmente nos lobos temporais e depois nos lobos frontais e parietais(13,23). 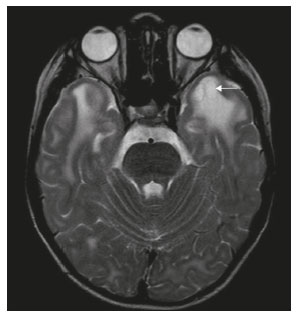 Figura 10. Paciente do sexo masculino, 9 anos, com antecedente de macrocrania desde os 5 meses de idade e atraso do desenvolvimento neuropsicomotor. Axial T2 demonstrando imagens císticas no polo temporal esquerdo (seta). Há, ainda, hipersinal em regiões subcorticais e profundas de lobos temporais e regiões subcorticais occipitais. ETIOLOGIA NEOPLÁSICA As neoplasias podem envolver os lobos temporais simultaneamente por disseminação via comissura anterior (mais comum), corpo caloso e comissura hipocampal. Esse padrão é mais frequente nos tumores gliais (Figura 11), contudo, pode ocorrer em outros contextos, como no caso do linfoma secundário (Figura 12). O astrocitoma difuso de baixo grau (grau 2) tem crescimento lento, a maioria é de localização supratentorial, com acometimento preferencial dos lobos frontal e temporal. Nos exames tomográficos apresenta-se como lesão hipodensa sem realce pelo meio de contraste. Nos estudos de RM são lesões hipointensas em T1 e hiperintensas em T2, com moderado efeito expansivo e sem realce. Não apresentam restrição à difusão e seu volume sanguíneo cerebral relativo é relativamente baixo na sequência de perfusão (não costuma ser maior do que 1,75 vez em relação ao parênquima contralateral)(1,23). 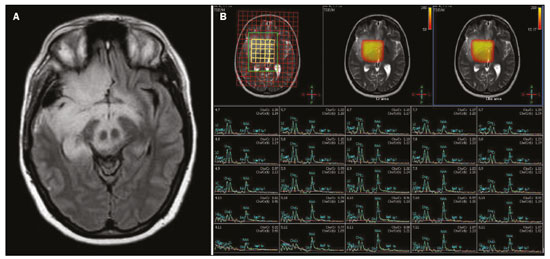 Figura 11. Paciente do sexo feminino, 31 anos, com história de cefaleia e crises convulsivas. A: Axial FLAIR demonstrando hipersinal em ambos os lobos temporais, frontais (com maior conspicuidade à direita) e envolvimento do parênquima mesencefálico. Nas sequências pós-contraste não foi identificado realce e não havia aumento perfusional (imagens não mostradas). B: Espectroscopia multivoxel com tempo de eco de 144 ms revelou relação Cho/Cr de no máximo 1,23 e também tendência à redução de NAA. Paciente submetida a lobectomia temporal e amigdalo-hipocampectomia direita, com anatomopatológico de astrocitoma difuso de baixo grau (grau II) padrão histológico fibrilar. 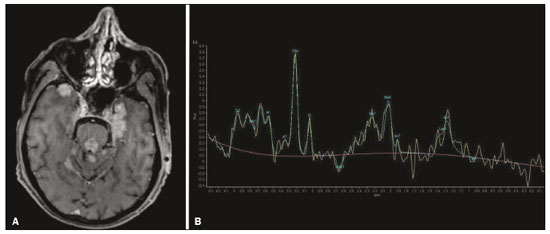 Figura 12. Paciente do sexo masculino, 47 anos, com diagnóstico de linfoma não Hodgkin de alto grau imunofenótipo B. Queixa súbita de diplopia, ataxia e desequilíbrio. Avaliação inicial do líquor sem alterações. A: Axial T1 pós-contraste mostrando lesões com realce difuso e intenso no aspecto anterior dos lobos temporais, hipocampos, tegmento mesencefálico e cerebelo. B: Espectroscopia (PRESS com tempo de eco curto, de 31 ms) mostrando importante pico de lipídios/lactato em lesão de aspecto sólido e homogeneamente captante (que pode ser decorrente de necrose microscópica, favorecendo linfoma, tendo em vista que gliomas e metástases costumam apresentar este pico em zonas hipocaptantes). Há ainda aumento dos níveis de colina, inferindo alto turnover celular. Há evidências de que o linfoma apresenta baixo volume sanguíneo cerebral relativo em comparação com neoplasias gliais(24). Normalmente, as lesões de linfoma apresentam alta celularidade (com iso ou hipossinal em T2), restrição à difusão e realce intenso pelo meio de contraste(12,25). CONCLUSÃO Diversas afecções podem acometer os lobos temporais bilateralmente. O conhecimento dessas doenças e dos principais aspectos de imagem, com ênfase em RM, auxilia no diagnóstico precoce, com possibilidade de melhor prognóstico. REFERÊNCIAS 1. Eran A, Hodes A, Izbudak I. Bilateral temporal lobe disease: looking beyond herpes encephalitis. Insights Imaging. 2016;7:26574. 2. Hitosugi M, Ichijo M, Matsouka Y, et al. Proton MR spectroscopy findings in herpes simplex encephalitis. Rinsho Shinkeigaku. 1996;36:83943. 3. Demaerel P, Wilms G, Robberecht W, et al. MRI of herpes simplex encephalitis. Neuroradiology. 1992;34:4903. 4. Khatri GD, Krishnan V, Antil N, et al. Magnetic resonance imaging spectrum of intracranial tuberculous lesions: one disease, many faces. Pol J Radiol. 2018;83:e524e535. 5. Mader I, Rauer S, Gall P, et al. (1)H MR spectroscopy of inflammation, infection and ischemia of the brain. Eur J Radiol. 2008;67:2507. 6. Isik N, Candan F, Dincer A, et al. Serial cranial MR imaging and single voxel proton MR spectroscopy in paraneoplastic limbic encephalitis. Eur J Radiol Extra. 2004;50:17. 7. Kantarci K. Magnetic resonance spectroscopy in common dementias. Neuroimaging Clin N Am. 2013;23:393406. 8. Capizzano AA, Vermathen P, Laxer KD, et al. Multisection proton MR spectroscopy for mesial temporal lobe epilepsy. AJNR Am J Neuroradiol. 2002;23:135968. 9. Faria AV, Reis F, Zanardi VA, et al. The pattern of proton magnetic resonance spectroscopy in non-neoplastic encephalic lesions. Arq Neuropsiquiatr. 2004;62:42936. 10. Oakden WK, Moore AM, Blaser S, et al. 1H MR spectroscopic characteristics of kernicterus: a possible metabolic signature. AJNR Am J Neuroradiol. 2005;26:15714. 11. Reis F, Kido RYZ, Mesquita JA, et al. Megalencephalic leukoencephalopathy with subcortical cysts (MLC) a case with clinical and magnetic resonance imaging (MRI) dissociation. Arq Neuropsiquiatr. 2015;73:1712. 12. Reis F, Schwingel R, Nascimento FBP. Central nervous system lymphoma: iconographic essay. Radiol Bras. 2013;46:1106. 13. Soares BP, Provenzale JM. Imaging of herpes virus infections of the CNS. AJR Am J Roentgenol. 2016;206:3948. 14. Sureka J, Jakkani RK. Clinico-radiological spectrum of bilateral temporal lobe hyperintensity: a retrospective review. Br J Radiol. 2012;85:e78292. 15. Burrill J, Williams CJ, Bain G, et al. Tuberculosis: a radiologic review. Radiographics. 2007;27:125573. 16. Kelley BP, Patel SC, Marin HL, et al. Autoimmune encephalitis: pathophysiology and imaging review of an overlooked diagnosis. AJNR Am J Neuroradiol. 2017;38:10708. 17. van de Pol LA, Hensel A, Barkhof F, et al. Hippocampal atrophy in Alzheimer disease: age matters. Neurology. 2006;66:2368. 18. Urbach H. Imaging of the epilepsies. Eur Radiol. 2005;15:494500. 19. Allen LM, Hasso AN, Handwerker J, et al. Sequence-specific MR imaging findings that are useful in dating ischemic stroke. Radiographics. 2012;32:128597. 20. Martich-Kriss V, Kollias SS, Ball WS Jr. MR findings in kernicterus. AJNR Am J Neuroradiol. 1995;16(4 Suppl):81921. 21. Shroff MM, Soares-Fernandes JP, Whyte H, et al. MR imaging for diagnostic evaluation of encephalopathy in the newborn. Radiographics. 2010;30:76380. 22. Niemeyer B, Lima GA, Ventura N, et al. Chronic kernicterus: magnetic resonance imaging findings. Radiol Bras. 2016;49:4078. 23. Osborn AG. Encefalo de Osborn: imagem, patologia e anatomia. Porto Alegre, RS: Artmed; 2014. 24. Provenzale JM, Mukundan S, Barboriak DP. Diffusion-weighted and perfusion MR imaging for brain tumor characterization and assessment of treatment response. Radiology. 2006;239:63249. 25. Schwingel R, Reis F, Zanardi VA, et al. Central nervous system lymphoma: magnetic resonance imaging features at presentation. Arq Neuropsiquiatr. 2012;70:97101. Universidade Estadual de Campinas (Unicamp), Campinas, SP, Brasil a. https://orcid.org/0000-0003-1191-4396 b. https://orcid.org/0000-0002-7391-1193 c. https://orcid.org/0000-0003-2256-4379 Correspondência: Dr. Fabiano Reis Universidade Estadual de Campinas Radiologia e Diagnóstico por Imagem Rua Vital Brasil, 241, Cidade Universitária Campinas, SP, Brasil, 13083-872 E-mail: fabianoreis2@gmail.com Recebido para publicação em 26/11/2019 Aceito, após revisão, em 18/3/2020 |
|
Av. Paulista, 37 - 7° andar - Conj. 71 - CEP 01311-902 - São Paulo - SP - Brazil - Phone: (11) 3372-4544 - Fax: (11) 3372-4554