Radiologia Brasileira - Publicação Científica Oficial do Colégio Brasileiro de Radiologia
AMB - Associação Médica Brasileira CNA - Comissão Nacional de Acreditação
 Vol. 53 nº 6 - Nov. / Dez. of 2020
Vol. 53 nº 6 - Nov. / Dez. of 2020
|
ENSAIO ICONOGRÁFICO
|
|
|
|
|
Autho(rs): Flavio Scavone Stefaninia; Franklin Wilson Caires Goisb; Tiago Cesar Silva Borba de Arrudac; Almir Galvão Vieira Bitencourtd; Wagner Santana Cerqueirae |
|
|
Descritores: Neoplasias ósseas/diagnóstico por imagem; Linfoma/patologia; Radiologia; Ressonância magnética. |
|
|
Resumo: INTRODUÇÃO
O linfoma ósseo primário (LOP) é uma doença rara, responsável por cerca de 37% de todas as neoplasias ósseas primárias, aproximadamente 5% dos linfomas extranodais e menos que 1% de todos os linfomas não Hodgkin(1,2), sendo o linfoma difuso de grandes células B o mais comum(14). São extremamente raros na população pediátrica e adulta jovem(2). Os critérios para o diagnóstico dessa entidade são amplamente aceitos e incluem: a) local primário de origem do tumor na medula óssea, sem outro sítio indicando a existência da lesão no exame físico ou de imagem; b) ausência de identificação de linfoma em qualquer outro local seis meses após o diagnóstico de LOP; c) o diagnóstico deve ser confirmado por patologia e imuno-histoquímica; d) os linfomas malignos, com exceção do LOP e do linfoma secundário do osso, devem ser excluídos(1). As lesões linfomatosas ósseas ocorrem mais frequentemente na metadiáfise(1), sendo o fêmur o local mais acometido, seguido por tíbia e úmero(5), apesar de haver grande divergência na literatura entre envolvimento apendicular versus axial, principalmente em estudos japoneses(3,6). Outros locais incluem pelve, crânio e pescoço(3,7). Lesões multifocais costumam ter envolvimento axial e apendicular(5). Na maioria das séries, o LOP é geralmente diagnosticado em pacientes entre 50 e 70 anos de idade, havendo predominância no sexo masculino(3). Clinicamente, se manifestam por dor local, massa palpável, fratura patológica, e alguns pacientes ainda podem evoluir com sintomas B (febre, sudorese noturna e perda ponderal). A apresentação clínica e os achados de imagem não são específicos, com amplo espectro de diagnósticos diferenciais possíveis, incluindo sarcoma de Ewing, osteossarcoma, condrossarcoma, metástases e histiocitose de células de Langerhans(2), no entanto, a avaliação minuciosa de padrões radiológicos específicos pode aumentar o nível de suspeição para LOP antes da biópsia tecidual. O objetivo deste trabalho é descrever os achados mais frequentes nos diferentes métodos de imagem utilizados em pacientes com LOP. CARACTERÍSTICAS GERAIS POR IMAGEM LOP é uma neoplasia com origem na medular óssea, apresenta padrão de imagem bastante variável, com achados que podem sobrepor a numerosas causas não neoplásicas, além de neoplasias benignas ou malignas. Uma característica marcante e frequente é de massa de tecido mole muito maior do que seria de esperar, dado o grau de destruição óssea cortical. Em outras palavras, extensão para partes moles com relativa preservação da cortical pode ser típica de LOP(4,7). Tem sido sugerido que esse padrão resulte de disseminação de pequenas células tumorais azuis e redondas pelo osso cortical através dos canais vasculares de Volkmann e Havers para os tecidos moles circundantes, em vez de uma franca ruptura cortical(4,7). RADIOGRAFIA A radiografia simples é empregada como avaliação inicial da queixa clínica, podendo mostrar achados que mereçam investigação adicional. Nesse contexto clínico, a aparência radiológica de um linfoma ósseo pode ser normal ou com discretas alterações texturais medulares(1) (Figura 1). A maioria dos relatos de LOP descreve um padrão osteolítico de destruição óssea permeativo com zona de transição larga ou roído de traça (Figura 2), e uma reação periosteal comumente descrita com aspecto lamelar, multilamelada em casca de cebola ou descontínua(1). 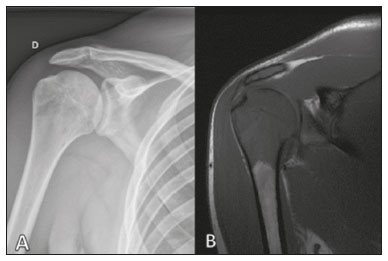 Figura 1. Paciente do sexo masculino, 36 anos, com dor espontânea no ombro sem melhora com uso de analgésicos. Radiografia em anteroposterior (A) do ombro demonstra alteração textura na metaepífise proximal do úmero. RM sequência T1 (B) mostra acometimento medular da metadiáfise e epífise umeral. 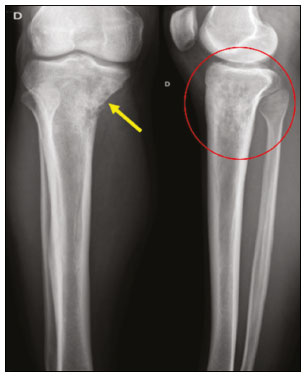 Figura 2. Paciente do sexo masculino, 22 anos, apresentando dor intermitente no joelho direito e progressiva limitação das atividades diárias. Radiografias simples da perna (anteroposterior e perfil) demonstram lesão intramedular mista, predominantemente osteolítica, na metadiáfise proximal da tíbia, com padrão roído de traça e zona de transição larga (círculo), associado a discretas irregularidades e áreas de descontinuidade cortical (seta). ULTRASSONOGRAFIA A ultrassonografia tem especificidade limitada para diagnosticar e diferenciar lesões do LOP. Sua principal função fica reservada para orientação e realização de punção ou biópsia percutânea em tumores ósseos que cursam com massa de tecidos moles extraóssea associada (Figura 3). A ultrassonografia pode ser usada em adição à RM quando artefatos de suscetibilidade secundários impedem a avaliação de áreas específicas(8). 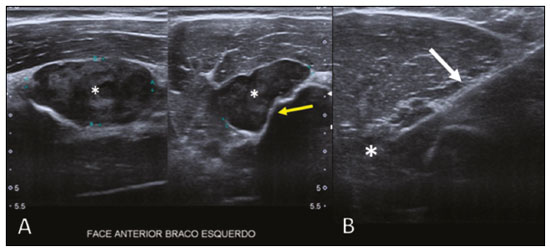 Figura 3. Paciente do sexo masculino, 30 anos, com dor no braço esquerdo e sintomas B, submetido a biópsia do componente de partes moles após biópsia óssea inconclusiva. Estudo por ultrassom delimita as dimensões do componente de partes moles (asteriscos) e mostra o trajeto da agulha da biópsia até o componente tumoral. A seta amarela identifica a cortical óssea relacionada ao tumor extraósseo e a seta branca indica a agulha de biópsia. TOMOGRAFIA COMPUTADORIZADA A tomografia computadorizada (TC), além de ser método muito utilizado para as biópsias nos casos de tumores ósseos (Figura 4), também é um excelente método para delinear a destruição cortical. Mesmo que as demais características identificadas sejam inespecíficas, o diagnóstico de LOP deve ser considerado sempre que se observar uma grande massa de tecido mole e atenuação medular anormal sem que haja uma destruição cortical extensa proporcional ao volume de lesão extraóssea(9). 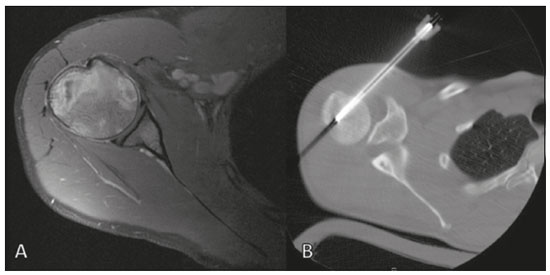 Figura 4. Mesmo paciente da Figura 1. Exame de RM em T1 pós-contraste (A) revela lesão infiltrativa na cabeça umeral. TC do úmero (B) utilizada para guiar biópsia percutânea. CINTILOGRAFIA ÓSSEA A cintilografia óssea com radionuclídeos (cintilografia com 99mTc) geralmente é inespecífica, mas ajuda a detectar qualquer área ativa no esqueleto, determinando se o tumor está latente ou em atividade(7). Nos casos de LOP, demonstra captação aumentada de traçador em 98% dos pacientes, com atividade marcadamente aumentada em 64%(7,10). PET/CT A PET/CT apresenta maior especificidade e sensibilidade que a cintilografia óssea convencional na identificação da infiltração linfomatosa do esqueleto(1). O LOP geralmente apresenta-se como uma lesão hipermetabólica no exame com fluordesoxiglicose (Figura 5). No acompanhamento de pacientes com LOP, a PET/CT é uma ferramenta importante para avaliar a presença de lesão viável, sendo utilizada inclusive para definir a resposta terapêutica. Muitas vezes, alterações pós-terapêuticas como necrose tumoral, tecido de granulação e/ou fibrose são difíceis de serem distinguidas de lesão tumoral remanescente nos exames de TC e/ou ressonância magnética (RM). Nesse contexto, a presença ou ausência de captação do radiomarcador em um exame de PET/CT ajuda a definir com mais precisão a natureza do tecido remanescente. 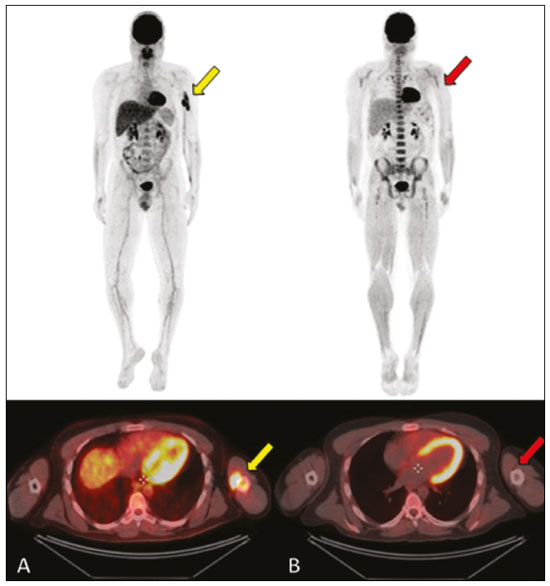 Figura 5. Exames de PET/CT antes (A) e após quimioterapia (B) do mesmo paciente da Figura 3. Observar resposta completa após tratamento quimioterápico, com resolução da captação do radiofármaco. RM A RM, pelo excelente contraste de partes moles entre tecidos e compartimentos, demonstra bem a relação com estruturas neurovasculares e mostra a extensão medular óssea, o tamanho e o volume da lesão. Permite a caracterização tecidual pela avaliação de intensidades de sinal com diferentes sequências de pulso, as características de realce pelo meio de contraste e a intensidade de restrição à difusão(4). As sequências ponderadas em T1 demonstram áreas de baixa intensidade de sinal, sendo, geralmente, a melhor sequência para identificar alterações do conteúdo medular. Nas sequências ponderadas em T2 observa-se sinal intermediário (Figura 6), na qual o edema peritumoral e a alteração reativa da medula podem produzir sinal elevado, mas variável de acordo com o grau de fibrose existente(1,4). Mostram realce variado pelo meio de contraste e, de acordo com sua celularidade, relativamente alta, os LOPs exibem difusão restrita com baixo valor de coeficiente de difusão aparente nas sequências ponderadas em difusão(1). 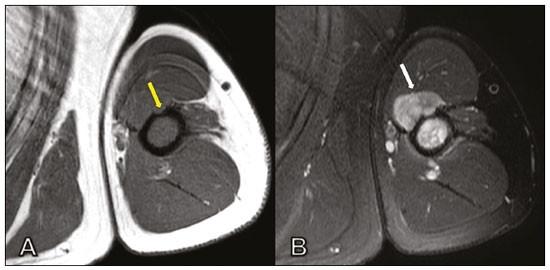 Figura 6. Mesmo paciente das Figuras 3 e 5. Imagens axiais de RM ponderadas em T1 (A) e T1 pós-contraste (B) demonstram defeito na cortical anterior (seta amarela) comunicando lesão intramedular com seu componente de partes moles (seta branca), representando extensão do tumor através dos canais vasculares/vasculoneurais. Por fim, a RM se configura como o melhor método de imagem para avaliar a extensão da lesão óssea para os compartimentos de partes moles e o grau do comprometimento cortical, que geralmente se encontra preservado, em virtude do padrão de penetração cortical permeativo (Figura 7)(9). 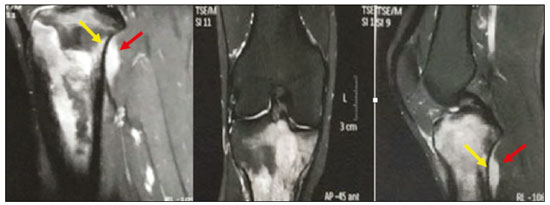 Figura 7. Mesmo paciente da Figura 2. Imagens de RM (em planos e cortes diferentes) demonstrando lesão óssea intramedular infiltrativa localizada na metadiáfise da tíbia proximal, mal delimitada, com baixo sinal em T1, alto sinal em T2 e realce heterogêneo pelo meio de contraste. Nota-se envolvimento de partes moles na região posteromedial (seta vermelha), com relativa preservação cortical quando se leva em consideração a extensão extraóssea (seta amarela). CONCLUSÃO Embora o LOP seja uma entidade rara e seu diagnóstico final seja realizado por meio de análise anatomopatológica e imuno-histoquímica, a avaliação radiológica é importante para diagnóstico precoce nas descobertas incidentais, orientação de biópsia, estadiamento, avaliação de comprometimento locorregional, assim como seguimento e avaliação de resposta. Uma vez que não há características de imagens específicas, o conhecimento clinicoepidemiológico, evolutivo e de imagem auxiliam no direcionamento do diagnóstico diferencial de LOP, e para isso contamos com um arsenal de métodos de imagem que os radiologistas e médicos gerais devem estar cientes, tanto na interpretação como na indicação mais adequada de cada modalidade. REFERÊNCIAS 1. Messina C, Christie D, Zucca E, et al. Primary and secondary bone lymphomas. Cancer Treat Rev. 2015;41:23546. 2. Elhassadi E. Primary lymphoma of bone literature review. J Orthop Oncol. 2017;3:1000119. 3. Matikas A, Briasoulis A, Tzannou I, et al. Primary bone lymphoma: a retrospective analysis of 22 patients treated in a single tertiary center. Acta Haematol. 2013;130:2916. 4. Caracciolo JT, Rose T, Bui MM. Primary lymphoma of bone: imaging findings to improve diagnosis of a rarely considered disease prior to biopsy. Open Journal of Clinical Diagnostics. 2015;5:97106. 5. Lim CY, Ong KO. Imaging of musculoskeletal lymphoma. Cancer Imaging. 2013;13:44857. 6. Maruyama D, Watanabe T, Beppu Y, et al. Primary bone lymphoma: a new and detailed characterization of 28 patients in a single-institution study. Jpn J Clin Oncol. 2007;37:21623. 7. Coley BL, Higinbotham NL, Groesbeck HP. Primary reticulum-cell sarcoma of bone; summary of 37 cases. Radiology. 1950;55:64158. 8. Van der Woude HJ, Vanderschueren G. Ultrasound in musculoskeletal tumors with emphasis on its role in tumor follow-up. Radiol Clin North Am. 1999;37:75366. 9. Weber MA, Papakonstantinou O, Nikodinovska VV, et al. Ewings sarcoma and primary osseous lymphoma: spectrum of imaging appearances. Semin Musculoskelet Radiol. 2019;23:3657. 10. Zhou HY, Gao F, Bu B, et al. Primary bone lymphoma: a case report and review of the literature. Oncol Lett. 2014;8:15516. 1. Departamento de Imagem, A.C.Camargo Cancer Center, São Paulo, SP, Brasil a. https://orcid.org/0000-0002-0738-177X b. https://orcid.org/0000-0002-8079-0123 c. https://orcid.org/0000-0002-4124-8032 d. https://orcid.org/0000-0003-0192-9885 e. https://orcid.org/0000-0003-0203-6376 Correspondência: Dr. Wagner Santana Cerqueira A.C.Camargo Cancer Center Departamento de Imagem Rua Professor Antônio Prudente, 211, Liberdade São Paulo, SP, Brasil, 01509-010 E-mail: wagner_scerqueira@yahoo.com.br Recebido para publicação em 9/12/2019 Aceito, após revisão, em 5/2/2020 |
|
Av. Paulista, 37 - 7° andar - Conj. 71 - CEP 01311-902 - São Paulo - SP - Brazil - Phone: (11) 3372-4544 - Fax: (11) 3372-4554