Radiologia Brasileira - Publicação Científica Oficial do Colégio Brasileiro de Radiologia
AMB - Associação Médica Brasileira CNA - Comissão Nacional de Acreditação
 Vol. 53 nº 3 - Maio / Jun. of 2020
Vol. 53 nº 3 - Maio / Jun. of 2020
|
ENSAIO ICONOGRÁFICO
|
|
|
|
|
Autho(rs): Abdallah de Paula Houat1,a; Augusto Castelli von Atzingen2,b; Fernanda Garozzo Velloni3,c; Rafael Andrade Santiago de Oliveira3,d; Ulysses dos Santos Torres4,e; Giuseppe DIppolito1,f |
|
|
Descritores: Carcinoma neuroendócrino; Tumores neuroendócrinos; Metástase neoplásica; Fígado. |
|
|
Resumo: INTRODUÇÃO
As neoplasias neuroendócrinas (NNEs) são um grupo heterogêneo de tumores com manifestações morfológicas e biológicas distintas que podem surgir em qualquer tecido, sendo o trato gastrointestinal (TGI) seu principal sítio primário (6674%)(1). Apresentam associações com fatores genéticos (síndrome neoplasia endócrina múltipla tipo I e síndrome de von Hippel-Lindau, entre outras), entretanto, a maioria compõe-se de tumores esporádicos. Nos últimos anos, principalmente em razão dos avanços dos métodos diagnósticos, tem-se observado um aumento da incidência de NNEs, passando de 1,52 para 7,41 casos por 100.000 habitantes, nos Estados Unidos, de 1973 a 2012(2). O diagnóstico da NNE envolve testes hormonais, estudo radiológico e anatomopatológico. Para os pacientes que apresentam sintomas decorrentes da produção hormonal, testes bioquímicos devem ser direcionados à síndrome correspondente, por exemplo, para a síndrome carcinoide (hipersecreção de serotonina), com o ácido 5-hidroxi-indolacético na urina de 24 horas. A cromogranina A é o biomarcador diagnóstico de escolha, pois é o mais sensível, sendo utilizado tanto nos casos sintomáticos como nos assintomáticos, além de ser importante no seguimento dos pacientes(3). A obtenção de amostras para estudo anatomopatológico tem grande importância para o diagnóstico definitivo. A via de acesso dependerá do sítio acometido por exemplo, por meio de ecoendoscopia nos casos de neoplasia pancreática ou percutânea quando há acometimento hepático. Neste caso, prefere-se o acesso percutâneo por ultrassonografia (US), porém, em casos mais difíceis, uma abordagem por tomografia computadorizada (TC) poderá ser realizada(1). As modalidades radiológicas utilizadas para detecção de NNEs incluem, principalmente, a TC, a ressonância magnética (RM) e estudos de medicina nuclear, principalmente a tomografia por emissão de pósitrons (PET/CT) com 18F-fluorodesoxiglicose (FDG) e gálio 68-dotatate(4). A TC e a RM são utilizadas para a localização e o estadiamento, demonstrando a extensão da lesão primária e a presença de metástases(4,5). Na maioria das vezes, independentemente da localização, as lesões são hipervasculares, e por isso a fase arterial é essencial nos protocolos de exame. No entanto, dependendo do tipo, tamanho e localização do tumor, as fases portal e tardia também são importantes para uma análise mais eficaz. Na RM, além do realce hipervascular, as lesões apresentam, geralmente, hipersinal em imagens ponderadas em T2 e expressiva restrição nas imagens com a técnica de difusão. Esta técnica, aliada ao uso do meio de contraste hepatoespecífico, tem permitido aumentar a sensibilidade da RM para detecção de metástases hepáticas, inclusive as por NNEs(46). A PET/CT, por sua vez, é utilizada na detecção tumoral e estadiamento, e também no monitoramento e orientação do tratamento nos pacientes com NNE. Além da localização da lesão, fornece informações fisiológicas representadas pelo aumento do metabolismo da glicose ou dos receptores da somatostatina, dependendo do grau de diferenciação do tumor. A FDG é usada principalmente para se visualizar a atividade metabólica das NNEs pouco diferenciadas, e o gálio 68-dotatate para tumores bem diferenciados(6). Aproximadamente 15% dos pacientes com NNE apresentam metástases, sendo o fígado o órgão mais afetado (4693%) e o sítio primário localizado geralmente no pâncreas e intestino delgado(7). O acometimento primário hepático é extremamente raro, com aproximadamente 150 casos relatados. O diagnóstico do acometimento hepático pela NNE é desafiador, em razão dos seus sintomas frustros, indolentes e frequentemente inespecíficos, estreita semelhança radiológica com outras lesões hepáticas e as suas variadas formas de apresentação(1). Atualmente, não há diretrizes definitivas para tratamento das NNEs hepáticas primária e secundária. O plano terapêutico é baseado no sítio, estágio e grau de diferenciação do tumor, e idade, comorbidades e sintomas dos pacientes, ou seja, um tratamento individualizado que requer a colaboração multidisciplinar, em que há disponíveis cirurgia, quimioterapia, radioterapia, quimioembolização arterial transcateter e análogos de somatostatina(1,8,9). Dada a diversidade dos tipos e das características clínicas das NNEs, atualmente não há consenso sobre o monitoramento desses pacientes após a terapia. Pode-se dizer que o acompanhamento de pacientes com metástases hepáticas é individualizado, com base no estado clínico do paciente (incluindo sintomas) e grau de diferenciação do tumor, utilizando-se uma combinação de análise laboratorial e de marcadores tumorais (incluindo cromogranina A), e achados de imagem (anatômica e funcional)(9). Para a NNE hepática primária (NNHP) deve-se procurar, na medida do possível, descartar a presença de um sítio extra-hepático primário, durante o acompanhamento evolutivo. Nesse sentido, a realização de exames complementares, como endoscopia, colonoscopia, broncoscopia, entre outros, pode ser necessária(10). O objetivo deste estudo é ilustrar as diversas formas de apresentações comuns e incomuns das NNEs hepáticas primária e secundária, para auxiliar no seu reconhecimento diagnóstico. NNHP A NNHP é rara, representando 0,3% de todos os tumores neuroendócrinos. A sua histogênese não é conhecida, tendo como possível origem células pancreáticas ou adrenais ectópicas no fígado, tecido neuroendócrino no epitélio biliar intra-hepático ou inflamação crônica no sistema biliar induzindo metaplasia intestinal(10). Esta neoplasia pode ocorrer em pacientes de qualquer idade, porém, é relatada principalmente na população adulta (40 a 50 anos), com distribuição semelhante entre os sexos(11). Não se conhecem fatores de risco e sua taxa de mortalidade é estimada em 25%; na maioria dos casos (80%) não é acompanhada de metástases no momento do diagnóstico(1). As NNHPs são tumores de crescimento lento e com manifestações clínicas ausentes ou inespecíficas, sendo mais frequentemente descobertos com base nos sintomas associados aos efeitos de massa no fígado e órgãos adjacentes, como icterícia, massa palpável e distensão e dor abdominal. A síndrome carcinoide clássica pode estar presente em cerca de 5% dos doentes(11). O diagnóstico pode ser desafiador, em razão da estreita semelhança radiológica com outras lesões hepáticas, tais como o carcinoma hepatocelular, o colangiocarcinoma, a doença hepática metastática, o cisto hidático, entre outras. Um dos critérios diagnósticos que caracteriza a NNHP é a ausência de lesão em outro sítio comumente afetado pelo tumor, como o intestino delgado, o pâncreas e os pulmões(12). Por este motivo, quando uma NNE é encontrada no fígado, é crucial procurar um sítio primário extra-hepático(10). As características radiológicas são pouco conhecidas, provavelmente por conta dos poucos casos descritos. São lesões geralmente únicas, heterogêneas, com realce hipervascular, mais evidente na periferia, realce tardio do centro da lesão, eventualmente com áreas císticas de permeio, correspondendo a necrose (Figura 1), e às vezes contendo nível líquido-líquido (Figura 2)(13,14). Na nossa experiência, este aspecto tem sido curiosamente recorrente nos casos estudados. 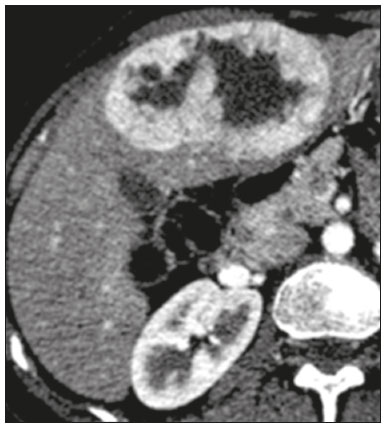 Figura 1. NNE hepática primária. TC fase arterial mostrando volumosa massa hepática heterogênea, com realce hipervascular e componente necrótico. 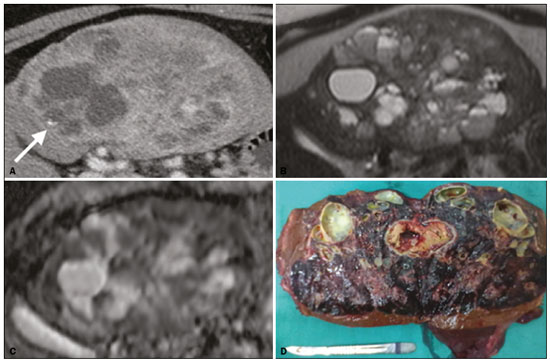 Figura 2. NNE hepática primária. TC fase arterial (A), RM pesada em T2 (B), mapa ADC (C) e peça cirúrgica com múltiplas formações císticas (D). Nota-se volumosa massa no lobo hepático esquerdo, heterogênea, com porção sólida apresentando realce hipervascular, componente multicístico caracterizado por áreas hipoatenuantes na TC e alto sinal em T2, algumas com nível líquido-líquido e foco de calcificação puntiforme (seta em A). Observa-se ainda intensa restrição à difusão da porção sólida da massa. METÁSTASE HEPÁTICA DE NNE A metástase hepática das NNEs representa cerca de 10% de todas as lesões secundárias do fígado, sendo este o principal órgão acometido. No momento do diagnóstico, pouco mais da metade das NNEs do TGI já apresentam comprometimento hepático e ocorrem, em média, sete anos após o surgimento da lesão primária. O principal sítio primário é o intestino delgado (íleo terminal)(7). A sua ocorrência depende principalmente da extensão da lesão primária, do grau de diferenciação e da sua atividade proliferativa. A metástase hepática é o preditor mais importante de sobrevida e que se encontra significativamente reduzida em cinco anos, quando se comparam pacientes com e sem comprometimento hepático (3040% × 7599%)(7,15). Embora a NNE do TGI tenha progressão lenta, alguns casos costumam ser sintomáticos devido principalmente a produção e hipersecreção hormonal em síndromes correspondentes. Em pacientes com tumores não funcionantes, os sintomas dependem do tamanho do tumor e da localização das metástases, sendo a dor abdominal não específica a clínica mais comum, seguida pela perda de peso(7). As lesões metastáticas se apresentam mais comumente como múltiplos nódulos hipervasculares (Figura 3)(15), à semelhança das metástases de tireoide, melanoma e carcinoma de células renais (Figura 4A). 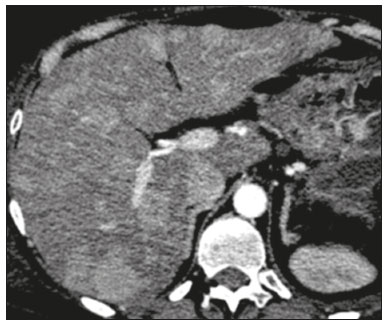 Figura 3. TC fase arterial. Metástase de NNE caracterizada por múltiplos nódulos hepáticos com realce hipervascular. 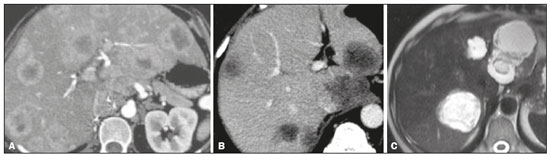 Figura 4. Alguns diagnósticos diferenciais de NNHS. Metástase hepática de carcinoma de células renais TC fase arterial (A), adenocarcinoma de cólon TC fase arterial (B) e sarcoma RM pesada em T2 (C). As metástases das NNEs também podem se apresentar como massas ou nódulos hipovasculares (Figura 5); em lesões maiores, a aparência pode ser cística por causa do componente de liquefação decorrente de necrose tumoral (Figura 5A)(15). Outros tumores que apresentam este mesmo padrão são as metástases do TGI (Figura 4B), do pulmão e dos sarcomas. 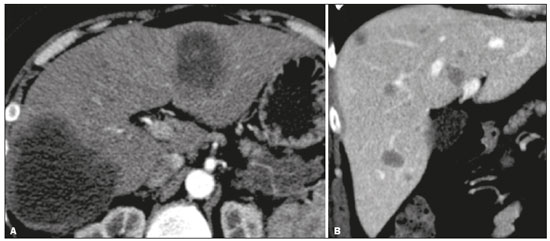 Figura 5. TC na fase arterial. Metástase de NNE caracterizada por massas (A) e múltiplos nódulos (B) com realce hipovascular. O acometimento hepático com componente de calcificação (Figura 6) não é frequente, tendo apenas alguns casos descritos(16). Já uma lesão com nível líquido-líquido é bastante sugestiva de alteração secundária de NNE (Figura 7), ocorrendo provavelmente por hemorragia/alto teor proteico relacionado à produção hormonal intralesional(17). No entanto, este aspecto também pode ser visto em metástases de sarcoma (Figura 4C) e de carcinoma de ovário. 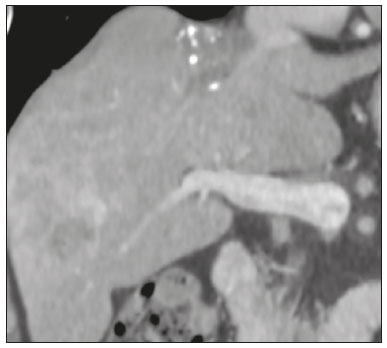 Figura 6. TC fase portal. Metástase hepática apresentando focos de calcificações de permeio. 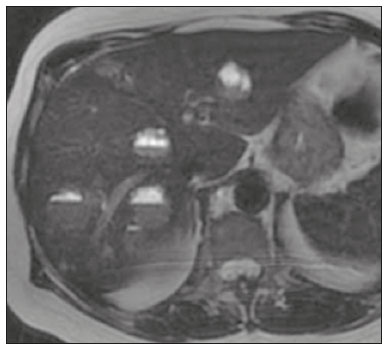 Figura 7. RM pesada em T2. Metástases hepáticas com componente cístico apresentando nível líquido-líquido. A lesão secundária de NNE pode se apresentar com deposição de gordura perilesional, a qual foi descrita especificamente para metástases de insulinoma. Acredita-se que isto esteja relacionado aos efeitos da insulina, ou seja, à inibição da oxidação de ácidos graxos e consequente acúmulo de triglicerídeos nos hepatócitos(18). O padrão de realce da metástase hepática da NNE pode orientar na busca do sítio primário. Por exemplo, uma lesão hipervascular sem clareamento portal pode estar relacionada ao sítio pancreático (Figuras 8A e 8B), enquanto uma lesão hipervascular com clareamento estaria mais frequentemente relacionada a lesões de origem entérica (Figuras 8C e 8D)(19). 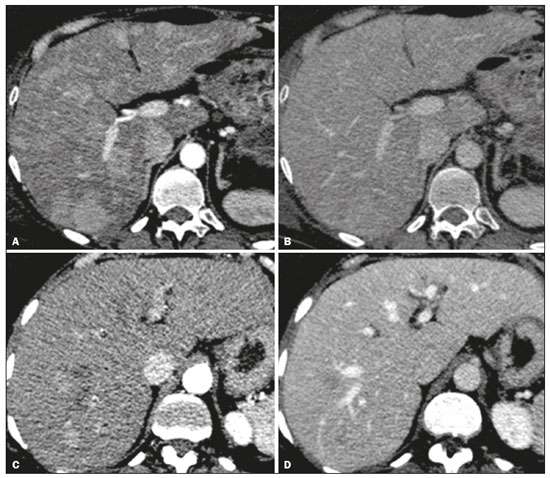 Figura 8. TC fase arterial (A,C) e TC fase portal (B,D). Múltiplos nódulos hepáticos com realce hipervascular (A,C) apresentando isoatenuação na fase portal em um caso de NNE pancreática (A,B) e hipoatenuação na fase portal em um caso de NNE ileal (C,D). O uso do meio de contraste hepatoespecífico associado a técnica de difusão, já descrita com alta acurácia na pesquisa de metástase hepática em paciente com câncer colorretal(20), também tem-se mostrado, na nossa experiência, mais eficaz que a TC na detecção de lesões secundárias hepáticas no contexto de NNEs(6) (Figura 9). 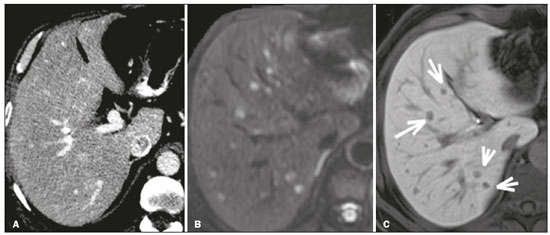 Figura 9. TC fase arterial (A), RM difusão com b = 800 s/mm2 (B) e RM fase hepatobiliar com 20 minutos (C). A TC mostra alguns nódulos hipervasculares esparsos no parênquima hepático. Porém, quando se observa a RM com contraste hepatoespecífico, analisando-se em conjunto a difusão e a fase hepatobiliar (setas em C), são caracterizados múltiplos nódulos hepáticos. CONCLUSÃO As NNEs primária e secundária do fígado possuem vasta gama de apresentações radiológicas que se confundem com outras lesões hepáticas. No entanto, alguns aspectos podem alertar para a sua origem, tais como a presença de múltiplas lesões hipervasculares coexistindo com massas ileais ou pancreáticas na doença metastática, ou massa única, com cavidades císticas e nível líquido, na sua forma primária. O papel do radiologista estende-se à sua participação no manejo, orientação terapêutica e acompanhamento deste grupo de pacientes. REFERÊNCIAS 1. Lin CW, Lai CH, Hsu CC, et al. Primary hepatic carcinoid tumor: a case report and review of the literature. Cases J. 2009;2:90. 2. Leoncini E, Boffetta P, Shafir M, et al. Increased incidence trend of low-grade and high-grade neuroendocrine neoplasms. Endocrine. 2017;58:36879. 3. Sippel RS, Chen H. Carcinoid tumors. Surg Oncol Clin N Am. 2006;15:46378. 4. Sahani DV, Bonaffini PA, Fernández-Del Castillo C, et al. Gastroenteropancreatic neuroendocrine tumors: role of imaging in diagnosis and management. Radiology. 2013;266:3861. 5. Morse B, Jeong D, Thomas K, et al. Magnetic resonance imaging of neuroendocrine tumor hepatic metastases: does hepatobiliary phase imaging improve lesion conspicuity and interobserver agreement of lesion measurements? Pancreas. 2017;46:121924. 6. Sundin A. Radiological and nuclear medicine imaging of gastroenteropancreatic neuroendocrine tumours. Best Pract Res Clin Gastroenterol. 2012;26:80318. 7. Frilling A, Sotiropoulos GC, Li J, et al. Multimodal management of neuroendocrine liver metastases. HPB (Oxford). 2010;12:36179. 8. Steinmüller T, Kianmanesh R, Falconi M, et al. Consensus guidelines for the management of patients with liver metastases from digestive (neuro)endocrine tumors: foregut, midgut, hindgut, and unknown primary. Neuroendocrinology. 2008;87:4762. 9. Madoff DC, Gupta S, Ahrar K, et al. Update on the management of neuroendocrine hepatic metastases. J Vasc Interv Radiol. 2006; 17:123549. 10. Zhao ZM, Wang J, Ugwuowo UC, et al. Primary hepatic neuroendocrine carcinoma: report of two cases and literature review. BMC Clin Pathol. 2018;18:3. 11. Quartey B. Primary hepatic neuroendocrine tumor: what do we know now? World J Oncol. 2011;2:20916. 12. Pedrassa BC, Rocha EL, Kierzenbaum ML, et al. Uncommon hepatic tumors: iconographic essay Part 2. Radiol Bras. 2014;47:3749. 13. van der Hoef M, Crook DW, Marincek B, et al. Primary neuroendocrine tumors of the liver: MRI features in two cases. Abdom Imaging. 2004;29:7781. 14. Yang K, Cheng YS, Yang JJ, et al. Primary hepatic neuroendocrine tumors: multi-modal imaging features with pathological correlations. Cancer Imaging. 2017;17:20. 15. Dromain C, de Baere T, Lumbroso J, et al. Detection of liver metastases from endocrine tumors: a prospective comparison of somatostatin receptor scintigraphy, computed tomography, and magnetic resonance imaging. J Clin Oncol. 2005;23:708. 16. Kawamoto T, Hishima T, Kimura K. Calcified liver metastases from a non-functioning pancreatic neuroendocrine tumor. Clin J Gastroenterol. 2014;7:4604. 17. Sommer WH, Zech CJ, Bamberg F, et al. Fluid-fluid level in hepatic metastases: a characteristic sign of metastases of neuroendocrine origin. Eur J Radiol. 2012;81:212732. 18. Kroncke TJ, Taupitz M, Kivelitz D, et al. Multifocal nodular fatty infiltration of the liver mimicking metastatic disease on CT: imaging findings and diagnosis using MR imaging. Eur Radiol. 2000;10: 1095100. 19. Ronot M, Cuccioli F, Dioguardi Burgio M, et al. Neuroendocrine liver metastases: vascular patterns on triple-phase MDCT are indicative of primary tumour location. Eur J Radiol. 2017;89:15662. 20. Koh DM, Collins DJ, Wallace T, et al. Combining diffusion-weighted MRI with Gd-EOB-DTPA-enhanced MRI improves the detection of colorectal liver metastases. Br J Radiol. 2012;85:9809. 1. Escola Paulista de Medicina da Universidade Federal de São Paulo (EPM-Unifesp), São Paulo, SP, Brasil 2. Universidade do Vale do Sapucaí (Univás), Pouso Alegre, MG, Brasil 3. Diagnósticos da América S/A (Dasa), Barueri, SP, Brasil 4. Grupo Fleury, São Paulo, SP, Brasil a. https://orcid.org/0000-0001-5543-2079 b. https://orcid.org/0000-0001-9009-1409 c. https://orcid.org/0000-0002-2019-7918 d. https://orcid.org/0000-0003-0838-3731 e. https://orcid.org/0000-0002-1911-9090 f. https://orcid.org/0000-0002-2701-1928 Correspondência: Dr. Abdallah de Paula Houat EPM-Unifesp Departamento de Diagnóstico por Imagem Rua Napoleão de Barros, 800, Vila Clementino São Paulo, SP, Brasil, 04024-002 E-mail: abdallah.houat@gmail.com Recebido para publicação em 14/3/2019 Aceito, após revisão, em 21/6/2019 Data de publicação: 15/04/2020 |
|
Av. Paulista, 37 - 7° andar - Conj. 71 - CEP 01311-902 - São Paulo - SP - Brazil - Phone: (11) 3372-4544 - Fax: (11) 3372-4554