Radiologia Brasileira - Publicação Científica Oficial do Colégio Brasileiro de Radiologia
AMB - Associação Médica Brasileira CNA - Comissão Nacional de Acreditação
 Vol. 52 nº 4 - Jul. / Ago. of 2019
Vol. 52 nº 4 - Jul. / Ago. of 2019
|
NOVIDADE EM RADIOLOGIA
|
|
|
|
|
Autho(rs): Tiago Kojun Tibana1; Renata Motta Grubert2; Denise Maria Rissato Camilo3; Edson Marchiori4; Thiago Franchi Nunes5 |
|
|
INTRODUÇÃO
A punção guiada por tomografia computadorizada (TC) é uma das técnicas de radiologia intervencionista mais utilizadas e inclui biópsias, drenagens e procedimentos de ablação por radiofrequência(18). Esta técnica varia muito de acordo com o método de imagem escolhido para guiar os procedimentos. Embora a desvantagem de usar a fluoro-TC como método em tempo real seja a sua tendência para aumentar a exposição à radiação ionizante(9,10), existem grandes vantagens em poder fornecer os locais de destino em tempo real, as posições dos órgãos circundantes e a localização da agulha de punção(11). No entanto, a sua instalação é de alto custo e a realidade é que muitas regiões e cidades não têm acesso à fluoro-TC. Portanto, o uso de uma técnica de punção não fluoroscópica continua a ser importante na prática atual(12). A técnica de punção convencional não fornece capacidade de orientação em tempo real para rastrear a agulha e a localização do alvo. O executante deve avançar a agulha seguindo o ângulo planejado com base em seus próprios sentidos. Este procedimento pode ser estressante, devido ao potencial de erros de punção, afetando órgãos vitais, levando eventualmente a complicações. Portanto, para evitar esses erros, é necessário um processo passo-a-passo, com a varredura intermitente da região de interesse para confirmar a localização da agulha cada vez que esta é avançada(12), aumentando, assim, a dose de radiação recebida pelo paciente. Para melhorar a conveniência e a precisão da técnica de punção convencional, pode-se utilizar um aplicativo de smartphone desenvolvido especificamente para auxiliar a orientação da punção(12), associado a um marcador radiodenso posicionado na pele. PROCEDIMENTO O local de punção e o ângulo são determinados da mesma maneira que a técnica convencional, calculado inicialmente pela estação de trabalho da TC, com subsequente marcação do local de punção na superfície corporal do paciente (Figura 1). 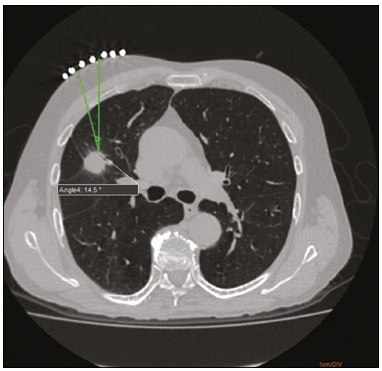 Figura 1. TC de tórax axial mostra o planejamento do local da punção, com cálculo do ângulo e marcação na pele entre os marcadores radiopacos (seta). O smartphone é colocado dentro de um plástico esterilizado para facilitar o processo de limpeza e melhorar a segurança do paciente. Uma vez que o ângulo de punção planejado é inserido no aplicativo, um guia é exibido na tela de LCD. Os sensores de movimento incorporados no dispositivo garantem que essa orientação seja constantemente mantida no ângulo desejado, independentemente do ângulo em que o dispositivo está sendo mantido ou se movimentando. A cor de fundo muda de acordo com o ângulo da tela: voltada para cima (rosa), tela voltada para baixo (azul) (Figura 2) e vertical (preto). O centro de rotação do guia move-se livremente no visor e pode ser bloqueado em qualquer local da tela, para que esteja alinhado com o local de punção desejado. O aparelho é finalmente colocado ao longo da linha do feixe marcado na superfície da pele do paciente e a punção é realizada alinhando-se a agulha, de acordo com a orientação mostrada no dispositivo (Figura 3). Isto evita desvios e permite a perfuração mais precisa e no ângulo apropriado (Figura 4). 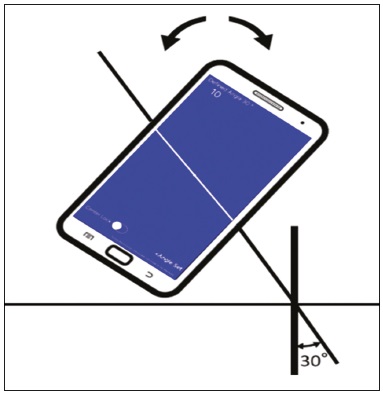 Figura 2. Ilustração mostrando situação hipotética de punção num ângulo de 30° com inclinação do visor para baixo (tela azul). 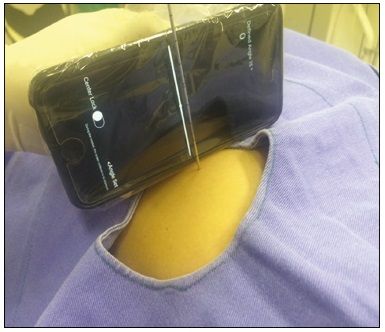 Figura 3. Inserção da agulha coaxial guiada pelo ângulo ajustado no aplicativo. 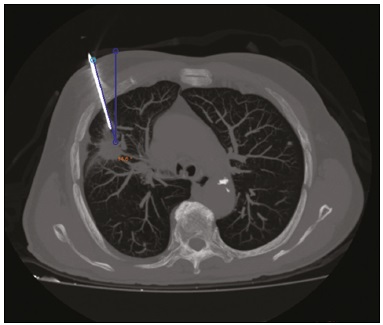 Figura 4. Reconstrução MIP de projeção axial demonstra inserção correta da agulha no ângulo pretendido. REFERÊNCIAS 1. Haaga JR, Alfidi RJ. Precise biopsy localization by computer tomography. Radiology. 1976;118:6037. 2. Haaga JR, Alfidi RJ, Havrilla TR, et al. CT detection and aspiration of abdominal abscesses. AJR Am J Roentgenol. 1977;128:46574. 3. Guimarães MD, Marchiori E, Hochhegger B, et al. CT-guided biopsy of lung lesions: defining the best needle option for a specific diagnosis. Clinics (Sao Paulo). 2014;69:33540. 4. Wile GE, Leyendecker JR, Krehbiel KA, et al. CT and MR imaging after imaging-guided thermal ablation of renal neoplasms. Radiographics. 2007;27:32539. 5. Tyng CJ, Santos EFV, Guerra LFA, et al. Computed tomographyguided percutaneous gastrostomy: initial experience at a cancer center. Radiol Bras. 2017;50:10914. 6. Cardarelli-Leite L, Fornazari VAV, Peres RR, et al. The value of percutaneous transhepatic treatment of biliary strictures following pediatric liver transplantation. Radiol Bras. 2017;50:30813. 7. Schiavon LHO, Tyng CJ, Travesso DJ, et al. Computed tomographyguided percutaneous biopsy of abdominal lesions: indications, techniques, results, and complications. Radiol Bras. 2018;51:1416. 8. Nunes TF. Percutaneous biopsy of abdominal lesions: what is currently the best diagnostic strategy? Radiol Bras. 2018;51(3):vvi. 9. Froelich JJ, Saar B, Hoppe M, et al. Real-time CT-fluoroscopy for guidance of percutaneous drainage procedures. J Vasc Interv Radiol. 1998;9:73540. 10. Silverman SG, Tuncali K, Adams DF, et al. CT fluoroscopy-guided abdominal interventions: techniques, results, and radiation exposure. Radiology. 1999;212:67381. 11. Daly B, Templeton PA. Real-time CT fluoroscopy: evolution of an interventional tool. Radiology. 1999;211:30915. 12. Hirata M, Watanabe R, Koyano Y, et al. Using a motion sensorequipped smartphone to facilitate CT-guided puncture. Cardiovasc Intervent Radiol. 2017;40:60915. 1. Hospital Universitário Maria Aparecida Pedrossian da Universidade Federal de Mato Grosso do Sul (HUMAP-UFMS), Campo Grande, MS, Brasil; https://orcid.org/0000-0001-5930-1383 2. Hospital Universitário Maria Aparecida Pedrossian da Universidade Federal de Mato Grosso do Sul (HUMAP-UFMS), Campo Grande, MS, Brasil; https://orcid.org/0000-0001-6713-2575 3. Hospital Universitário Maria Aparecida Pedrossian da Universidade Federal de Mato Grosso do Sul (HUMAP-UFMS), Campo Grande, MS, Brasil; https://orcid.org/0000-0002-9016-8610 4. Universidade Federal do Rio de Janeiro (UFRJ), Rio de Janeiro, RJ, Brasil; https://orcid.org/0000-0001-8797-7380 5. Hospital Universitário Maria Aparecida Pedrossian da Universidade Federal de Mato Grosso do Sul (HUMAP-UFMS), Campo Grande, MS, Brasil; https://orcid.org/0000-0003-0006-3725 Correspondência: Dr. Thiago Franchi Nunes Avenida Senador Filinto Müller, 355, Vila Ipiranga Campo Grande, MS, Brasil, 79080-190 E-mail: thiagofranchinunes@gmail.com Recebido para publicação em 29/3/2018 Aceito, após revisão, em 18/5/2018 |
|
GN1© Copyright 2025 - All rights reserved to Colégio Brasileiro de Radiologia e Diagnóstico por Imagem
Av. Paulista, 37 - 7° andar - Conj. 71 - CEP 01311-902 - São Paulo - SP - Brazil - Phone: (11) 3372-4544 - Fax: (11) 3372-4554
Av. Paulista, 37 - 7° andar - Conj. 71 - CEP 01311-902 - São Paulo - SP - Brazil - Phone: (11) 3372-4544 - Fax: (11) 3372-4554