Radiologia Brasileira - Publicação Científica Oficial do Colégio Brasileiro de Radiologia
AMB - Associação Médica Brasileira CNA - Comissão Nacional de Acreditação
 Vol. 51 nº 5 - Set. / Out. of 2018
Vol. 51 nº 5 - Set. / Out. of 2018
|
ARTIGOS ORIGINAIS
|
|
|
|
|
Autho(rs): Felipe Costa Moreira1; André Yui Aihara2; Henrique Manoel Lederman2; Ivan Torres Pisa1; Josceli Maria Tenório1 |
|
|
Descritores: Técnicas de apoio para a decisão; Neoplasias ósseas; Saúde da criança; Diagnóstico diferencial; Erros de diagnóstico; Diagnóstico por imagem. |
|
|
Resumo: INTRODUÇÃO
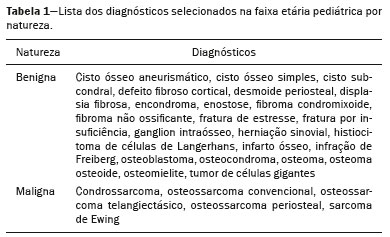
Os tumores ósseos malignos primários constituem a minoria de todas as neoplasias ósseas. Os tumores ósseos benignos são mais comuns, mas a verdadeira prevalência é desconhecida porque eles são frequentemente assintomáticos e não são descobertos. De fato, a apresentação clínica de tumores ósseos pode ser um desafio. Algumas lesões são acidentalmente encontradas em estudo radiográfico de rotina, e dependendo da sua aparência e das hipóteses diagnósticas, as próximas técnicas de imagem a serem utilizadas devem ser a tomografia computadorizada e a ressonância magnética, de acordo com os critérios do American College of Radiology(1). Diante de uma lesão óssea utilizam-se, rotineiramente, parâmetros clínicos e de imagem para definir o diagnóstico final e, mais importante, se a lesão é benigna ou maligna, com boa margem de segurança. Estudos têm descrito um padrão de varredura visual de médicos radiologistas na avaliação de imagens médicas(2-5). Embora existam padrões comuns de comportamento de pesquisa visual entre radiologistas com nível de experiência semelhante, ainda há grande variabilidade no seu processo de erro(6). Além disso, nem todo profissional tem conhecimento sedimentado e treinamento adequado para combinar achados radiológicos e clínicos com o objetivo de formular de forma segura um raciocínio lógico para a tomada de decisão quanto a benignidade ou malignidade de uma lesão, tampouco para sugerir hipóteses de diagnóstico final(7). Tal fato predispõe a erros de diagnóstico e impacto negativo, sobretudo à saúde física e psicológica de pacientes e familiares. Nesse cenário, os sistemas de suporte à decisão clínica e diagnóstica vêm contribuindo significativamente para a gestão do conhecimento médico, apoiando processos e o uso do conhecimento, desde o diagnóstico e investigação até o tratamento e cuidados de longa duração. Seu papel e aceitação na prática clínica diária está aumentando. A informatização das diretrizes clínicas tem atraído interesse nos últimos anos, por facilitar a sua divulgação e por melhorar o processo baseado no conhecimento pelo qual eles são produzidos(8). Os mapas cognitivos têm contribuído com parte da evolução desses sistemas de apoio a decisão. Segundo Bougon(9), mapa cognitivo é um termo genérico para representar possíveis padrões de relações entre conceitos. As palavras e frases que os indivíduos enunciam para expressar ideias ou conceitos em um dado contexto constituem os blocos para a construção do mapa cognitivo. Swan(10) diferencia os mapas das técnicas de mapeamento. Para ele, o mapeamento cognitivo é entendido como o conjunto de técnicas ou ferramentas de pesquisa voltadas para identificar os elementos que integram esses mapas ou modelos construídos pelos indivíduos e partilhados, em maior ou menor grau, por outros indivíduos. O mapa cognitivo é usado para identificar valores de um indivíduo ou grupo de indivíduos e reduzir o antagonismo entre esses valores. Sua capacidade de capturar múltiplos valores e reduzir seus aspectos conflitantes fornece uma lógica para a análise de problemas de decisão com partes interessadas(11). O objetivo do presente estudo é apresentar um mapa cognitivo para suporte no diagnóstico radiológico, com determinação da natureza benigna ou maligna de tumores ósseos solitários na faixa etária pediátrica - crianças e adolescentes de 0 a 19 anos(12). O mapa foi construído com base em um modelo de rede de crenças bayesianas(13), usando multicritérios sequenciais baseados em atributos clínicos e radiológicos específicos que podem ser obtidos por métodos de radiografia simples, tomografia computadorizada e ressonância magnética. MATERIAIS E MÉTODOS O método utilizado para a construção da estrutura cognitiva final foi o modelo de rede de crenças bayesianas(13) com a técnica de encadeamento regressivo (back-ward chaining)(14). Uma rede bayesiana - rede de crenças ou modelo de gráfico acíclico dirigido - é um modelo gráfico probabilístico que representa um conjunto de variáveis (nós) e suas interdependências condicionais. Os nós podem representar observáveis médicas, tais como achados de imagem, atributos clínicos, etc., enquanto as arestas interligadas podem apoiar medidas de origem quantitativa ou qualitativa para descrever a relação dada. Os nós podem ser conhecidos com certeza ou serem descritos como incertezas por meio de uma probabilidade subjetiva. As probabilidades subjetivas expressam o grau de crença de uma pessoa, tendo em conta o seu conhecimento de base. Essa noção de probabilidade difere da probabilidade clássica mais comumente usada(15,16). A construção de uma rede de crenças segue um conjunto comum de diretrizes, como incluir todos os conceitos (entrada e conceitos de decisão) para modelagem de sistemas, usar conhecimento causal para atribuir interconexões no gráfico e usar conhecimento prévio para especificar distribuições condicionais (probabilidades)(13). Já o processo de encadeamento regressivo parte do atributo final (diagnóstico) e busca apenas os valores das variáveis necessárias para sua dedução, processando somente o que for relevante para a obtenção do diagnóstico(14). Os passos para a construção do mapa cognitivo consistem de aquisição de conhecimento, seleção de diagnósticos, agrupamento de lesões e encadeamento regressivo (Figura 1). Para iniciar a construção dessa estrutura, foi realizado um processo de aquisição de conhecimento baseado na literatura, em busca dos principais tumores ósseos que fazem parte da lista de diferenciais na faixa etária pediátrica(1,17-22). Foi realizada uma seleção de 23 lesões benignas e 5 lesões malignas principais usando como critério de inclusão as mais comuns na faixa etária de 0 a 19 anos e seus principais diferenciais, mesmo que de baixa incidência na faixa pediátrica(21) (Tabela 1). Foram incluídos diagnósticos mais relevantes e com maior impacto no seguimento e estado de saúde dos pacientes, como tumores ósseos malignos, que, apesar de raros, apresentam alto grau de morbimortalidade. Por último, foram incluídas lesões que representam achados altamente específicos (patognomônicos), que, mesmo com baixa incidência na faixa etária pediátrica, quando encontradas, pode-se fechar com segurança o seu diagnóstico, como fraturas de estresse e infração de Freiberg (Tabela 2). Lesões tipicamente inespecíficas não foram incluídas, em razão de as diferentes formas de apresentação nos estudos de imagem poderem simular qualquer outro tumor.  Após a seleção dos tumores, foram identificados achados característicos e associados a cada diagnóstico radiológico (Tabela 3). Os termos utilizados foram escolhidos segundo a bibliografia selecionada(1,17-21). As principais características radiográficas que devem ser avaliadas diante de uma lesão óssea são localização (longitudinal e transversal), margens e zona de transição, reação periosteal, mineralização, tamanho, número de lesões (esta não foi aplicada no estudo, porque trata apenas de avaliação de lesões solitárias) e presença de componente de partes moles(22). Foram considerados, também, achados radiológicos como realce pelo meio de contraste, localização no esqueleto e achados com alto grau de especificidade para determinadas lesões, como formação de nível líquido-líquido, aspecto em vidro fosco, linha serpiginosa, lesões densas/escleróticas e localização subcondral. Alguns achados clínicos também foram considerados para oferecer suporte e aumentar a especificidade do diagnóstico final.  Inicialmente, foram separadas as lesões relacionadas a esses achados de alto grau de especificidade e que, por isso, se associam a apenas um diagnóstico (patognomônico) ou dois diagnósticos possíveis. Em seguida, foi feita uma avaliação conceitual do sistema de classificação para taxa de agressividade de Lodwick(23) (Tabela 4). Essa classificação é amplamente utilizada na previsão da taxa de crescimento para lesões ósseas líticas e considera como aspectos mais relevantes para estadiamento radiológico os seguintes critérios: destruição óssea, definição das margens, esclerose marginal, expansão cortical maior ou menor que 1 cm e penetração cortical. Desses critérios, a esclerose marginal é o único que só pode ser encontrado no estágio I-A (baixo grau; não agressivo) e, portanto, foi considerado o critério mais importante (maior grau de especificidade) para definir a natureza benigna das lesões, também conhecidas como lesões do tipo não toque. Os demais foram combinados para formar dois outros grupamentos, sendo um com lesões equivalentes aos estágios I-B e I-C de Lodwick (médio grau; moderadamente agressivo), possivelmente benignas, e outro grupo com lesões definitivamente suspeitas, equivalente aos estágios II e III de Lodwick (alto grau; muito agressivo). Após a distribuição das lesões em quatro grupos, foram aplicados a cada grupo os demais achados radiológicos, de forma sucessiva, partindo-se dos critérios de menor especificidade para os critérios de maior especificidade. Assim, formou-se um encadeamento regressivo ordenado por especificidade de critérios até o diagnóstico final (maior especificidade). Foi utilizado o software CMapTools, de uso gratuito e código aberto, para a construção gráfica de uma estrutura linear e acíclica por meio de nós e arestas estruturados na forma semelhante a uma árvore de decisão, usando os atributos clínicos e radiológicos. Após a construção do mapa cognitivo, dois médicos radiologistas especialistas e experientes, um especialista em musculoesquelético e outro em radiologia pediátrica, com 21 e 44 anos de atividade profissional, respectivamente, foram consultados para validação e ajustes do mapa cognitivo final, com conceitos radiológicos e clínicos aplicados ao diagnóstico de tumores ósseos pediátricos. RESULTADOS O mapa inicia-se de uma lesão óssea solitária, em princípio indeterminada. Logo no início sofre a primeira ramificação, contemplando lesões que são facilmente identificáveis e com achados característicos. Nesse ponto observa-se a subdivisão de três pequenos ramos: um contendo lesões blásticas bem definidas, como osteoma, enostose, displasia fibrosa e metástases de mama e próstata; outro pequeno grupo de lesões líticas epifisárias com localização tipicamente subcondral, entre elas cisto subcondral degenerativo e ganglion cístico intraósseo; e o terceiro contendo apenas infarto ósseo com seu achado característico de linha serpiginosa periférica. Caso não apresente nenhuma dessas características, o mapa progride para um próximo nó, que se subdivide em duas grandes ramificações, uma com lesões que apresentam esclerose perilesional e outra sem esse achado. O ramo de lesões com esclerose perilesional, a partir desse ponto, inicia o processo de encadeamento regressivo, até os diagnósticos finais, como se pode observar em um de seus ramos principais (Figura 2). Já o ramo com lesões não associadas a esclerose perilesional é, por sua vez, subdividido em outros dois ramos, utilizando os demais critérios da classificação de Lodwick - um contemplando lesões suspeitas e outro de lesões com características de agressividade. O grupo de lesões suspeitas inicia o processo de encadeamento regressivo. Entretanto, o ramo das lesões com características agressivas, antes do processo de encadeamento regressivo, passa por um pequeno filtro para separar algumas lesões benignas que se manifestam radiologicamente com atributos de agressividade, mas que, quando associadas a determinados achados ou ocorrência em determinada localização no esqueleto, podem ser diagnosticadas e sugeridas sem muita dificuldade, como fratura de estresse/insuficiência ou infração de Freiberg, por exemplo. 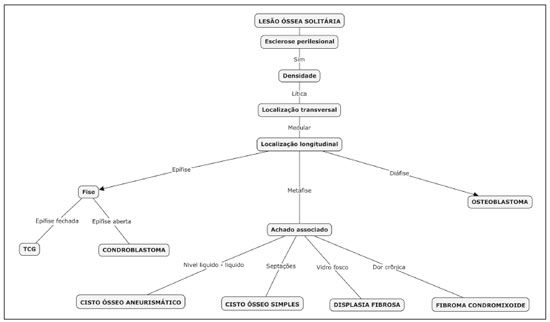 Figura 2. Ramo do mapa cognitivo construído que representa parcialmente o grupo das lesões benignas. TCG, tumor de células gigantes. DISCUSSÃO A decisão e o raciocínio para o diagnóstico apropriado do câncer ósseo são um problema complexo que envolve critérios subjetivos de decisão e uma variedade de diferenciais possíveis. Além disso, erros diagnósticos podem surgir por diversas razões que envolvem o profissional, o ambiente de trabalho ou ambos(24). Esses erros podem causar impactos negativos aos pacientes e familiares. Podem ainda trazer consequências econômicas a distintos atores envolvidos, como o agente público, os planos de saúde, os profissionais de saúde, etc.(25), por exigir novas abordagens diagnósticas potencialmente desnecessárias. Isso sem considerar as consequências jurídicas que também podem advir desses erros. Diante desse contexto, vale ressaltar que mais importante que o diagnóstico final é a definição na natureza ou grau de agressividade de uma lesão óssea. De fato, é com base nessa definição que decisões serão tomadas sobre o seguimento, necessidade de novas técnicas de imagem, indicação de manipulação cirúrgica ou biópsia. O presente estudo não é pioneiro ao apresentar uma estrutura para classificação de lesões tumorais. Entretanto, o número de estudos que relatam a aplicação de redes bayesianas ao câncer é limitado. Além disso, a maioria dos resultados publicados é de estudos preliminares que se baseiam em dados de pacientes(26). Forsberg et al.(27) realizaram um estudo que visou determinar a viabilidade do desenvolvimento de classificadores bayesianos para estimar a sobrevida em pacientes submetidos a cirurgia para metástases do esqueleto axial e apendicular. Para isso, desenvolveram e treinaram um modelo de rede bayesiana para estimar a sobrevivência em meses, usando características de candidatos com base em dados históricos. Já Kharya et al.(28) realizaram um estudo de utilização da rede bayesiana no domínio do câncer de mama. Esse tipo de modelo é apropriado em razão da sua capacidade de representação simbólica e do manuseio de incerteza no qual diferentes cenários são possíveis segundo evidências dadas. Esses autores pesquisaram a utilidade de uma rede para detecção automatizada do câncer de mama e constataram tratar-se de uma técnica potencialmente útil. No nosso estudo foi desenvolvido um mapa cognitivo seguindo um método de mapeamento bem definido usando um modelo de rede bayesiana que pudesse emular um raciocínio lógico e sequencial para o diagnóstico de tumores ósseos pediátricos. Acredita-se que esse mapa pode contribuir para minimizar os esforços e erros na definição da agressividade de uma lesão e na sugestão de um diagnóstico final. Ainda, pode colaborar com médicos radiologistas menos experientes ao fornecer uma estrutura organizada e sistematizada do raciocínio lógico humano. Por exemplo, esse mapa pode apoiar a formulação de hipóteses mais robustas e orientar médicos ortopedistas na condução e tratamento de lesões desconhecidas. Como limitação deste estudo, é importante relatar que nem todos os tumores possíveis dentro do universo oncológico ósseo pediátrico puderam ser incluídos, o que, consequentemente, resulta em um menor poder de assertividade e de acurácia. Além disso, há outras limitações, como a própria característica acíclica da estrutura, impedindo que seja possível transitar entre os diversos ramos da árvore - como ocorre com redes em forma de grafo -, impedindo que diagnósticos de ramos diferentes sejam apresentados em conjunto frente a uma combinação de achados diferentes das previstas e pré-formuladas presentes no mapa. Ou seja, o mapa cognitivo aqui proposto é uma primeira versão de uma combinação determinística e limitada de tumores e respectivos atributos. Não foram encontradas, na literatura consultada, definições claras dos graus de especificidade e sensibilidade dos achados radiológicos de tumores ósseos, o que, por si só, impossibilitou o uso de abordagem quantitativa na distribuição e organização dos multicritérios. Por isso, foi adotado um método predominantemente qualitativo e subjetivo para a construção do mapa cognitivo. Como atividade futura acredita-se que um levantamento estatístico para apresentar de maneira precisa o grau de especificidade de cada achado em relação a determinados tumores será útil, porque possibilitará a inclusão de probabilidades nos diversos níveis e ramos do mapa. Está em curso a construção de um aplicativo capaz de auxiliar um usuário a navegar anterogradamente ou retrogradamente nos ramos da árvore. Além disso, será introduzido um mecanismo de ensino que consiste em apresentar, junto aos nós e arestas do mapa, informação e conteúdo teórico. Estão planejadas avaliações com grupos de residentes, com o objetivo de medir a acurácia do mapa e sua aceitação como apoio ao raciocínio em prol do diagnóstico de lesões ósseas pediátricas. CONCLUSÃO A complexidade na decisão e o raciocínio para o diagnóstico de câncer ósseo podem gerar inúmeras consequências negativas secundárias a erros iatrogênicos no diagnóstico de uma lesão óssea. Nem todos os profissionais têm acesso a treinamento e educação adequados que os capacite a uma cognição lógica correta em cima de uma lesão óssea. Este trabalho propõe um mapa cognitivo para auxiliar no diagnóstico radiológico de tumores ósseos solitários na faixa pediátrica. Com base nesse mapa será possível oferecer um aplicativo para apoio a profissionais e residentes médicos e colaborar com o treinamento nessa área e, consequentemente, diminuir erros no diagnóstico de uma lesão óssea. REFERÊNCIAS 1. Ladd LM, Roth TD. Computed tomography and magnetic resonance imaging of bone tumors. Semin Roentgenol. 2017;52:209-26. 2. Alamudun F, Yoon HJ, Hudson KB, et al. Fractal analysis of visual search activity for mass detection during mammographic screening. Med Phys. 2017;44:832-46. 3. Kundel HL, Wright DJ. The influence of prior knowledge on visual search strategies during the viewing of chest radiographs. Radiology. 1969;93:315-20. 4. Kundel HL, Nodine CF, Carmody D. Visual scanning, pattern recognition and decision-making in pulmonary nodule detection. Invest Radiol. 1978;13:175-81. 5. Manning DJ, Ethell SC, Donovan T. Detection or decision errors? Missed lung cancer from the posteroanterior chest radiograph. Br J Radiol. 2004;77:231-5. 6. Voisin S, Pinto F, Morin-Ducote G, et al. Predicting diagnostic error in radiology via eye-tracking and image analytics: preliminary investigation in mammography. Med Phys. 2013;40:101906. 7. Lubarsky S, Dory V, Duggan P, et al. Script concordance testing: from theory to practice: AMEE guide no. 75. Med Teach. 2013;35: 184-93. 8. Douali N, Papageorgiou EI, De Roo J, et al. Clinical decision support system based on fuzzy cognitive maps. J Comput Sci Syst Biol. 2015;8:112-20. 9. Bougon MG. Uncovering cognitive maps: the self-Q technique. In: Morgan G, editor. Beyond method: strategies for social research. Los Angeles, CA: Sage Publications; 1983. p. 173-88. 10. Swan J. Using cognitive mapping in management research: decisions about technical innovation. Br J Manag. 1997;8:183-98. 11. Kpoumié A, Damart S, Tsoukiàs A. Integrating cognitive mapping analysis into multi-criteria decision aiding. 2012. <hal-01510937> 12. World Health Organization. Young people's health-a challenge for society. Report of a WHO Study Group on Young People and "Health for All by the Year 2000". Geneva: WHO Technical Report Series, 731; 1986. 13. Douali N, Csaba H, De Roo J, et al. Diagnosis support system based on clinical guidelines: comparison between case-based fuzzy cognitive maps and Bayesian networks. Comput Methods Programs Biomed. 2014;113:133-43. 14. Suner A, Çelikoglu CC, Dicle O, et al. Sequential decision tree using the analytic hierarchy process for decision support in rectal cancer. Artif Intell Med. 2012;56:59-68. 15. Cooper GF. The computational complexity of probabilistic inference using bayesian belief networks. Artificial Intelligence. 1990; 42:393-405. 16. Cooper GF. A method for using belief networks as influence diagrams. Proceedings of the Fourth Conference on Uncertainty in Artificial Intelligence; 1988 July 10-12; Minneapolis, MN. 17. Mehta K, McBee MP, Mihal DC, et al. Radiographic analysis of bone tumors: a systematic approach. Semin Roentgenol. 2017;52: 194-208. 18. Tselikas L, Joskin J, Roquet F, et al. Percutaneous bone biopsies: comparison between flat-panel cone-beam CT and CT-scan guidance. Cardiovasc Intervent Radiol. 2015;38:167-76. 19. Nguyen M, Beaulieu C, Weinstein S, et al. The incidental bone lesion on computed tomography: management tips for abdominal radiologists. Abdom Radiol (NY). 2017;42:1586-605. 20. Benndorf M, Neubauer J, Langer M, et al. Bayesian pretest probability estimation for primary malignant bone tumors based on the Surveillance, Epidemiology and End Results Program (SEER) database. Int J Comput Assist Radiol Surg. 2017;12:485-91. 21. Silva FD, Pinheiro L, Cristofano C, et al. Magnetic resonance imaging in pediatric bone tumors. Curr Radiol Rep. 2014;2:77. 22. Miller TT. Bone tumors and tumorlike conditions: analysis with conventional radiography. Radiology. 2008;246:662-74. 23. Caracciolo JT, Temple HT, Letson GD, et al. A modified Lodwick-Madewell grading system for the evaluation of lytic bone lesions. AJR Am J Roentgenol. 2016;207:150-6. 24. Boushehri E, Soltani-Arabshahi K, Monajemi A. Clinical reasoning assessment through medical expertise theories: past, present and future directions. Med J Islam Repub Iran. 2015;29:222. 25. Newman-Toker DE, McDonald KM, Meltzer DO. How much diagnostic safety can we afford, and how should we decide? A health economics perspective. BMJ Qual Saf. 2013;22 Suppl 2:ii11-ii20. 26. Sesen MB, Nicholson AE, Banares-Alcantara R, et al. Bayesian networks for clinical decision support in lung cancer care. PLoS One. 2013;8:e82349. 27. Forsberg JA, Eberhardt J, Boland PJ, et al. Estimating survival in patients with operable skeletal metastases: an application of a bayesian belief network. PLoS One. 2011;6:e19956. 28. Kharya S, Agrawal S, Soni S. Using Bayesian belief networks for prognosis & diagnosis of breast cancer. IJARCCE. 2014;3:5423-7. 1. Departamento de Informática em Saúde, Escola Paulista de Medicina da Universidade Federal de São Paulo (EPM-Unifesp), São Paulo, SP, Brasil 2. Departamento de Diagnóstico por Imagem, Escola Paulista de Medicina da Universidade Federal de São Paulo (EPM-Unifesp), São Paulo, SP, Brasil Correspondência: Felipe Costa Moreira EPM-Unifesp - Departamento de Informática em Saúde Rua Botucatu, 862, Vila Clementino São Paulo, SP, Brasil, 04021-001 E-mail: felipecmed@gmail.com Received July 20, 2017 Accepted after revision September 14, 2017 Trabalho realizado no Departamento de Informática em Saúde da Escola Paulista de Medicina da Universidade Federal de São Paulo (EPM-Unifesp), São Paulo, SP, Brasil |
|
Av. Paulista, 37 - 7° andar - Conj. 71 - CEP 01311-902 - São Paulo - SP - Brazil - Phone: (11) 3372-4544 - Fax: (11) 3372-4554