Radiologia Brasileira - Publicação Científica Oficial do Colégio Brasileiro de Radiologia
AMB - Associação Médica Brasileira CNA - Comissão Nacional de Acreditação
 Vol. 51 nº 2 - Mar. / Abr. of 2018
Vol. 51 nº 2 - Mar. / Abr. of 2018
|
CARTAS AO EDITOR
|
|
|
|
|
Autho(rs): Renato Niemeyer de Freitas Ribeiro1; Bruno Niemeyer de Freitas Ribeiro2; Wolney de Andrade Martins1; Lívia de Oliveira Antunes3; Edson Marchiori4 |
|
|
Sr. Editor,
Paciente do sexo feminino, 74 anos de idade, realizando rastreio para neoplasia devido a emagrecimento nos últimos seis meses, sem outras queixas associadas. Portadora de hipertensão arterial e diabetes mellitus, com bom controle medicamentoso. Durante a investigação foi demonstrado, na tomografia computadorizada (TC) de tórax, espessamento do septo interatrial (SIA) medindo 2,4 cm, devido a componente com densidade de gordura, poupando a fossa oval (Figuras 1A, 1B e 1C). A avaliação complementar por ecocardiograma transesofágico corroborou os achados prévios (Figura 1D). Com base em tais dados, foi confirmado o diagnóstico de hipertrofia lipomatosa do septo interatrial (HLSIA). 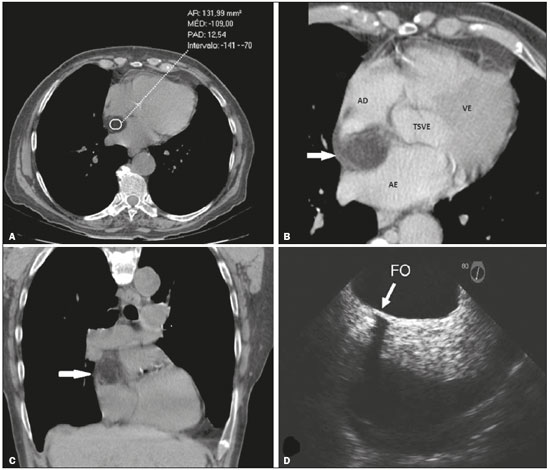 Figura 1. A: TC sem contraste demonstrando espessamento do SIA, medindo 2,4 cm e com densidade de 109 UH, caracterizando a infiltração gordurosa. B: TC pós-contraste, reformatação angulada para as quatro câmaras cardíacas, demonstrando o espessamento do SIA sem evidência de realce pelo meio de contraste (seta). C: TC sem contraste, corte coronal, demonstrando a infiltração gordurosa do SIA (seta). D: Ecocardiograma transesofágico demonstrando o espessamento do SIA poupando a fossa oval (seta). AD, átrio direito; AE, átrio esquerdo; VE, ventrículo esquerdo; TSVE, trato de saída do ventrículo esquerdo; FO, fossa oval. A avaliação do sistema cardiovascular por métodos de imagem tem sido motivo de uma série de publicações recentes na literatura radiológica nacional(14). A HLSIA é caracterizada pela deposição excessiva de gordura no SIA, poupando a fossa oval e fazendo com que o diâmetro transverso do septo ultrapasse 2 cm(59). Existe predileção pelo sexo feminino, com acometimento preferencialmente em idosos, e associação reconhecida ao uso de corticoide, obesidade e enfisema pulmonar(58). Na maioria dos casos apresenta-se como um achado incidental nos exames de imagem, porém, raramente pode determinar obstrução da veia cava e arritmias cardíacas, especialmente de origem atrial. Na avaliação por imagem, o ecocardiograma é limitado em demonstrar o tecido que compõe as massas cardíacas, sendo, portanto, fundamentais a TC e a ressonância magnética (RM) para avaliação complementar. Tais métodos são capazes de individualizar o espessamento do SIA, maior que 2 cm, poupando a fossa oval e podendo assumir o aspecto em haltere, assim como caracterizar a infiltração gordurosa do SIA por densidades entre 80 e 120 UH na TC e hipersinal em T1 com queda de sinal nas sequências para supressão de gordura na RM(5,6,8,10). Estudos recentes destacam o uso da FDG PET/CT na avaliação da HLSIA, mostrando aumento na captação da FDG comparada com a captação da gordura subcutânea da parede torácica, fato este decorrente da presença de gordura marrom metabolicamente ativa na HLSIA. Este fato pode representar armadilha de imagem em potencial, levando ao diagnóstico incorreto de lesão infecciosa, inflamatória ou neoplásica. A correlação com TC e RM evita falsas interpretações(6,7,11). Por ser uma condição benigna, a maioria dos casos não requer tratamento, porém, raramente, pode ser indicada cirurgia quando há sintomas secundários a compressão de estruturas, como as veias cava e pulmonares(6,8). Dentre os diagnósticos diferenciais, o principal é o lipoma cardíaco, o qual apresenta cápsula e acomete a fossa oval. Outro diagnóstico diferencial importante é o lipossarcoma, porém, nestes estão presentes atipias e evolução rápida e agressiva. Concluindo, o diagnóstico de HLSIA deve ser considerado quando existe espessamento por infiltração gordurosa do SIA, maior que 2 cm, poupando a fossa oval, principalmente em pacientes idosos. REFERÊNCIAS 1. Assunção FB, Oliveira DCL, Souza VF, et al. Cardiac magnetic resonance imaging and computed tomography in ischemic cardiomyopathy: an update. Radiol Bras. 2016;49:2634. 2. Neves PO, Andrade J, Monção H. Coronary artery calcium score: current status. Radiol Bras. 2017;50:1829. 3. Assunção FB, Oliveira DCL, Santos AASMD, et al. Caseous calcification of the mitral annulus: computed tomography features. Radiol Bras. 2016;49:2734. 4. Rochitte CE. Cardiac MRI and CT: the eyes to visualize coronary arterial disease and their effect on the prognosis explained by the Schrödinger''s cat paradox. Radiol Bras. 2016;49(1):viiviii. 5. Kimura F, Matsuo Y, Nakajima T, et al. Myocardial fat at cardiac imaging: how can we differentiate pathologic from physiologic fatty infiltration? Radiographics. 2010;30:1587602. 6. Stojanovska J, Attili AK. AJR teaching file: fat-containing mass in the interatrial septum. AJR Am J Roentgenol. 2010;195(6 Suppl):S735. 7. Maurer AH, Burshteyn M, Adler LP, et al. How to differentiate benign versus malignant cardiac and paracardiac 18F FDG uptake at oncologic PET/CT. Radiographics. 2011;31:1287305. 8. Gottlieb I, Vávere A, Hannon K, et al. Hipertrofia lipídica do septo interatrial: relato de casos e revisão da literatura. Rev SOCERJ. 2007; 20:2357. 9. Motwani M, Kidambi A, Herzog BA, et al. MR imaging of cardiac tumors and masses: a review of methods and clinical applications. Radiology. 2013;268:2643. 10. Malik SB, Kwan D, Shah AB, et al. The right atrium: gateway to the heart anatomic and pathologic imaging findings. Radiographics. 2015;35:1431. 11. Buckley O, Madan R, Kwong R, et al. Cardiac masses, part 2: key imaging features for diagnosis and surgical planning. AJR Am J Roentgenol. 2011;197:W84251. 1. Universidade Federal Fluminense (UFF), Niterói, RJ, Brasil 2. Instituto Estadual do Cérebro Paulo Niemeyer, Rio de Janeiro, RJ, Brasil 3. Hospital Casa de Portugal/3D Diagnóstico por Imagem, Rio de Janeiro, RJ, Brasil 4. Universidade Federal do Rio de Janeiro (UFRJ), Rio de Janeiro, RJ, Brasil Endereço para correspondência: Dr. Renato Niemeyer de Freitas Ribeiro Universidade Federal Fluminense, Departamento de Cardiologia Rua Miguel de Frias, 9, Icaraí Niterói, RJ, Brasil, 24220-900 E-mail: renato.niemeyer@hotmail.com |
|
GN1© Copyright 2025 - All rights reserved to Colégio Brasileiro de Radiologia e Diagnóstico por Imagem
Av. Paulista, 37 - 7° andar - Conj. 71 - CEP 01311-902 - São Paulo - SP - Brazil - Phone: (11) 3372-4544 - Fax: (11) 3372-4554
Av. Paulista, 37 - 7° andar - Conj. 71 - CEP 01311-902 - São Paulo - SP - Brazil - Phone: (11) 3372-4544 - Fax: (11) 3372-4554