Radiologia Brasileira - Publicação Científica Oficial do Colégio Brasileiro de Radiologia
AMB - Associação Médica Brasileira CNA - Comissão Nacional de Acreditação
 Vol. 50 nº 5 - Set. / Out. of 2017
Vol. 50 nº 5 - Set. / Out. of 2017
|
CARTA AO EDITOR
|
|
|
|
|
Autho(rs): Tiago Medina Salata1; Lívia de Oliveira Antunes1; Bruno Niemeyer de Freitas Ribeiro2; Rafael Silveira Borges1; Diogo Goulart Corrêa1 |
|
|
Sr. Editor,
Mulher, 61 anos, em uso irregular de insulina para tratamento de diabetes tipo II, apresentando hemicoreia-hemibalismo de aparecimento súbito no braço e perna esquerdos há duas semanas. Os exames de sangue revelaram glicemia de 450 mg/dL, creatinina de 0,9 mg/dL, ureia de 38 mg/dL e o hemograma não apresentou alterações. A análise do líquor mostrou glicorraquia de 350 mg/dL. A ressonância magnética (RM) revelou lesão hiperintensa nas imagens ponderadas em T1 e levemente hiperintensa em T2, na região dos núcleos caudado e putâmen à direita, sem realce pelo meio de contraste, sem evidência de sangramento na sequência para suscetibilidade magnética e sem restrição à difusão (Figura 1). Tais achados de imagem, associados à história clinicolaboratorial, confirmaram o diagnóstico de hemicoreia-hemibalismo decorrente de hiperglicemia não cetótica. 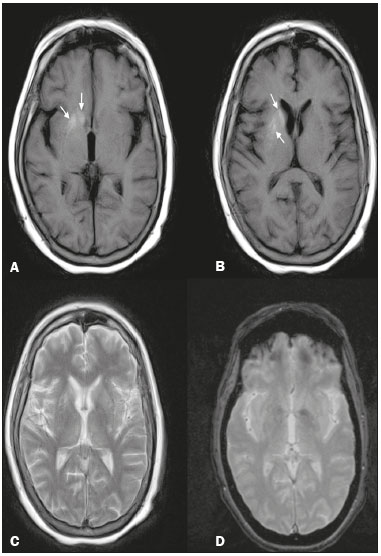 Figura 1. Ressonância magnética. A,B: Imagens ponderadas em T1 mostram lesão hiperintensa nos núcleos caudado e putâmen à direita (setas). C: Imagem ponderada em T2 mostra sinal levemente hiperintenso nas mesmas regiões. D: Imagem ponderada em T2* não revela deposição de sangue nessas regiões. Hiperglicemia não cetótica, também chamada de estriatopatia diabética, é uma causa rara de movimentos involuntários como manifestação primária de diabete mellitus e acomete principalmente pacientes idosos, com a tríade hemicoreia-hemibalismo, hiperglicemia e lesão hiperintensa nos núcleos da base nas imagens ponderadas em T1(1). Normalmente, os achados clínicos e de imagens são unilaterais, mas podem ser bilaterais em até 11,4% dos casos(2), e são potencialmente reversíveis e normalmente apresentam resolução em 2 a 12 meses após o tratamento da hiperglicemia(3,4). A fisiopatologia é desconhecida, porém, alterações metabólicas como deposição de proteínas, produtos de degradação de mielina, sangue ou cálcio ou outros minerais têm sido propostas e tendem a diminuir à medida que a glicose sérica é controlada(5). Outra teoria aceita é que a alteração de perfusão induzida pela hiperglicemia determina uma redução da atividade do ciclo de Krebs, induzindo a um metabolismo anaeróbio, fazendo com que o cérebro use fontes alternativas de energia e metabolize o neurotransmissor inibitório ácido gama-aminobutírico (GABA). Em um estado de hiperglicemia não cetótica, os níveis de GABA e acetato são reduzidos rapidamente, levando a uma diminuição da síntese de acetilcolina. Especula-se que a redução de acetilcolina e GABA nos núcleos da base pode provocar uma disfunção dessas estruturas, levando a movimentos involuntários, como coreia-hemibalismo(6,7). A RM é o exame de escolha para avaliação das doenças do sistema nervoso central(8-14). Os achados de imagem na RM na hemicoreia-hemibalismo por hiperglicemia não cetótica são caracterizados por hiperintensidade nas sequências pesadas em T1 e discreta hiperintensidade em T2, na região do núcleo caudado e núcleo lentiforme, sem realce pelo meio de contraste e sem restrição à difusão, geralmente unilateral, como em nosso caso, mas podendo ser bilateral(1,3,4). O diagnóstico diferencial de lesões hiperintensas nas sequências pesadas em T1 na região dos núcleos da base é amplo, podendo ser citadas como principais causas: encefalopatia hepática, exposição prolongada a manganês, nutrição parenteral prolongada, doença de Wilson, hemorragia intracerebral em fase subaguda, intoxicação exógena por monóxido de carbono e metanol, entre outras, sendo fundamental a correlação com dados clinicolaboratoriais para definição diagnóstica(1,4). Concluindo, apesar de a ocorrência de hemicoreia-hemibalismo como complicação de diabetes descontrolada ser incomum, o diagnóstico deve ser considerado quando os achados clínicos e de RM típicos são encontrados, evitando atrasos na instituição do tratamento adequado. REFERÊNCIAS 1. Bekiesinska-Figatowska M, Romaniuk-Doroszewska A, Banaszek M, et al. Lesions in basal ganglia in a patient with involuntary movements as a first sign of diabetes - case report and review of the literature. Pol J Radiol. 2010;75:61-4. 2. Krishna S, Sodhi KS, Saxena AK, et al. Hyperdense basal ganglia in nonketotic hyperglycemia. J Emerg Med. 2015;49:e57-8. 3. Bekiesinska-Figatowska M, Mierzewska H, Jurkiewicz E. Basal ganglia lesions in children and adults. Eur J Radiol. 2013;82:837-49. 4. Chokshi FH, Aygun N, Mullins ME. Imaging of acquired metabolic and toxic disorders of the basal ganglia. Semin Ultrasound CT MR. 2014; 35:75-84. 5. Hegde AN, Mohan S, Lath N, et al. Differential diagnosis for bilateral abnormalities of the basal ganglia and thalamus. Radiographics. 2011; 31:5-30. 6. Aggarwal A, Bansal N, Aggarwal R. Nonketotic hyperglycemia presenting as monoballism. J Emerg Med. 2016;50:e133-4. 7. Hansford BG, Albert D, Yang E. Classic neuroimaging findings of nonketotic hyperglycemia on computed tomography and magnetic resonance imaging with absence of typical movement disorder symptoms (hemichorea-hemiballism). J Radiol Case Rep. 2013;7:1-9. 8. Machado VS, Silva Junior NA, Queiroz LS, et al. Central nervous system involvement in sarcoidosis. Radiol Bras. 2015;48:334-5. 9. Dultra AHA, Noro F, Melo ASA, et al. Primary intercavernous lymphoma of the central nervous system. Radiol Bras. 2015;48:337-8. 10. Ribeiro BNF, Lima GA, Ventura N, et al. Chronic kernicterus: magnetic resonance imaging findings. Radiol Bras. 2016;49:407-8. 11. Langer FW, Suertegaray G, Santos D, et al. Hemichorea-hemiballism: the role of imaging in diagnosing an unusual disorder in patients with nonketotic hyperglycemia. Radiol Bras. 2016;49:267-8. 12. Ribeiro BNF, Salata TM, Borges RS, et al. Posterior reversible encephalopathy syndrome following immunoglobulin therapy in a patient with Miller-Fisher syndrome. Radiol Bras. 2016;49:58-9. 13. Campos LG, Trindade RAR, Faistauer A, et al. Rhombencephalitis: pictorial essay. Radiol Bras. 2016;49:329-36. 14. Georgeto SM, Zicarelli CAM, Gariba MA, et al. T1-weighted gradient-echo imaging, with and without inversion recovery, in the identification of anatomical structures on the lateral surface of the brain. Radiol Bras. 2016;49:382-8. 1. Hospital Casa de Portugal, Rio de Janeiro, RJ, Brasil 2. Instituto Estadual do Cérebro Paulo Niemeyer, Rio de Janeiro, RJ, Brasil Endereço para correspondência: Dr. Tiago Medina Salata Rua do Bispo, 72, Rio Comprido Rio de Janeiro. RJ, Brasil, 20261-064 E-mail: tiago_salata@yahoo.com.br |
|
GN1© Copyright 2025 - All rights reserved to Colégio Brasileiro de Radiologia e Diagnóstico por Imagem
Av. Paulista, 37 - 7° andar - Conj. 71 - CEP 01311-902 - São Paulo - SP - Brazil - Phone: (11) 3372-4544 - Fax: (11) 3372-4554
Av. Paulista, 37 - 7° andar - Conj. 71 - CEP 01311-902 - São Paulo - SP - Brazil - Phone: (11) 3372-4544 - Fax: (11) 3372-4554