Radiologia Brasileira - Publicação Científica Oficial do Colégio Brasileiro de Radiologia
AMB - Associação Médica Brasileira CNA - Comissão Nacional de Acreditação
 Vol. 50 nº 2 - Mar. / Abr. of 2017
Vol. 50 nº 2 - Mar. / Abr. of 2017
|
ARTIGOS ORIGINAIS
|
|
|
|
|
Autho(rs): Roberto Mogami1; João Luiz Pereira Vaz2; Yêdda de Fátima Barcelos Chagas3; Rodrigo Sperling Torezani4; André de Almeida Vieira4; Ana Célia Baptista Koifman1; Yasmin Baptista Barbosa5; Mirhelen Mendes de Abreu6 |
|
|
Descritores: Vírus chikungunya; Arbovírus; Ultrassonografia; Sinovite; Tenossinovite. |
|
|
Resumo: INTRODUÇÃO
A febre chikungunya é doença causada por um vírus da família Togaviridae, gênero Alphavirus e transmitida pelos mosquitos Aedes aegypti e Aedes albopictus(14). A maioria dos pacientes que se infecta apresenta sintomas e a doença evolui por três fases: uma fase aguda, que pode durar até 10 dias e se caracteriza por febre, dores, edemas periarticulares e, em vários casos, exantema(2); uma fase subaguda, que dura de 11 dias a 3 meses, em que predominam os sintomas reumatológicos caracterizados por sinovites de grandes e pequenas articulações e tenossinovites; e uma fase crônica, após 3 meses de evolução, em que persistem os sintomas inflamatórios em alguns sítios, mialgias e síndromes compressivas de nervos periféricos. Uma pequena porcentagem desses pacientes na fase crônica evolui para quadros que se assemelham à artrite reumatoide, e o principal achado em exames de imagem é a erosão articular(1,5,6). O vírus da febre chikungunya foi isolado, inicialmente, na Tanzânia em 1952. Após surtos esporádicos na África e Ásia ao longo das décadas de 60 e 70, a doença se tornou estatisticamente importante após uma epidemia no Quênia em 2004 e, principalmente, após a epidemia das Ilhas Reunião, no Oceano Índico, em 2005. Os primeiros casos no Hemisfério Ocidental ocorreram no Caribe a partir de 2013, de onde o vírus se espalhou para os países da América do Sul(5,711). No Brasil, casos autóctones foram, inicialmente, identificados em 2014 no Oiapoque, região norte do Brasil(12). Em 2015, foram registrados 23.431 casos prováveis de febre chikungunya no país, número que subiu para 236.287 casos em 2016 (aumento de 1.008,4%) até o mês de setembro. A região nordeste responde por 88,2% desses casos em 2016 e a região sudeste, 8,0%. O Rio de Janeiro contribui com 71,5% dos casos de febre chikungunya na região sudeste. O aumento do número de casos em 2016 (até o período de outubro-novembro) na cidade do Rio de Janeiro, em relação a 2015, é ainda mais absurdo: 33.270%. Esse número corresponde a 0,2% da população da cidade, segundo o censo de 2010. Se lembrarmos que nas Ilhas Reunião, 30% da população foram afetados pelo vírus, podemos ter uma ideia do tamanho do problema no Brasil(1315). Em consequência do surto no Rio de Janeiro, os serviços de emergência no primeiro semestre de 2016 ficaram lotados com pacientes que se queixavam de febre e artralgias intensas. A descrição das alterações ultrassonográficas desses quadros por Mogami et al.(8) foi pioneira ao fazer menção ao surto fluminense e ao relatar, em revista de radiologia, os achados característicos da doença pela ultrassonografia. O objetivo principal do presente trabalho é descrever as alterações relevantes no tornozelo que ocorrem em decorrência da infecção pelo vírus da febre chikungunya. MATERIAIS E MÉTODOS Este é um estudo transversal e observacional com 52 pacientes encaminhados ao Serviço de Radiologia do Hospital Universitário Pedro Ernesto nos meses de junho a outubro de 2016. A pesquisa foi aprovada pelo Comitê de Ética da Instituição. Todos os pacientes foram informados acerca do trabalho e assinaram termo de consentimento. Os critérios de inclusão foram pacientes adultos, maiores que 18 anos, de ambos os sexos, com história de febre súbita, dores articulares em múltiplos locais, com ou sem exantema, e diagnóstico laboratorial positivo para febre chikungunya (IgM/IgG). Pacientes com doenças reumáticas, como artrite reumatoide, espondiloartropatias, gota ou artrite séptica, foram excluídos, além de pacientes com sequelas de fraturas. Os exames de ultrassonografia de tornozelos foram realizados por um radiologista com mais de 20 anos de experiência no método. Além da rotina de investigação do tornozelo, o mesmo examinador avaliou o estado da musculatura sural para identificação de possíveis sinais sugestivos de miosite. Um total de 104 exames foi realizado em equipamento modelo Aplio XG (Toshiba Medical Systems; Otawara, Japão), com transdutor linear multifrequencial de 1418 MHz em modo B e com Doppler de amplitude. RESULTADOS Na casuística, 6 pacientes eram do sexo masculino (11,5%) e 46 eram do sexo feminino (88,5%). A média das idades foi 58,4 anos. A cidade foi dividida em quatro regiões principais, de acordo com o domicílio de origem dos doentes: 32 residiam na zona norte, subúrbio da cidade (61,5%), 10 na zona oeste (19,2%), 9 na região metropolitana, periferia do Rio de Janeiro (17,3%), e 1 na zona sul, região mais elitizada da cidade (1,9%). Os sintomas mais frequentes, em ordem decrescente, foram: 52 com dores articulares (100%), 46 com febre (88,5%), 37 com alterações cutâneas (71,2%), 31 com prurido (59,6%), 22 com parestesias (42,3%) e 4 com linfonodomegalias (7,7%). Em relação ao tratamento em curso na época em que os exames foram realizados, 24 pacientes faziam uso de esteroides (46,2%), 14 estavam sem nenhuma medicação (26,9%), 6 faziam uso de anti-inflamatórios (11,5%) e 5 pacientes estavam sendo tratados com uma combinação de esteroides e imunossupressores (9,6%). Na média, os exames de ultrassonografia foram realizados 4,1 meses após o início da doença, o que correspondeu à fase crônica de evolução. As alterações ultrassonográficas mais frequentes nos tornozelos, em ordem decrescente, foram: derrame articular (Figura 1) em 36 pacientes (69,2%), tenossinovites (Figura 2) em 31 (59,6%), celulite em 24 (46,2%), espessamento da gordura de Kager (Figura 3) em 14 (29,9%), miosite (sóleo e/ou flexor longo do hálux) (Figura 4) em 9 (17,3%), bursite retrocalcânea (Figura 5) em 3 (5,8%), roturas tendíneas (Figura 6) em 2 (3,8%) e hiperfluxo vascular pelo Doppler de amplitude em 2 pacientes (3,8%). 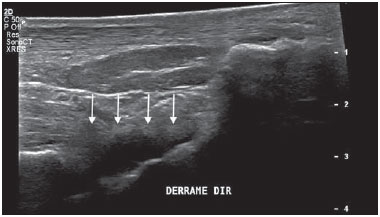 Figura 1. Imagem longitudinal sagital do recesso tibiotarsal, obtida com transdutor linear de 14 MHz, mostra áreas hipoecoicas no interior, o que caracteriza derrame (setas). 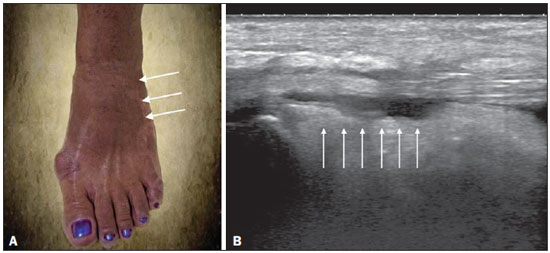 Figura 2. A: Foto da região dorsal do pé esquerdo, em que se nota abaulamento da porção anterolateral (setas). B: Em correspondência com a alteração presente no exame físico, o corte sagital da ultrassonografia do tendão extensor longo dos dedos, obtido com transdutor linear de 14 MHz, mostra distensão da bainha peritendínea por coleção anecoica (setas), o que caracteriza tenossinovite. 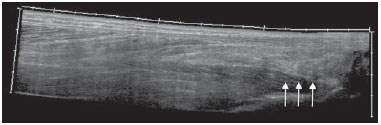 Figura 3. Corte ultrassonográfico sagital da região sural posterior, obtido com transdutor linear de 14 MHz, mostra espessamento e aumento da ecogenicidade da gordura de Kager (setas). 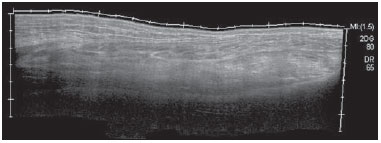 Figura 4. Visão panorâmica sagital da panturrilha, obtida com varredura por meio de transdutor linear de 14 MHz, mostra hiperecogenicidade difusa dos músculos sóleo e flexor longo do hálux por miosite. 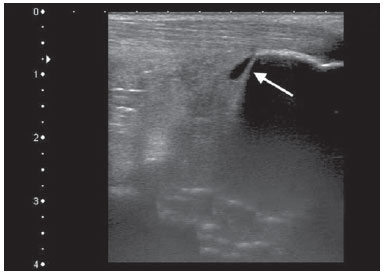 Figura 5. Imagem sagital inferior da panturrilha, obtida com transdutor linear de 14 MHz, mostra coleção anecoica na projeção da bolsa retrocalcânea (seta), o que caracteriza bursite. 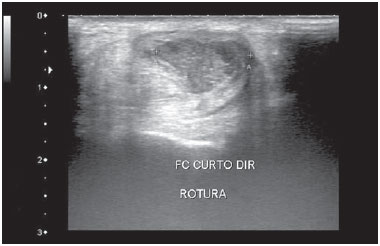 Figura 6. Imagem transversa do tendão fibular curto, obtida com transdutor linear de 14 MHz, mostra extensa área hipoecoica na região posterior, o que caracteriza rotura parcial. Em relação ao derrame articular, as coleções se localizavam no recesso tibiotarsal (Figura 1) em 27 pacientes (51,9%) e no recesso intertarsal proximal em 23 (44,2%). Os sinais de tenossinovite foram encontrados principalmente na bainha tibial posterior em 19 pacientes (36,5%) e na bainha dos fibulares em 17 pacientes (32,7%). Destaca-se, na presente casuística, a identificação de lesões preexistentes do tendão do calcâneo: calcificações em 33 pacientes (63,5%) e tendinopatia em 6 pacientes (11,5%). Em 13 pacientes (25%) não foram encontradas lesões tendíneas aquilianas. DISCUSSÃO Os exames de imagem no estudo das infecções, especialmente as de incidência regional, têm sido motivo de várias publicações na literatura radiológica nacional(1624). No presente trabalho são apresentados os resultados parciais de um estudo maior, em andamento, na Universidade do Estado do Rio de Janeiro, que investiga o comprometimento musculoesquelético de membros superiores e inferiores num grupo de indivíduos com diagnóstico de febre chikungunya. A população estudada se mostrava, evolutivamente, nas fases subaguda e crônica da doença, como pode ser constatado pelo tempo médio decorrido entre o diagnóstico e a realização dos exames (4,1 meses). Nota-se um predomínio marcante do sexo feminino e de indivíduos numa faixa etária mais elevada (58,4 anos), achados que são semelhantes aos de um estudo realizado na Martinica (território francês)(25) e do clássico trabalho sobre a epidemia de febre chikungunya nas Ilhas Reunião(5), mas bastante diferentes das casuísticas indiana(26), italiana(27), do Sri Lanka(3) e colombiana(28). É importante citar que, na literatura, pacientes acima de 35 anos com febre chikungunya têm um risco aumentado de desenvolver atralgias crônicas(29,30). A localização geográfica preferencial dos casos estudados na zona norte da cidade, subúrbio do Rio de Janeiro, pode ser indicativa da vulnerabilidade dessa região à proliferação do mosquito, mas pode também ser um viés, em razão da localização do hospital em que se situou o estudo. No entanto, dados da Secretaria Municipal de Saúde do Rio de Janeiro mostram que, durante o mês de abril de 2016, quando houve o maior número mensal de casos da doença 5.109 ocorrências , os bairros mais afetados se localizavam nas zonas norte e oeste(31). Dos sintomas relatados, todos são descritos na literatura como associados às infecções por arbovírus, principalmente as dores articulares crônicas, no caso de chikungunya(8,26,32). A heterogeneidade de condutas em relação ao tratamento dos pacientes reflete o desconhecimento sobre a doença e o próprio fluxo de encaminhamento dos pacientes que provinham de ambulatórios gerais ou especializados, assim como de serviços de emergência do Rio de Janeiro. Em acordo com a literatura, na nossa casuística, o acometimento dos tornozelos se deu de forma simétrica(29,33,34). As duas principais alterações foram os derrames e as tenossinovites, como ocorre em outros segmentos anatômicos e descrito na literatura(8,35,36). Na fase crônica da doença, estas coleções não são muito volumosas, mas as tenossinovites, principalmente, respondem bem ao tratamento anti-inflamatório. Em exames de controle que temos realizado, observamos que a regressão do quadro inflamatório pode ocorrer, com persistência de focos residuais assimétricos intra- ou extra-articulares, e que merecem estudos adicionais para identificação de possíveis erosões articulares associadas. Miosite isolada ou associada a celulite foi um achado presente em 17,3% dos pacientes. Os grupos musculares mais acometidos em nossa casuística foram o sóleo e o flexor longo do hálux. Frequentemente havia acometimento associado da gordura de Kager, que se apresentava hiperecoica nestas ocasiões e formava um aspecto ecográfico contínuo e semelhante ao da miosite do sóleo. O comprometimento é quase sempre simétrico e no caso dos membros inferiores está associado a queixas de fadiga e desconforto nas regiões surais. Acreditamos que a posição encurvada, que originou o nome "chikungunya" no dialeto makonde da Tanzânia(37), tem relação não somente com a artrite dos tornozelos, mas também com a miosite generalizada da musculatura sural. Em exames de controle já realizados, temos verificado que a miosite pode persistir por longo tempo, mesmo quando o paciente responde bem à terapia com esteroides e imunossupressores. Como agentes virais podem causar miopatias inflamatórias idiopáticas, talvez o vírus da febre chikungunya também possa desencadear esse tipo de condição a longo prazo(38). O comprometimento inflamatório secundário a infecções é assunto que vem sendo discutido há tempos, e o vírus da febre chikungunya tem destaque nestas condições(34). Assim como ocorre nas mãos e punhos, e com uma frequência ainda menor (Mogami, dados não publicados), o Doppler de amplitude apresentou pouca positividade no tornozelo (3,8%). Acreditamos que a maior utilidade deste recurso seja no acompanhamento evolutivo dos pacientes; o hiperfluxo vascular em exames de seguimento pode sinalizar focos inflamatórios persistentes e chamar a atenção do médico assistente para a possibilidade de reumatismo inflamatório crônico(25,28). Esta hipótese necessita de outros estudos para ser confirmada. Uma comorbidade musculoesquelética encontrada em alta frequência nos pacientes com febre chikungunya foi o comprometimento do tendão do calcâneo, seja por entesófitos (63,5%) ou por tendinopatia (11,5%). Na prática isto se traduz por amplificação de sintomas previamente existentes à infecção pelo vírus. São comuns queixas de intensificação de dores durante a fase crônica da doença. Chen et al. afirmaram que doenças musculoesqueléticas degenerativas preexistentes poderiam prolongar os sintomas de artralgia, e por isso essas comorbidades têm relevância clínica para o acompanhamento desses doentes(10). Após a explosão de casos de febre chikungunya em 2016(8,13,31), as expectativas das autoridades sanitárias é de que a doença retorne com mais força no verão de 2017. Apesar das limitações deste estudo, a caracterização e quantificação pioneira das lesões de tornozelo por meio da ultrassonografia foram importantes para ressaltar o papel do método no diagnóstico destas complicações. Outros estudos são necessários para avaliar o papel do exame no acompanhamento evolutivo e possível apontamento dos casos que podem evoluir para reumatismo inflamatório crônico ou até mesmo artrite reumatoide secundária(39). Esta necessidade de estudos evolutivos dos casos de artralgia crônica com potencial para artrite inflamatória tem sido citada por outros autores(10). Em resumo, pode-se afirmar que o surto epidêmico ocorrido no Rio de Janeiro entre 2015 e 2016 se caracterizou pelo acometimento predominante de mulheres numa faixa etária mais elevada, moradoras do subúrbio e sem um tratamento definido para a doença, a maioria em uso de esteroides. Os achados predominantes em nossa casuística foram de derrames e tenossinovites, principalmente fibulares e tibial posterior. A comorbidade musculoesquelética mais comum foi o acometimento do tendão do calcâneo. O Doppler mostrou-se pouco útil na identificação de áreas com inflamação sinovial. Agradecimento Esta pesquisa recebeu suporte da Fundação Carlos Chagas Filho de Amparo à Pesquisa do Estado do Rio de Janeiro (Faperj), por intermédio do projeto E-26/110.255/2014. REFERÊNCIAS 1. Imai K, Nakayama E, Maeda T, et al. Chikungunya fever in Japan imported from the Caribbean Islands. Jpn J Infect Dis. 2016;69: 1513. 2. Horcada ML, Díaz-Calderón C, Garrido L. Chikungunya fever. Rheumatic manifestations of an emerging disease in Europe. Reumatol Clin. 2015;11:1614. 3. Kularatne SA, Weerasinghe SC, Gihan C, et al. Epidemiology, clinical manifestations, and long-term outcomes of a major outbreak of chikungunya in a hamlet in Sri Lanka, in 2007: a longitudinal cohort study. J Trop Med. 2012;2012:639178. 4. Weaver SC, Lecuit M. Chikungunya virus and the global spread of a mosquito-borne disease. N Engl J Med. 2015;372:12319. 5. Javelle E, Gautret P, Simon F. Chikungunya, the emerging migratory rheumatism. Lancet Infect Dis. 2015;15:50910. 6. Parola P, Simon F, Oliver M. Tenosynovitis and vascular disorders associated with chikungunya virus-related rheumatism. Clin Infect Dis. 2007;45:8012. 7. Alfaro-Toloza P, Clouet-Huerta DE, Rodríguez-Morales AJ. Chikungunya, the emerging migratory rheumatism. Lancet Infect Dis. 2015;15:5102. 8. Mogami R, de Almeida Vieira A, Junqueira Filho EA, et al. Chikungunya fever outbreak in Rio de Janeiro, Brazil: ultrasonographic aspects of musculoskeletal complications. J Clin Ultrasound. 2017; 45:434. 9. Olowokure B, Francis L, Polson-Edwards K, et al. The Caribbean response to chikungunya. Lancet Infect Dis. 2014;14:103940. 10. Chen W, Foo SS, Sims NA, et al. Arthritogenic alphaviruses: new insights into arthritis and bone pathology. Trends Microbiol. 2015; 23:3543. 11. McSweegan E, Weaver SC, Lecuit M, et al. The global virus network: challenging chikungunya. Antiviral Res. 2015;120:14752. 12. Honório NA, Câmara DC, Calvet GA, et al. Chikungunya: an arbovirus infection in the process of establishment and expansion in Brazil. Cad Saude Publica. 2015;31:9068. 13. Brasil. Ministério da Saúde. Secretaria de Vigilância em Saúde. Monitoramento dos casos de dengue, febre de chikungunya e febre pelo vírus Zika até a semana epidemiológica 37, 2016. Boletim Epidemiológico. 2016;47(34). 14. Pierrotti L. Zika, chikungunya e dengue: epidemiologia no Brasil e no Mundo. Inovar Saúde. 2016;2:328. 15. Collucci C. Brazil sees sharp rise in chikungunya cases. BMJ. 2016; 354:i4560. 16. Vermelho MB, Correia AS, Michailowsky TC, et al. Abdominal alterations in disseminated paracoccidioidomycosis: computed tomography findings. Radiol Bras. 2015;48:815. 17. Gava P, Melo AS, Marchiori E, et al. Intestinal and appendiceal paracoccidioidomycosis. Radiol Bras. 2015;48:1267. 18. Rocha EL, Pedrassa BC, Bormann RL, et al. Abdominal tuberculosis: a radiological review with emphasis on computed tomography and magnetic resonance imaging findings. Radiol Bras. 2015;48: 18191. 19. Lima Júnior FVA, Savarese LG, Monsignore LM, et al. Computed tomography findings of paracoccidiodomycosis in musculoskeletal system. Radiol Bras. 2015;48:16. 20. Lachi T, Nakayama M. Radiological findings of pulmonary tuberculosis in indigenous patients in Dourados, MS, Brazil. Radiol Bras. 2015;48:27581. 21. Abud TG, Abud LG, Vilar VS, et al. Radiological findings in megaesophagus secondary to Chagas disease: chest X-ray and esophagogram. Radiol Bras. 2016;49:35862. 22. Marchiori E. Chagas disease: a tropical infection of interest to the radiologist. Radiol Bras. 2016;49(6):vvi. 23. Queiroz RM, Gomes MP, Valentin MVN. Pulmonary paracoccidioidomycosis showing reversed halo sign with nodular/coarse contour. Radiol Bras. 2016;49:5960. 24. Barbosa BC, Amorim VB, Ribeiro LFM, et al. Tuberculosis: tracheal involvement. Radiol Bras. 2016;49:4101. 25. Blettery M, Brunier L, Polomat K, et al. Brief report: management of chronic post-chikungunya rheumatic disease: the Martinican experience. Arthritis Rheumatol. 2016;68:281724. 26. Manimunda SP, Vijayachari P, Uppoor R, et al. Clinical progression of chikungunya fever during acute and chronic arthritic stages and the changes in joint morphology as revealed by imaging. Trans R Soc Trop Med Hyg. 2010;104:3929. 27. Liumbruno GM, Calteri D, Petropulacos K, et al. The chikungunya epidemic in Italy and its repercussion on the blood system. Blood Transfus. 2008;6:199210. 28. Rodríguez-Morales AJ, Anaya JM. Impacto de las arbovirosis artritogénicas emergentes en Colombia y América Latina. Rev Colomb Reumatol. 2016;23:1457. 29. Schilte C, Staikowsky F, Couderc T, et al. Chikungunya virusassociated long-term arthralgia: a 36-month prospective longitudinal study. PLoS Negl Trop Dis. 2013;7:e2137. 30. Schwartz KL, Giga A, Boggild AK. Chikungunya fever in Canada: fever and polyarthritis in a returned traveller. CMAJ. 2014;186:7724. 31. Secretaria Municipal de Saúde do Rio de Janeiro. Número de casos de chikungunya por mês, áreas de planejamento, regiões administrativas e bairros. Município do Rio de Janeiro, 2016. [Cited 2016 Aug 20]. Available from: http://www.rio.rj.gov.br/dlstatic/10112/6728534/4184408/CHIKVMES2016.pdf. 32. Rodriguez-Morales AJ, Cardona-Ospina JA, Villamil-Gómez WE. Chikungunya, a global threat currently circulating in Latin America. In: Rodriguez-Morales AJ, editor. Current topics in chikungunya. 1st ed. Rijeka, Croatia: Intech; 2016. 33. Hassan R, Rahman MM, Moniruzzaman M, et al. Chikungunya an emerging infection in Bangladesh: a case series. J Med Case Rep. 2014;8:67. 34. Khasnis AA, Schoen RT, Calabrese LH. Emerging viral infections in rheumatic diseases. Semin Arthritis Rheum. 2011;41:23646. 35. Thiberville SD, Moyen N, Dupuis-Maguiraga L, et al. Chikungunya fever: epidemiology, clinical syndrome, pathogenesis and therapy. Antiviral Res. 2013;99:34570. 36. Chopra A, Anuradha V, Lagoo-Joshi V, et al. Chikungunya virus aches and pains: an emerging challenge. Arthritis Rheum. 2008;58: 29212. 37. Morens DM, Fauci AS. Chikungunya at the doordéjà vu all over again? N Engl J Med. 2014;371:8857. 38. Gan L, Miller FW. State of the art: what we know about infectious agents and myositis. Curr Opin Rheumatol. 2011;23:58594. 39. Rodriguez-Morales AJ, Cardona-Ospina JA, Villamil-Gómez W, et al. How many patients with post-chikungunya chronic inflammatory rheumatism can we expect in the new endemic areas of Latin America? Rheumatol Int. 2015;35:20914. 1. Doutores, Professores Adjuntos de Radiologia da Faculdade de Ciências Médicas da Universidade do Estado do Rio de Janeiro (UERJ), Rio de Janeiro, RJ, Brasil 2. Doutor, Professor Adjunto de Reumatologia da Universidade Federal do Estado do Rio de Janeiro (Unirio), Rio de Janeiro, RJ, Brasil 3. Médica Residente de Reumatologia do Hospital Universitário Gafrée e Guinle (HUGG) da Universidade Federal do Estado do Rio de Janeiro (Unirio), Rio de Janeiro, RJ, Brasil 4. Médicos Residentes de Radiologia do Hospital Universitário Pedro Ernesto (HUPE) da Universidade do Estado do Rio de Janeiro (UERJ), Rio de Janeiro, RJ, Brasil 5. Estudante do Curso de Graduação em Medicina da Universidade do Estado do Rio de Janeiro (UERJ), Rio de Janeiro, RJ, Brasil 6. Doutora, Professora Adjunta de Reumatologia da Universidade Federal do Rio de Janeiro (UFRJ), Rio de Janeiro, RJ, Brasil Endereço para correspondência: Dr. Roberto Mogami Serviço de Radiologia e Diagnóstico por Imagem HUPE/UERJ Avenida 28 de Setembro, 77, Vila Isabel Rio de Janeiro, RJ, Brasil, 20551-030 E-mail: ioga@pobox.com Recebido para publicação em 4/12/2016. Aceito, após revisão, em 5/1/2017. Trabalho realizado no Serviço de Radiologia e Diagnóstico por Imagem do Hospital Universitário Pedro Ernesto (HUPE) da Universidade do Estado do Rio de Janeiro (UERJ), Rio de Janeiro, RJ, Brasil. |
|
Av. Paulista, 37 - 7° andar - Conj. 71 - CEP 01311-902 - São Paulo - SP - Brazil - Phone: (11) 3372-4544 - Fax: (11) 3372-4554