RESUMO
OBJETIVO: Gerar modelos físicos de fetos utilizando imagens obtidas por ultrassonografia tridimensional (US3D), ressonância magnética (RM) e, em alguns casos, tomografia computadorizada (TC), para orientar a técnica de adição de camadas.
MATERIAIS E MÉTODOS: Foram usadas imagens obtidas de 31 gestantes, incluindo 5 casos de gestação gemelar. Os exames foram realizados usando US3D, RM e em alguns casos TC, e os arquivos foram exportados para uma estação de trabalho em formato DICOM. Um único observador realizou o processo de segmentação manual usando tela de alta resolução. Um software que converte imagens médicas em modelos numéricos foi utilizado para construir modelos virtuais 3D, que foram fisicamente materializados.
RESULTADOS: Os modelos virtuais e físicos baseados na US3D, RM e TC realizados separadamente ou em conjunto foram concluídos com sucesso. A aparência pós-natal do feto abortado ou do recém-nascido se assemelhou muito com os modelos físicos, particularmente nos casos de malformações.
CONCLUSÃO: O uso da US3D, RM e TC pode ajudar para melhor compreensão das características físicas do feto. Essas técnicas podem ser usadas com fins didáticos para auxiliar na abordagem multidisciplinar e na melhor compreensão dos pais. As imagens podem ser segmentadas e aplicadas separadamente ou combinadas para construir modelos virtuais 3D e físicos.
Palavras-chave:
Feto; Medicina fetal; Tecnologia tridimensional; Ultrassonografia; Ressonância magnética; Tomografia computadorizada.
ABSTRACT
OBJECTIVE: To generate physical models of fetuses from images obtained with three-dimensional ultrasound (3D-US), magnetic resonance imaging (MRI), and, occasionally, computed tomography (CT), in order to guide additive manufacturing technology.
MATERIALS AND METHODS: We used 3D-US images of 31 pregnant women, including 5 who were carrying twins. If abnormalities were detected by 3D-US, both MRI and in some cases CT scans were then immediately performed. The images were then exported to a workstation in DICOM format. A single observer performed slice-by-slice manual segmentation using a digital high resolution screen. Virtual 3D models were obtained from software that converts medical images into numerical models. Those models were then generated in physical form through the use of additive manufacturing techniques.
RESULTS: Physical models based upon 3D-US, MRI, and CT images were successfully generated. The postnatal appearance of either the aborted fetus or the neonate closely resembled the physical models, particularly in cases of malformations.
CONCLUSION: The combined use of 3D-US, MRI, and CT could help improve our understanding of fetal anatomy. These three screening modalities can be used for educational purposes and as tools to enable parents to visualize their unborn baby. The images can be segmented and then applied, separately or jointly, in order to construct virtual and physical 3D models.
Keywords:
Fetus; Fetal medicine; Three-dimensional technique; Ultrasound; Magnetic resonance imaging; Computed tomography.
INTRODUÇÃO
O crescente desenvolvimento tecnológico na obtenção e visualização de imagens por meio de técnicas não invasivas trouxe grande avanço na medicina, especialmente no diagnóstico de anomalias fetais(1,2). Em geral, duas modalidades de exames são usadas para obter imagens da cavidade uterina durante a gravidez: a ultrassonografia (US) e a ressonância magnética (RM)(1–3). A tomografia computadorizada (TC) também oferece imagens detalhadas do feto, especialmente do seu esqueleto, a partir da 30ª semana de gravidez, mas seu emprego é restrito devido à presença de radiações ionizantes(4).
A modelagem tridimensional (3D) virtual teve grande impulso nos últimos anos, em função do alto desempenho dos softwares aplicados nas áreas de engenharia, arquitetura e design. Ela vem tomando uma forma cada vez mais amigável, facilitando a visualização das imagens 3D(5–7).
O objetivo deste trabalho foi desenvolver modelos 3D virtuais de fetos durante a gestação, utilizando imagens de US, RM e TC, isoladas ou em conjunto.
MATERIAIS E MÉTODOS
Este estudo avaliou 31 gestantes no período de janeiro de 2008 a dezembro de 2014. O estudo foi aprovado pelo Comitê de Ética em Pesquisa do Instituto Fernandes Figueira (IFF/Fiocruz). Todas as pacientes envolvidas foram submetidas a US3D isoladamente ou US3D associada à RM, com intervalo de até um dia entre os exames (Tabela 1). A RM foi utilizada em associação com a US3D em todos os casos de suspeita de malformação fetal vista previamente pela US. Toda a reconstrução 3D para prototipagem foi realizada no Instituto Nacional de Tecnologia e no Núcleo de Experimentação Tridimensional da Pontifícia Universidade Católica do Rio de Janeiro.

Os critérios de inclusão foram: gestação única ou múltipla com idade gestacional estabelecida por US realizada até 16 semanas de gestação e/ou data precisa do último período menstrual em mulheres com história de ciclos regulares; fetos com suspeita de anormalidade ou malformados identificados previamente pela US.
Todas as pacientes tinham idade mínima de 18 anos e foram avaliadas entre 22 e 37 semanas de gestação, sendo algumas reagendadas para um segundo exame, de acordo com a necessidade de cada caso. Os exames de US e RM foram realizados e acompanhados por dois profissionais – um especialista em ginecologia, obstetrícia e medicina fetal e outro especialista em radiologia.
Os equipamentos usados para as avaliações ultrassonográficas foram o Voluson 730 e o Voluson E8 (GE Medical Systems Kretztechnik; Zipf, Áustria), com transdutor transvaginal e transabdominal de 4–8 MHz. O exame de RM foi realizado em aparelhos de 1,5 T Magnetom Avanto e Aera (Siemens Healthcare; Erlangen, Alemanha). As pacientes foram posicionadas em decúbito dorsal ou decúbito lateral esquerdo, de acordo com a posição em que se sentiram mais confortáveis, iniciando-se a introdução no aparelho pelos pés, no intuito de diminuir a sensação de claustrofobia. Foi utilizada bobina de superfície posicionada sobre o abdome da gestante, com o seguinte protocolo: sequências pesadas em T2 HASTE (tempo de repetição [TR]: 140 ms; tempo de eco [TE]: 140 ms;
field of view [FOV]: 300–200 mm;
gap: 0; matriz: 256 × 256 mm; cortes de 4 mm de espessura; tempo de aquisição: 18 s; 40 cortes nos planos axial, coronal e sagital do feto) e TrueFISP 3D volumétrico (TR: 3,02 ms; TE: 1,34 ms; FOV: 340 mm; matriz: 256 × 90–256 mm; cortes entre 1,0 e 1,6 mm; tempo de aquisição: 26 s; 96 a 196 cortes, dando preferência ao plano sagital do feto). O tempo total de exame não excedeu 40 minutos
(1–3).
Em cinco casos de malformação do esqueleto fetal foram utilizados arquivos de TCs realizadas após a 30ª semana de gestação (Tabela 1). Estes arquivos foram obtidos por tomógrafo
multislice de 64 canais Brilliance (Philips; Solingen, Alemanha) com os seguintes parâmetros: 40 mAs, 120 kV, 64 cortes por rotação, 0.75
pitch e 0,75 mm de espessura de corte. Isto corresponde a dose média de radiação de 3,12 mGy, produto dose-comprimento de 160,3 mGy.cm e dose efetiva de 2,40 mSv
(4,5).
Para a construção do modelo físico com base na US3D, RM e TC, o primeiro passo foi criar o modelo virtual 3D do feto. As imagens geradas por US3D, RM e TC foram exportadas para uma estação de trabalho, no formato DICOM. Em seguida, a segmentação foi feita por um técnico de modelagem em 3D e supervisionada pelo médico responsável. Os fetos foram reconstruídos utilizando os cortes finos que, somados, geravam uma superfície 3D, sendo a informação dos tecidos moles obtida pela US3D e/ou RM, e quando utilizada a TC, o esqueleto apenas. A segmentação pela US3D foi realizada em todos os casos (Tabelas 1, 2 e 3). Foi utilizado o
software Mimics v. 12 (Materialize: Leuven, Bélgica) para segmentação das imagens médicas, gerando ao final um modelo virtual nos formatos
wavefront object e standard triangular language, este último direcionado para impressão 3D.
O processo de reconstrução de fetos em modelos físicos utilizando imagens de US, RM e TC gerou patente com número de registro PI08090521.
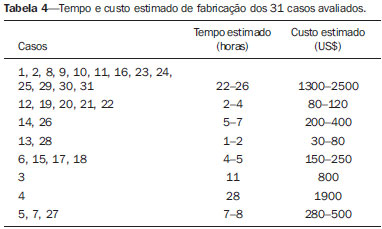
RESULTADOSOs modelos físicos gerados foram considerados satisfatórios em todos os casos (Figuras 1, 2, 3 e 4). O tempo médio de impressão e o custo para cada processo estão resumidos na Tabela 4.
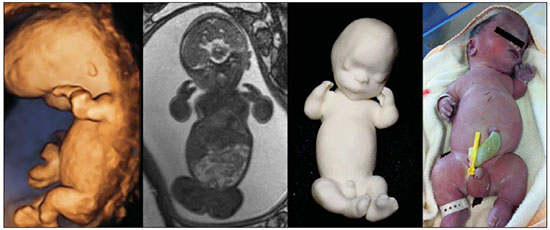 Figura 1. Caso 26
Figura 1. Caso 26. Feto portador de nanismo tanatofórico. US, RM, modelo físico e natimorto.
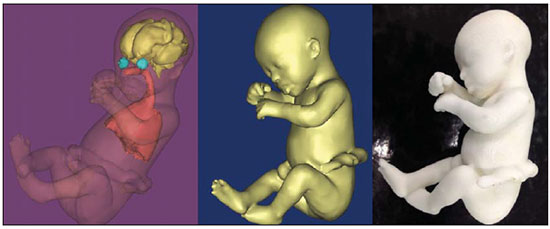 Figura 2. Caso 18
Figura 2. Caso 18. Feto portador de trissomia 21. Modelo virtual e físico do corpo inteiro obtido por RM.
 Figura 3. Caso 29
Figura 3. Caso 29. Feto portador de agenesia radial esquerda e onfalocele. Modelo virtual e físico do corpo inteiro obtido por RM.
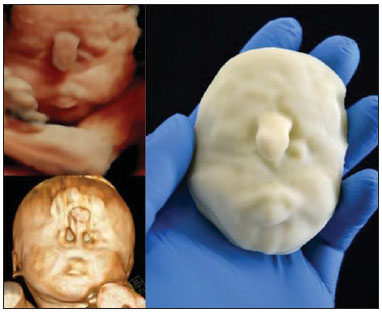 Figura 4A. Caso 16
Figura 4A. Caso 16. Feto de 25 semanas, portador de holoprosencefalia alobar com probóscide. Face obtida por US3D, RM e modelo físico com base na US.
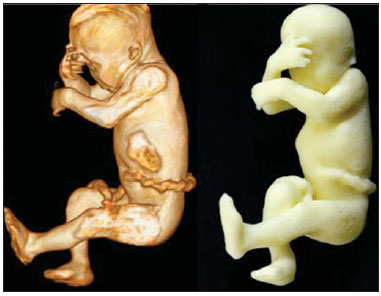 Figura 4B.
Figura 4B. Reconstrução 3D do corpo inteiro com base na RM e modelo físico.
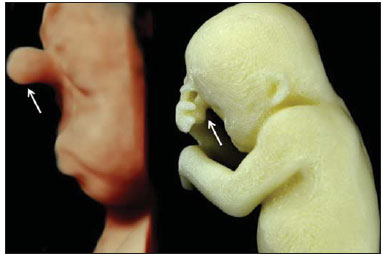 Figura 4C.
Figura 4C. Perfil fetal obtido por US3D e modelo físico. Notar a presença da probóscide (setas).
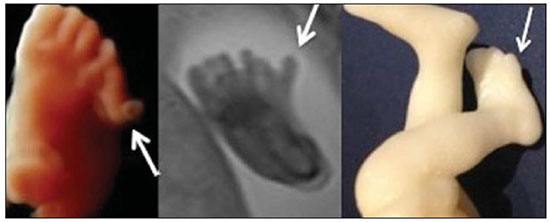 Figura 4D.
Figura 4D. Polidactilia no pé identificada pela US3D, RM e modelo físico.
A TC forneceu imagens de alta resolução do esqueleto fetal. As imagens de RM mostraram alto contraste entre os órgãos e superfície externa. Os modelos físicos obtidos pela US3D deram excelentes resultados nas impressões da face, orelhas, mãos e pés.
Uma combinação de métodos foi desenvolvida com sucesso para a construção de modelos físicos. Em um caso de feto de 25 semanas portador de holoprosencefalia alobar com probóscide (caso 16 – Tabela 3), que fora avaliado pela US3D e RM no mesmo dia, o corpo foi modelado com base no arquivo de RM e o rosto e as extremidades foram modelados com base na US3D. Neste caso, a US3D foi fundamental para a avaliação das extremidades e da face (Figura 4).
DISCUSSÃOA técnica de adição de materiais permite a conversão de um modelo virtual 3D para um modelo físico em um processo rápido, fácil e de dimensões precisas. O processo de construção transfere um arquivo de dados 3D, resultante da sobreposição das camadas individualmente segmentadas, para um equipamento de manufatura aditiva ou impressão 3D, que constrói modelos físicos por meio da sobreposição de finas camadas de matérias primas
(6–9).
O principal resultado apresentado neste estudo foi a possibilidade de criar modelos 3D virtuais e físicos com base na US3D e na RM, isoladamente ou em conjunto, nos casos de enfermidades mais complexas em que houve dificuldade no diagnóstico isolado por US. O uso de cinco casos em que foi realizada também a TC se justifica, porque todo o desenvolvimento desta técnica de reconstrução 3D do feto em modelo físico passou na primeira fase do seu desenvolvimento pela TC. Somente em seguida foi dominada a técnica com base na RM e US, respectivamente
(10,11).
Werner et al.
(10) introduziram o uso de modelos físicos na pesquisa de doenças fetais, uma área em que são escassos os estudos em modelagem digital (3D)
(11–14). Os resultados sugerem uma possibilidade nova na interação entre os pais e o feto durante o acompanhamento pré-natal, recriando fisicamente o interior do útero durante a gravidez, demonstrando o tamanho real do feto, assim como sua anatomia.
Uma das principais preocupações deste estudo foi obter imagens de alta qualidade que pudessem ser manipuladas com
software 3D, sem perda de precisão. Os movimentos fetais durante a aquisição de imagens foram uma das principais dificuldades, principalmente na avaliação por RM. Este problema é menor na US, pois a imagem é adquirida em tempo real, podendo ser congelada durante o movimento. No entanto, a menor resolução de contraste na US provocou, em alguns casos, dificuldades nos limites da escala de cinza. A qualidade do processo está diretamente associada à precisão dos dados matemáticos que serão utilizados para gerar o modelo físico. As imagens são adquiridas por fatias que são sobrepostas para a realização do modelo.
Os modelos físicos têm impacto no planejamento de intervenções médicas
(15,16). Podem também ser utilizados em medicina fetal para fins didáticos
(11,14,17,18). O ato de combinar imagens utilizando diferentes métodos (US e RM) pode resultar em melhor compreensão dos pais e de uma equipe médica multidisciplinar, na avaliação de determinados tipos de enfermidades
(11–14).
Estudos utilizando US e modelos 3D já foram realizados. Blaas et al.
(19) calcularam o volume de embriões e fetos no primeiro trimestre da gestação, transformando a área do embrião/feto obtida em um modelo virtual. Outro estudo foi desenvolvido por Nelson et al.
(20), que converteram dados 3D com base na US para um conjunto de polígonos representando uma superfície que poderia ser transferida para diversos tipos de equipamentos de prototipagem rápida, criando um objeto sólido 3D. Esta foi considerada a primeira tentativa de transformar dados da US3D em modelos físicos. No presente estudo procurou-se demonstrar as vantagens da visualização 3D em comparação com as imagens tradicionais. Nele, a área de interesse pode ser avaliada pelo observador e manipulada de forma clara, apreciando as características físicas do objeto e suas relações espaciais. Assim, a manufatura aditiva ou impressão 3D funcionou como um dispositivo de visualização 3D, representando uma poderosa ferramenta no auxilio à visualização de diversas estruturas anatômicas. Os modelos gerados representaram um importante meio de comunicação, de modo tangível, passando uma informação mais compreensível para as gestantes.
Com base nestes experimentos, este estudo de modelagem fetal 3D começou usando arquivos de TC de fetos com idade gestacional acima de 30 semanas para a construção de modelos físicos do esqueleto fetal
(7,11). O resultado foi uma série de estruturas de ligação de ossos em um ambiente virtual 3D
(6). Foi realizada a modelagem utilizando o
software Autodesk Maya (Alias Wavefront; California, EUA), para manter a integridade de todo o esqueleto virtual, com preservação de sua forma e coordenadas espaciais, permitindo a produção de um modelo físico, sem perder o posicionamento exato de suas diferentes partes. O desafio seguinte estava na delimitação de toda a superfície externa do corpo fetal a partir dos cortes obtidos da TC. Este processo interativo visual detectou os limites das partes do corpo fetal usando uma caneta digital
stylus, que interage diretamente com a tela do computador. As camadas resultantes de toda a superfície fetal foram sobrepostas, gerando um modelo volumétrico 3D.
Obtidos os resultados dos arquivos de TC, iniciaram-se os estudos usando arquivos oriundos da RM fetal. A segmentação manual foi empregada, porém, o maior problema encontrado estava na espessura dos cortes obtidos por RM e no número menor de cortes obtidos. A principal diferença entre os dados obtidos por TC e RM foi a qualidade do contraste entre os órgãos nas imagens por RM. O contraste da escala de cinza entre os órgãos obtido por RM é maior. Esta maior nitidez permitiu uma fácil separação visual das áreas relevantes usando tela para processamento gráfico com caneta
stylus de pressão variável. Na TC, apenas o esqueleto foi facilmente identificado. Contudo, apesar do melhor contraste obtido por RM, existiu num primeiro momento a limitação do número de cortes obtidos (cerca de 30 a 40 cortes), deixando o resultado final com precisão questionável. Todavia, com o uso da sequência TrueFISP, que passou a oferecer um número maior de cortes (acima de 90 cortes), o contorno fetal obtido passou a ser muito mais nítido. Com esta sequência, deixou-se de ter espessura de corte de 4 mm e passou-se a ter espessura de corte de cerca de 1,0 mm. Nos casos de RM, a obtenção de imagens com melhor qualidade foi mais fácil quanto maior foi a idade gestacional, em função da menor interferência dos artefatos de movimento.
O maior desafio foi a construção dos modelos utilizando a US
(7). Esta modalidade de exame permite uma varredura mais rápida do feto, sendo a imagem automaticamente transformada em imagem virtual 3D na tela
(21–23). Dependendo do tamanho do feto, até 18 semanas de gestação, este processo pode permitir a visualização completa do corpo fetal, ou mais tarde, juntar as partes do corpo fetal usando os blocos separados. Foi utilizada a função TUI (imagens ultrassonográficas de formas tomográficas) do
software GE 4D View para processar as imagens 3D da US, obtendo-se resultados semelhantes aos obtidos por RM. As imagens foram exportadas para o
software Mimics para reconstrução da imagem 3D, mantendo a precisão e a confiabilidade. Assim, o protocolo para RM foi adotado para o processamento das imagens de US.
Com o domínio da reconstrução pela US, abriu-se a possibilidade de combinação dos arquivos obtidos por RM e US, quando adquiridos no mesmo dia
(11). Dessa maneira, todos os arquivos 3D obtidos por US, RM e alguns casos de TC poderiam ser combinados. Como o exemplo do caso 13, imagens em 3D obtidas por US da face, mãos ou pés poderiam ser combinadas a imagens do corpo fetal obtidas por RM, mantendo as devidas proporções biométricas por meio de várias medidas por ambas as técnicas.
Quanto aos custos de produção dos modelos físicos, as quatro técnicas de fabricação adotadas neste estudo estão relacionadas ao tempo de construção e material utilizado, que são os principais itens a serem considerados para o cálculo dos custos
(11). A técnica mais utilizada foi a ZCorp (composto em pó baseado principalmente em gesso). Os modelos físicos resultantes deste processo são os mais baratos, especialmente quando comparados com processos como a estereolitografia ou a sinterização seletiva a laser, técnicas que usam feixe de laser para endurecimento de camada em resina fotossensível ou para sinterização de pó de poliamida
(6,7).
CONCLUSÃOAs técnicas de segmentação e de reconstrução desenvolvidas para a modelagem fetal podem ser aplicadas para a construção de modelos virtuais e físicos obtidos da US, RM e TC, combinadas ou não.
Com base nos resultados deste estudo, acreditamos que os modelos físicos ajudarão, num futuro próximo, no estudo tátil e interativo de anormalidades complexas nas diversas disciplinas. Estas técnicas poderão ser também úteis para os futuros pais, ao recriar um modelo 3D com características físicas do feto, permitindo uma conexão emocional mais direta com a criança por nascer.
REFERÊNCIAS1. Antunes EG, Werner H, Daltro PA, et al. Evaluation of fetal cervical lymphangioma by magnetic resonance imaging and correlation with sonographic findings. Radiol Bras. 2009;42:299–302.
2. Daltro P, Werner H, Gasparetto TD, et al. Congenital chest malformations: a multimodality approach with emphasis on fetal MR imaging. Radiographics. 2010;30:385–95.
3. Hellinger JC, Epelman M. Fetal MRI in the third dimension. Applied Radiology. 2010;39:8–22.
4. Cassart M, Massez A, Cos T, et al. Contribution of three-dimensional computed tomography in the assessment of fetal skeletal dysplasia. Ultrasound Obstet Gynecol. 2007;29:537–43.
5. Dos Santos JL, Werner H, Fontes R, et al. Additive manufactured models of fetuses built from 3D ultrasound, magnetic resonance imaging and computed tomography scan data. In.: Hoque ME, editor. Rapid prototyping technology – principles and functional requirements. Rijeka, Croatia: InTech; 2011. p. 179–92.
6. Werner H, dos Santos JR. Tecnologias 3D. Rio de Janeiro, RJ: Revinter; 2010.
7. Lopes J, Brancaglion Jr A, Azevedo SA, et al. Tecnologias 3D – desvendando o passado, modelando o futuro. Rio de Janeiro, RJ: Lexikon Editora Digital; 2013.
8. Willis A, Speicher J, Cooper DB. Rapid prototyping 3D objects from scanned measurement data. Image and Vision Computing. 2007;25:1174–84.
9. Ferreira C, Santos J, Silva J. Exemplos de aplicações da prototipagem rápida. In: Volpato N, Ahrens C, Ferreira C, et al., editors. Prototipagem rápida – tecnologias e aplicações. São Paulo, SP: Editora Blucher; 2007. p. 195–224.
10. Werner H, dos Santos JR, Fontes R, et al. The use of rapid prototyping didactic models in the study of fetal malformations. Ultrasound Obstet Gynecol. 2008;32:955–6.
11. Werner H, dos Santos JR, Fontes R, et al. Additive manufacturing models of fetuses built from three-dimensional ultrasound, magnetic resonance imaging and computed tomography scan data. Ultrasound Obstet Gynecol. 2010;36:355–61.
12. Werner H, Lopes J, Tonni G, et al. Physical model from 3D ultrasound and magnetic resonance imaging scan data reconstruction of lumbosacral myelomeningocele in a fetus with Chiari II malformation. Childs Nerv Syst. 2015;31:511–3.
13. Werner H, Rolo LC, Araujo Júnior E, et al. Manufacturing models of fetal malformations built from 3-dimensional ultrasound, magnetic resonance imaging, and computed tomography scan data. Ultrasound Q. 2014;30:69–75.
14. Werner H, Dos Santos JL, Araujo Júnior E. Physical models of the foetus created using magnetic resonance imaging, computed tomography, and ultrasound data: history, description, and potential uses. Rev Bras Ginecol Obstet. 2015;37:149–51.
15. Armillotta A, Bonhoeffer P, Dubini G, et al. Use of rapid prototyping models in the planning of percutaneous pulmonary valved stent implantation. Proc Inst Mech Eng H. 2007;221:407–16.
16. Robiony M, Salvo I, Costa F, et al. Virtual reality surgical planning for maxillofacial distraction osteogenesis: the role of reverse engineering rapid prototyping and cooperative work. J Oral Maxillofac Surg. 2007;65:1198–208.
17. Werner H, Dos Santos JRL, Fontes R, et al. Virtual bronchoscopy in the fetus. Ultrasound Obstet Gynecol. 2011;37:113–5.
18. Werner H, Lopes dos Santos JR, Fontes R, et al. Virtual bronchoscopy for evaluating cervical tumors of the fetus. Ultrasound Obstet Gynecol. 2013;41:90–4.
19. Blaas HG, Taipale P, Torp H, et al. Three-dimensional ultrasound volume calculations of human embryos and young fetuses: a study of the volumetry of compound structures and its reproducibility. Ultrasound Obstet Gynecol. 2006;27:640–6.
20. Nelson TR, Bailey MJ. Solid object visualization of 3D ultrasound data. J Med Imaging. 2000;3982:26–34.
21. Araujo Júnior E, Simioni C, Nardozza LMM, et al. Prenatal diagnosis of Beckwith-Wiedemann syndrome by two- and three-dimensional ultrasonography. Radiol Bras. 2013;46:379–81.
22. Araujo Júnior E, Santana EFM, Nardozza LMM, et al. Assessment of embryo/fetus during pregnancy by three-dimensional ultrasonography using the HD live software: iconographic essay. Radiol Bras. 2015;48:52–5.
23. Nardozza LMM, Passos AP, Araujo Júnior E, et al. Reference intervals of fetal cisterna magna volume by two-dimensional method using the multiplanar mode of three-dimensional ultrasonography. Radiol Bras. 2014;47:201–5.
1. Doutores, Médicos Radiologistas da Alta Excelência Diagnóstica e da Clínica de Diagnóstico Por Imagem (CDPI), Rio de Janeiro, RJ, Brasil
2. Doutor, Tecnologista do Instituto Nacional de Tecnologia, Rio de Janeiro, RJ, Designer do Núcleo de Experimentação Tridimensional da Pontifícia Universidade Católica do Rio de Janeiro (PUC-Rio), Rio de Janeiro, RJ, Brasil
3. Bióloga do Núcleo de Experimentação Tridimensional da Pontifícia Universidade Católica do Rio de Janeiro (PUC-Rio), Rio de Janeiro, RJ, Brasil
4. Designer do Núcleo de Experimentação Tridimensional da Pontifícia Universidade Católica do Rio de Janeiro (PUC-Rio), Rio de Janeiro, RJ, Brasil
5. Doutor, Médico Radiologista da Clínica de Diagnóstico Por Imagem (CDPI), Rio de Janeiro, RJ, Brasil
6. Doutor, Professor Titular de Radiologia da Universidade Federal do Rio de Janeiro (UFRJ), Rio de Janeiro, RJ, Brasil
Endereço para correspondência:
Dr. Heron Werner Júnior
Alta Excelência Diagnóstica – Radiologia
Avenida Voluntários da Pátria, 423, Botafogo
Rio de Janeiro, RJ, Brasil, 22270-000
E-mail:
heronwerner@hotmail.comRecebido para publicação em 27/5/2015.
Aceito, após revisão, em 3/9/2015.
Trabalho realizado na Alta Excelência Diagnóstica, Clínica de Diagnóstico Por Imagem (CDPI) e Instituto Fernandes Figueira (IFF/Fiocruz), Rio de Janeiro, RJ, Brasil.

 |
|








