Radiologia Brasileira - Publicação Científica Oficial do Colégio Brasileiro de Radiologia
AMB - Associação Médica Brasileira CNA - Comissão Nacional de Acreditação
 Vol. 49 nº 3 - Maio / Jun. of 2016
Vol. 49 nº 3 - Maio / Jun. of 2016
|
ARTIGOS ORIGINAIS
|
|
|
|
|
Autho(rs): Tiago da Silva Jornada1; Camila Hitomi Murata2; Regina Bitelli Medeiros3 |
|
|
Descritores: Ressonância magnética; Espaço K; Controle de qualidade; Imagens in vivo por ressonância magnética. |
|
|
Resumo: INTRODUÇÃO
Uma opção para diminuir o tempo de aquisição da imagem é reduzir o número de linhas a serem preenchidas no espaço K. Porém, ao adotar tal medida, a qualidade da imagem pode ser degradada(1). Todas as informações usadas para a apresentação das imagens por ressonância magnética (RM) são adquiridas primeiramente no espaço K, que representa o domínio da frequência espacial(2,3). O espaço K não é um local físico no equipamento de RM e sim um conceito abstrato, possível de ser entendido como uma matriz que contém uma série de informações relativas às frequências e fases dos sinais recolhidos(4). Cada vez que um eco - codificação de fase mais codificação de frequência - é obtido, a informação é armazenada numa linha do espaço K. Um ponto no espaço K não corresponde a um ponto na imagem. As linhas periféricas contêm informações sobre a resolução espacial do objeto, enquanto as linhas centrais representam o contraste, sendo que a relação entre o espaço K e a imagem pode ser obtida pela transformada de Fourier bidimensional (2D)(1,2,4). O entendimento sobre o espaço K pode orientar a rotina clínica(2,5), pois o seu preenchimento pode ser manipulado pelo operador. Existem técnicas, como as sequências spineco rápidas, aquisição de imagens paralelas, keyhole, single shot, ecoplanar, eco parcial e meia-Fourier(6), que organizam os dados adquiridos de diferentes modos no espaço K(7). Em alguns modelos de seus equipamentos de RM, a fabricante Philips oferece uma ferramenta chamada de scan percentage (ScP). Este recurso manipula o preenchimento do espaço K usando uma técnica similar à meia-Fourier. O diferencial da ferramenta ScP é que ao adotar um protocolo com valor de ScP máximo (100%), todos os sinais sem nenhum processamento (raw data) serão transportados e armazenados nas linhas do espaço K. Porém, ao mudar o percentual da ScP no protocolo de aquisição, ou seja, adotar uma porcentagem inferior ao valor máximo, algumas informações não serão transportadas, resultando em linhas não preenchidas, mais precisamente as periféricas superiores e inferiores. Nessas regiões, o valor da intensidade de cada pixel será aproximadamente zero(8). Já na meia-Fourier, somente nas linhas periféricas inferiores o valor da intensidade de cada pixel será de aproximadamente zero(6). A adoção da ferramenta ScP na rotina clínica sem o prévio conhecimento sobre a influência dela na qualidade da imagem pode comprometer a análise de doenças, como as associadas à cartilagem(5). A doença mais frequente relacionada à degradação da cartilagem hialina é a osteoartrite, na qual é adotada, por radiologistas, a escala Kellgren-Lawrence (KL) para avaliar o grau de comprometimento da cartilagem(9). A escala KL representa cinco graus de comprometimento: grau 0, que indica cartilagem normal; grau I, que indica estreitamento do espaço articular duvidoso; grau II, possível estreitamento da cartilagem; grau III, estreitamento visual da cartilagem; grau IV, estreitamento notável da cartilagem(9-11). Uma opção para avaliar a qualidade das imagens geradas em RM é usar objetos simuladores(12) dedicados que possibilitem julgar parâmetros técnicos, porém, faltam estudos associando essas imagens com testes in vivo. Para a execução dos testes de controle de qualidade em aparelhos de RM, indica-se usar objetos simuladores dedicados e seguir orientações de publicações de órgãos internacionais. Na literatura especializada, há publicações da Associação Americana de Físicos em Medicina(13), da Associação dos Fabricantes de Equipamentos dos Estados Unidos(14), do Colégio Americano de Radiologia(15), de Wood et al.(16) e do Instituto de Físicos em Medicina do Reino Unido(17). O Colégio Americano de Radiologia propõe a adequação por meio de um programa denominado Acreditação em Imagem por Ressonância Magnética(15). No Brasil não há nenhuma normatização vigente quanto aos testes de controle de qualidade, mas há um programa criado pela Organização Nacional de Acreditação(18) para a avaliação e certificação de serviços de saúde e o Programa de Qualidade em Ressonância Magnética do Colégio Brasileiro de Radiologia e Diagnóstico por Imagem(19). Além disso, existe a publicação de Mazzola et al.(20), adotada como referência na área. O presente trabalho tem como objetivo estudar a influência da ferramenta ScP na qualidade da imagem, associando objetos simuladores com imagens in vivo. MATERIAIS E MÉTODOS Objeto simulador Foi utilizado um equipamento de RM modelo ACS-NT Gyroscan 1,5 T (Philips Medical Systems; Best, Holanda) com gradiente de 15 mT, e o objeto simulador Magphan® (The Phantom Laboratory; Greenwich, NY, EUA) preenchido com água desmineralizada e o sinal captado pela bobina de quadratura de crânio. Os parâmetros técnicos dos protocolos adotados para a realização das imagens com o objeto simulador foram: axial T1 (FOV: 230 mm; RFOV: 100%; TR: 638 ms; TE: 14 ms; flip angle: 90º; NEX: 2; matriz de reconstrução: 512 × 512; matriz de aquisição: 256 × 256; gap: 1; espessura de corte: 4 mm; espaçamento: 4,4 mm) e axial T2 (FOV: 230 mm; RFOV: 100%; TR: 4986 ms; TE: 100 ms; flip angle: 90º; NEX: 2; matriz de reconstrução: 512 × 512; matriz de aquisição: 256 × 256; gap: 1; espessura de corte: 4 mm; espaçamento: 4,4 mm). Para cada protocolo foram estudados quatro valores de ScP: 50%, 70%, 85% e 100%. A influência das variações de intensidade do sinal no espaço K foi analisada a partir das imagens obtidas com o objeto simulador adotando-se três critérios de qualidade - 1) uniformidade; 2) razão sinal-ruído (RSR); 3) resolução espacial de alto contraste -, segundo as recomendações da Associação Americana de Físicos em Medicina(13) e do manual do fabricante(21). 1. Uniformidade - Quantifica o desempenho do equipamento em conseguir representar na imagem uma região homogênea, com um mínimo de variação de intensidade. A uniformidade pode ser dada por: 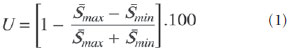 onde: 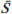 max é o valor da intensidade do pixel de maior sinal e max é o valor da intensidade do pixel de maior sinal e 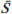 min é o valor da intensidade do pixel de menor sinal. min é o valor da intensidade do pixel de menor sinal.2. RSR - Quantifica a flutuação do sinal em uma dada região de interesse. A RSR pode ser obtida por:  onde: 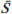 é a média do sinal em uma dada região de interesse e σ é o desvio-padrão decorrente da subtração de duas imagens. é a média do sinal em uma dada região de interesse e σ é o desvio-padrão decorrente da subtração de duas imagens.3. Resolução espacial de alto contraste - Demonstra a capacidade do equipamento em conseguir distinguir, sem sobrepor estruturas, o espaçamento entre objetos. A análise é feita por meio da análise qualitativa de estruturas internas de alta resolução do objeto simulador. Internamente, os objetos representam 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 e 11 pares de linhas/cm (Figura 1). 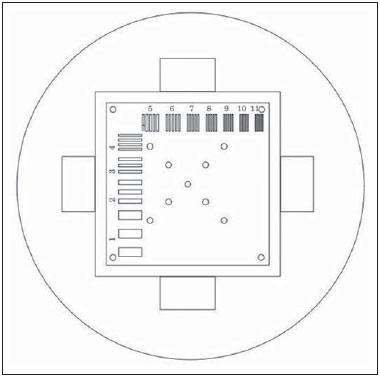 Figura 1. Região do objeto simulador onde é feita a análise da resolução espacial de alto contraste In vivo Para os testes in vivo (aprovado pelo Comitê de Ética e Pesquisa da Instituição - nº CAAE 16837213.1.0000.5505) foi usado o mesmo equipamento de RM com bobina dedicada de joelho, com os seguintes parâmetros de aquisição: plano sagital T1 (FOV: 230 mm; RFOV: 100%; TR: 535 ms; TE: 12 ms; flip angle: 90º; NEX: 2; matriz de reconstrução: 512 × 512; matriz de aquisição: 256 × 256; gap: 1; espessura de corte: 4 mm; espaçamento: 4,4 mm) e sagital T2 (FOV: 230 mm; RFOV: 100%; TR: 2440 ms; TE: 60 ms; flip angle: 90º; NEX: 2; matriz de reconstrução: 512 × 512; matriz de aquisição: 256 × 256; gap: 1; espessura de corte: 4 mm; espaçamento: 4,4 mm). Para cada protocolo foram estudadas sete variações para a ScP: 25%, 40%, 50%, 60%, 70%, 85% e 100%, sendo as imagens analisadas com o leitor RadiAnt DICOM Viewer(22) (Figura 2). 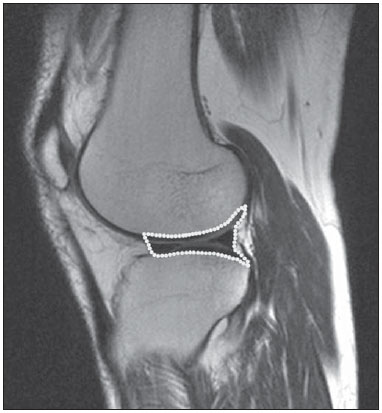 Figura 2. Imagem de ressonância magnética do objeto de estudo in vivo. O contorno pontilhado em branco indica a região de análise. Análise estatística Inicialmente verificou-se a normalidade na distribuição das intensidades dos valores dos pixels na região da cartilagem hialina (Figura 2) com o teste de Kolmogorov-Smirnov Z. No caso de normalidade dos dados, adotou-se a análise de variância com o pós-teste de Student Newman-Keuls. No caso da não normalidade, optou-se por usar Kruskal-Wallis com o pós-teste de Müller-Dunn. A análise estatística foi feita com os softwares SPSS (IBM Corp.; Armonk, NY, EUA) e BioEstat 5.3 (Instituto Mamirauá; Tefé, AM, Brasil). RESULTADOS Na análise das imagens com o objeto simulador, com o auxílio do software MatLab® (MathWorks; Natick, Mass., EUA), aplicamos a transformada inversa de Fourier 2D nas imagens obtidas com cada variação da ScP, resultando no espaço K da respectiva imagem, como mostra a Figura 3. 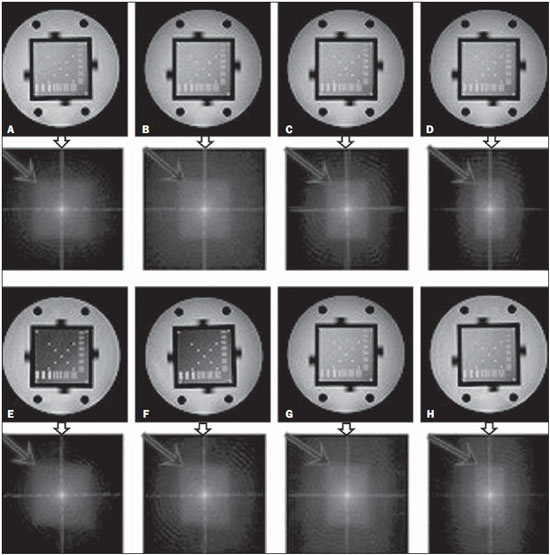 Figura 3. Imagens do objeto simulador com as seguintes variações da ScP: 100% (A), 85% (B), 70% (C) e 50% (D) ponderadas em T1 e 100% (E), 85% (F), 70% (G) e 50% (H) ponderadas em T2. As setas brancas indicam o espaço K de cada imagem. A influência da variação da intensidade do sinal no espaço K, em relação à análise da uniformidade, da RSR e da resolução espacial de alto contraste, consta na Tabela 1. 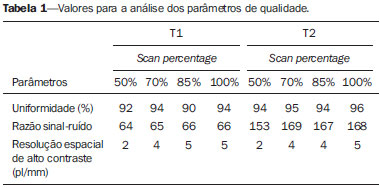 Adotando-se sete porcentagens de preenchimento para o espaço K (25%, 40%, 50%, 60%, 70%, 85% e 100%), foram obtidas imagens anatômicas in vivo (Figuras 4 e 5). 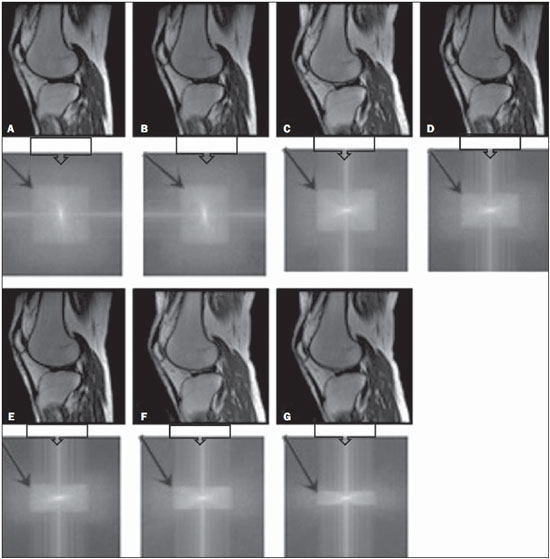 Figura 4. Imagens de ressonância magnética do objeto de estudo in vivo ponderadas em T1 com as seguintes variações da ScP: 100% (A), 80% (B), 70% (C), 60% (D), 50% (E), 40% (F) e 25% (G). As setas pretas indicam o espaço K de cada imagem. 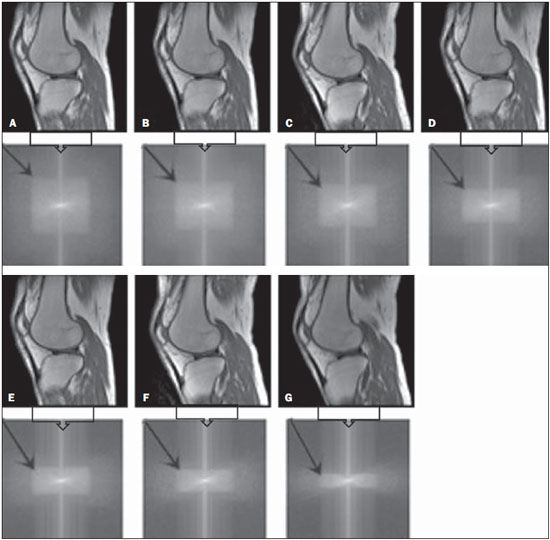 Figura 5. Imagens de ressonância magnética ponderadas em T2 com as seguintes variações da ScP: 100% (A), 80% (B), 70% (C), 60% (D), 50% (E), 40% (F) e 25% (G). As setas pretas indicam o espaço K de cada imagem. O teste de normalidade de Kolmogorov-Smirnov Z apresentou um p < 0,0001 em todas as regiões estudadas, independentemente da ScP adotada, comprovando que a distribuição da intensidade dos valores dos pixels representa uma distribuição paramétrica (normal). Sendo assim, a diferença entre as intensidades nos valores de pixels com as diferentes ScPs foi verificada por meio da análise de variância a 5% e pelo pós -teste de Student Newman-Keuls, também a 5%. A Tabela 2 apresenta os resultados da análise estatística das imagens ponderadas em T1 e a Tabela 3 mostra os resultados da análise estatística das imagens ponderadas em T2. DISCUSSÃO Analisando visualmente cada imagem do espaço K, é possível identificar uma área central com maior intensidade de sinal. Conforme o percentual de preenchimento do espaço K diminui, nota-se uma perda gradual dessa intensidade, independentemente da ponderação adotada. Observa-se que com a ScP a 50% a perda de sinal é mais acentuada, em decorrência da omissão de metade do espaço K. Verificou-se que os valores associados à uniformidade na imagem não apresentaram variações significativas com as ScPs adotadas, mantendo-se dentro do valor de aceitação de no mínimo 90%(15,23). Para o julgamento da RSR, recomenda-se confrontar os valores com referências fornecidas pelo fabricante, mediante medidas seriadas. Como esses dados estão indisponíveis, optou-se por estipular uma margem de aceitação de ±10% na variação da RSR em relação ao valor adquirido com a ScP a 100%. Nas ponderações em T1, a RSR variou em torno de 1%. Em T2, a maior variação na RSR foi 9,8%, adotando-se a ScP a 50%. Portanto, a RSR está em conformidade com a variação adotada. Como esse método de preenchimento mantém as linhas centrais do espaço K inalteradas, foi possível manter os valores da uniformidade e da RSR em conformidade com os critérios adotados. Na análise da resolução espacial houve perda da qualidade da imagem ao se adotar a ScP a 70% em T1 e 85% em T2. A quantificação da resolução espacial recomendada é um valor de ao menos 1 mm (5 pl/mm) com bordas bem definidas entre as estruturas de teste do objeto simulador(15,23), critério não satisfeito com a ScP a 70% em TI e 85% em T2. Uma omissão de 25% das linhas periféricas do espaço K mostrou-se suficiente para a degradação na resolução espacial de alto contraste de modo significativo. A cartilagem em estudo apresentou grau 0 de acometimento em todas as variações estudadas para a ScP. Tanto em T1 quanto em T2 não houve mudança no diagnóstico da degradação da cartilagem quanto à escala KL. Porém, ao se analisar visualmente todos os espaços K (Figuras 4 e 5), é possível notar que há redução na intensidade do sinal, resultando em perda de contraste e na resolução de estruturas. Segundo Albuquerque et al.(11), a análise da degradação da cartilagem e sua classificação KL são subjetivas e podem ser influenciadas pela experiência do radiologista. A perda no contraste e na resolução espacial detectada nas imagens poderá induzir a diagnósticos errôneos em profissionais inexperientes. Nas imagens ponderadas em T1 e T2 obteve-se p < 0,01, com evidências para rejeitar a hipótese nula. Portanto, existe ao menos um grupo com as variâncias populacionais não homogêneas; logo, o preenchimento parcial do espaço K apresentou variação estatisticamente perceptível quanto à intensidade nos valores dos pixels em ao menos uma situação adotada em relação à ScP a 100%. Por meio do pósteste de Student Newman-Keuls, provou-se que a variação no preenchimento do espaço K com a ScP a 25% apresentou diferença estatisticamente perceptível em relação à ScP a 100% nas imagens ponderadas em T1 e T2. CONCLUSÕES O objeto simulador permitiu detectar variações na resolução espacial de alto contraste que não foram perceptíveis nas imagens in vivo, pois o phantom contém padrões conhecidos que permitem uma análise mais criteriosa. A análise com o phantom mostrou ser possível utilizar ScP a 70% em T1 e 85% em T2 na aquisição de imagens clínicas sem que haja perda significativa na qualidade. Para adotar valores abaixo desses níveis de aquisição é necessária a análise junto a uma equipe multidisciplinar e com uma amostra significativa de pacientes. Não é aconselhável adotar ferramentas que limitem o espaço K sem que haja conhecimento sobre sua influência na qualidade da imagem clinicamente gerada. Agradecimentos À Coordenação de Aperfeiçoamento de Pessoal de Nível Superior (Capes), pelas bolsas de estudos de doutorado e mestrado. Aos técnicos em radiologia do setor, pela colaboração na obtenção das imagens e pelas informações específicas referentes a este trabalho. À equipe da Coordenadoria de Física e Higiene das Radiações do Departamento de Diagnóstico por Imagem da Escola Paulista de Medicina da Universidade Federal de São Paulo. REFERÊNCIAS 1. Bronzino JD. The biomedical engineering handbook. 2nd ed. Boca Raton, FL: CRC Press LLC; 2000. 2. Mezrich R. A perspective on k-space. Radiology. 1995;195:297-315. 3. Dhawan AP. Medical image analysis. 2nd ed. Hoboken, NJ: Wiley-IEEE Press; 2011. 4. Mazzola A. Ressonância magnética: princípios de formação da imagem e aplicações em imagem funcional. Rev Bras Fís Méd. 2009;3:117-29. 5. Paschal CB, Morris HD. K-space in the clinic. J Magn Reson Imaging. 2004;19:145-59. 6. Liney G. MRI from A to Z: a definitive guide for medical professionals. 2nd ed. London, UK: Springer-Verlag; 2011. 7. Westbrook C, Roth CK, Talbot J. Ressonância magnética: aplicações práticas. 4ª ed. Rio de Janeiro, RJ: Guanabara Koogan; 2013. 8. Bloemers K, Sjef G. Strategies for faster scanning in orthopedics. Philips NetForum Community; 2005. [cited 2015 June 6]. Available from: http://clinical.netforum.healthcare.philips.com/global/Operate/Application-Tips/MRI/Strategies-for-faster-scanning-inorthopedics 9. Peterfy CG, Guermazi A, Zaim S, et al. Whole-Organ Magnetic Resonance Imaging Score (WORMS) of the knee in osteoarthritis. Osteoarthritis Cartilage. 2004;12:177-90. 10. Roemer FW, Guermazi A, Hunter DJ, et al. The association of meniscal damage with joint effusion in persons without radiographic osteoarthritis: the Framingham and MOST osteoarthritis studies. Osteoarthritis Cartilage. 2009;17:748-53. 11. Albuquerque RP, Giordano V, Sturm L, et al. Análise da reprodutibilidade de três classificações para a osteoartrose do joelho. Rev Bras Ortop. 2008;43:329-35. 12. Chen CC, Wan YL, Wai YY, et al. Quality assurance of clinical MRI scanners using ACR MRI phantom: preliminary results. J Digit Imaging. 2004;17:279-84. 13. AAPM - American Association of Physicists in Medicine. AAPM Report No.100. Acceptance testing and quality assurance procedures for magnetic resonance imaging facilities. [cited 2015 June 6]. Available from: http://www.aapm.org/pubs/reports/RPT_100.pdf 14. NEMA - National Electrical Manufacturers Association. MS1-94. Determination of signal to noise ratio (SNR) in diagnostic magnetic resonance imaging. Rosslyn, VA: National Electrical Manufacturers Association; 1995. 15. ACR - American College of Radiology. Magnetic resonance imaging (MRI) quality control manual. Reston, VA: American College of Radiology; 2001. 16. Wood ML, Price RR. Quality control programs for MRI. In: The physics of MRI: 1992 AAPM Summer School Proceedings. American Institute of Physics. 1993; Medical Physics Monograph No. 21;53:718-53. 17. Lerski R, de Wilde J, Boyce D, et al. IPEM Publication, Report No. 80 - Quality control in magnetic resonance imaging. York, UK: Institute of Physics and Engineering in Medicine; 1998. 18. ONA - Organização Nacional de Acreditação: Selo de Qualificação ONA. [cited 2015 June 6]. Available from: https://www.ona.org.br/Pagina/306/Selo-de-Qualificacao-ONA 19. CBR - Colégio Brasileiro de Radiologia e Diagnóstico por Imagem. Normas Básicas para Inscrição no Programa de Qualidade em Ressonância Magnética [cited 2015 June 6]. Available from: http://cbr.org.br/wp-content/uploads/2013/05/Normativa-Resson--nciaMagn--tica-06.11.14.pdf 20. Mazzola AA, Herdade SB, Koch HA, et al. Protocolo de testes de aceitação em equipamentos de imagem por ressonância magnética. Radiol Bras. 2005;38:195-204. 21. The Phantom Laboratory. Magphan® manual. Greenwich, NY: The Phantom Laboratory Inc.; 2010. 22. RadiAnt DICOM Viewer. [cited 2014 Apr 17]. Available from: http://www.radiantviewer.com/radiant-dicom-viewer-standard.php 23. Kellgren JH, Lawrence JS. Radiological assessment of osteo-arthrosis. Ann Rheum Dis. 1957;16:494-502. 1. Físico Médico, Mestre, Doutorando em Radiologia Clínica no Departamento de Diagnóstico por Imagem da Escola Paulista de Medicina da Universidade Federal de São Paulo (EPM-Unifesp), São Paulo, SP, Brasil 2. Física do Hospital São Paulo, São Paulo, SP, Brasil 3. Professora Associada aposentada da Escola Paulista de Medicina da Universidade Federal de São Paulo (EPM-Unifesp), São Paulo, SP, Brasil Endereço para correspondência: Tiago da Silva Jornada EPM-Unifesp, Departamento de Diagnóstico por Imagem Rua Napoleão de Barros, 800, Vila Clementino São Paulo, SP, Brasil, 04024-002 E-mail: tiagosjornada@gmail.com Recebido para publicação em 19/2/2015. Aceito, após revisão, em 3/7/2015. Trabalho realizado no Departamento de Diagnóstico por Imagem da Escola Paulista de Medicina da Universidade Federal de São Paulo (EPM-Unifesp), São Paulo, SP, Brasil. |
|
Av. Paulista, 37 - 7° andar - Conj. 71 - CEP 01311-902 - São Paulo - SP - Brazil - Phone: (11) 3372-4544 - Fax: (11) 3372-4554