Radiologia Brasileira - Publicação Científica Oficial do Colégio Brasileiro de Radiologia
AMB - Associação Médica Brasileira CNA - Comissão Nacional de Acreditação
 Vol. 48 nº 5 - Set. / Out. of 2015
Vol. 48 nº 5 - Set. / Out. of 2015
|
ARTIGO DE REVISÃO
|
|
|
|
|
Autho(rs): Raquel de Melo Santos Vilas Boas1; Ivana Andrade Madeira1; Alexia Abuhid Lopes2; Edson Barreto Paiva3; André Soares Rodrigues3 |
|
|
Descritores: Ressonância magnética; Pseudotumor inflamatório do quadril; Artroplastia do quadril. |
|
|
Resumo: INTRODUÇÃO
Complicações em partes moles pós-artroplastia do quadril são suscetíveis de ocorrer, seja quando da artroplastia total, seja quando se utiliza a técnica de recapeamento da cabeça femoral (resurfacing). Tanto a literatura ortopédica quanto a radiológica têm chamado a atenção para "massas sintomáticas" que surgem em partes moles adjacentes a próteses, denominadas pseudotumores, reação adversa ao metal, lesões associadas a vasculite linfocítica asséptica, dentre outras. O pseudotumor inflamatório acomete principalmente pacientes com próteses de superfície metal-metal, porém, já foram descritos em próteses metal-polietileno(1-3). Historicamente, as próteses metal-metal ficaram em segundo plano após o advento das próteses de polietileno, em decorrência de maiores taxas de complicações(4,5). Posteriormente, surgiu a necessidade de se criar próteses mais duradouras, principalmente para os pacientes jovens e mais ativos, tendo sido então desenvolvidas próteses metal-metal mais modernas, com a promessa de menores índices de morbidade pós-operatória(4-8). O objetivo deste trabalho é fazer uma revisão da literatura sobre o assunto, descrevendo os principais achados de ressonância magnética desta complicação relacionada à artroplastia do quadril, que precisa ser reconhecida pelo radiologista. DISCUSSÃO O pseudotumor inflamatório é de origem ainda desconhecida, mas parece estar relacionado a reação de hipersensibilidade ao metal e/ou efeito citotóxico decorrente das partículas de metal liberadas pela prótese, acometendo predominantemente os tecidos moles, com surgimento de massas císticas, sólidas ou mistas periprotéticas, podendo evoluir com necrose e dano estrutural mais extenso a longo prazo(4-6,9). Pode manifestar-se meses ou anos após o procedimento cirúrgico(3,4). A sua prevalência na literatura é bastante variável, com relatos de 14% a 36%(6). Os sintomas são inespecíficos e nem sempre estão presentes, podendo ocorrer dor, instabilidade, massa palpável e estar associados ao comprometimento das estruturas neurovasculares adjacentes(7). Existem relatos de níveis aumentados de cromo e cobalto no sangue, urina e no fluido articular, entretanto, não são definidores do diagnóstico e não ocorrem em todos os casos(4,7,9-11). Os principais fatores de risco relatados na literatura são: sexo feminino, jovens (pela maior sobrecarga na prótese em decorrência de maior atividade), mal-posicionamento da prótese e diâmetro reduzido do componente femoral(4,5,9,10). Os principais diagnósticos diferenciais a serem considerados são infecção e neoplasia. A pesquisa de proteína C reativa e velocidade de hemossedimentação séricos auxiliam na exclusão de infecção(9). A ausência de células neoplásicas nos achados histológicos exclui neoplasia. Os achados histológicos incluem necrose e infiltração linfocítica perivascular densa no tecido viável circunjacente. A presença de partículas metálicas é geralmente escassa, mas essas partículas podem ser encontradas no interior de macrófagos(4,6,8,9). Avaliação diagnóstica Uma série de trabalhos recentes publicados no Brasil tem ressaltado a importância dos métodos de imagem na avaliação do sistema musculoesquelético(12-24). A radiografia simples permanece o método de escolha na avaliação do alinhamento e integridade dos componentes da prótese, bem como das complicações mais conhecidas, que incluem osteólise, fraturas, ossificação heterotópica e soltura da prótese(4-7). A ultrassonografia auxilia na avaliação de coleções líquidas e massas, entretanto, tem limitação em lesões maiores ou localizadas em planos profundos(4,5,7,8). A tomografia computadorizada é capaz de detectar grandes coleções, porém, é mais utilizada em conjunto com a radiografia simples para avaliação de complicações ósseas (osteólise) e posicionamento da prótese. As suas principais limitações são o baixo contraste entre os tecidos moles, o que dificulta a identificação de pequenas coleções periprotéticas, e os artefatos, que podem ser minimizados com o uso de equipamentos com multidetectores(4,5,7). A ressonância magnética se tornou um importante aliado no diagnóstico das complicações em partes moles, sobretudo do pseudotumor, com o uso de sequências que minimizam os artefatos de suscetibilidade magnética em aparelhos de 1,5 tesla. O aspecto do pseudotumor na ressonância magnética é geralmente de uma coleção, podendo, entretanto, aparecer como uma massa sólida em partes moles periprotéticas(4-7,9). A intensidade de sinal da coleção é variável na ponderação T1, tendo a maioria sinal semelhante ao conteúdo da bexiga, o que sugere um transudato(9), podendo ter ainda sinal mais alto que o do músculo, o que é mais específico, sugerindo um exsudato complexo(9). Também apresenta intensidade de sinal variável nas ponderações T2 e DP, geralmente hiperintensa em relação ao músculo, podendo ser homogênea ou heterogênea (Figuras 1 e 2). O conteúdo hipointenso nestas ponderações pode estar relacionado a necrose ou depósito de metal(4-6,9), sendo tais ponderações, juntamente com a ponderação STIR, melhores para detectar debris (Figura 2) e nível líquido-líquido, e para avaliar a cápsula, que geralmente é hipointensa e pode ser fina ou espessa, lisa ou irregular (Figuras 2 e 3). A massa sólida é geralmente hipointensa nas ponderações T1 e T2. O contraste intravenoso não é necessário para o diagnóstico, mas quando usado, pode haver impregnação periférica, somente da cápsula da lesão (Figuras 3 e 4)(5,6,9). 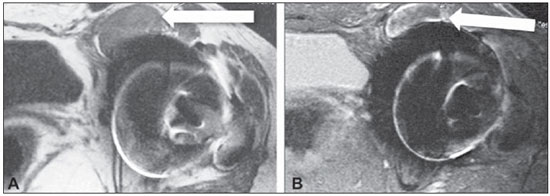 Figura 1. A: Corte axial ponderado em T1 mostrando coleção anterior contígua com a articulação (seta), com conteúdo hiperintenso em comparação com a bexiga. B: Corte axial ponderado em STIR mostrando coleção heterogênea com focos de hipossinal em seu interior (seta). 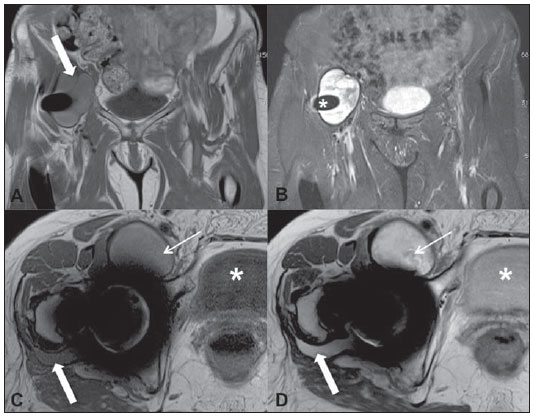 Figura 2. A: Corte coronal ponderado em T1 mostrando coleção predominantemente hiperintensa (seta) em relação ao conteúdo vesical. B: Corte coronal ponderado em STIR mostrando coleção predominantemente hiperintensa com cápsula fina, lisa e hipointensa, em contiguidade com a prótese (asterisco). C,D: Cortes axiais ponderados em T1 e DP mostrando coleção anterior (setas finas). Comparar a intensidade de sinal da coleção nas diferentes sequências em relação à bexiga (asteriscos). Existe pequena coleção no aspecto posterior da articulação coxofemoral, com intensidade de sinal semelhante à coleção anterior, que não pode deixar de ser relatada (setas grossas). 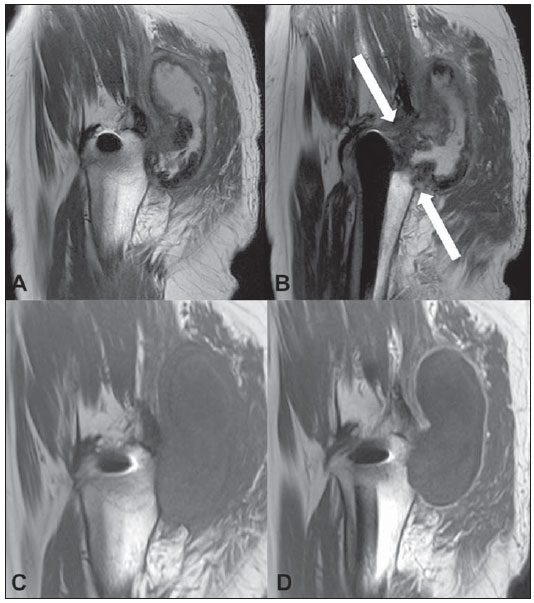 Figura 3. A,B: Cortes sagitais mostrando coleção posterior heterogênea, predominantemente hiperintensa, com cápsula hipointensa espessa e irregular, estendendo-se ao compartimento glúteo. Notar a contiguidade com a articulação (setas). Nos cortes sagitais ponderados em T1, pré-contraste (C) e pós-contraste (D), observar coleção posterior isointensa ao músculo com impregnação periférica pelo contraste. 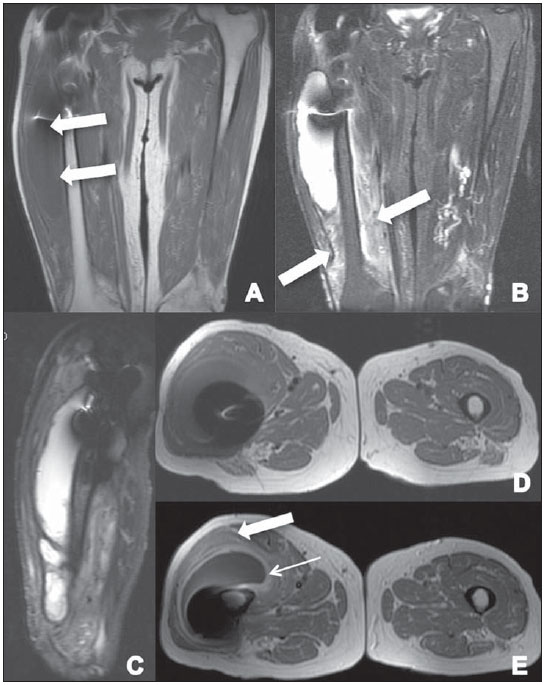 Figura 4. A: Corte coronal ponderado em T1 demonstrando coleção na região lateral da coxa isointensa à musculatura (setas). B: Corte coronal ponderado em STIR mostrando coleção hiperintensa associada a edema na musculatura da coxa (setas). C: Corte sagital STIR identificando coleção hiperintensa com cápsula hipointensa na região anterolateral da coxa. D,E: Cortes axiais ponderados em T1 antes e após injeção de contraste venoso demonstrando coleção isointensa à musculatura, com impregnação da cápsula (seta fina) e da musculatura (seta grossa) pelo contraste, esta última inferindo a presença de edema muscular/miosite. A localização é muito característica, sempre adjacente à prótese e à articulação (Figuras 1, 2 e 3), geralmente relacionada ao trajeto cirúrgico, sendo importante tentar buscar a contiguidade com a articulação, algumas vezes de difícil identificação(Figura 2)(9). O pseudotumor pode se estender aos compartimentos adjacentes - glúteo, adutor, quadricipital, peritrocantérico, anterior (próximo ao iliopsoas), posterior (isquiotibiais) e subcutâneo - através da fáscia profunda(6,9). A presença de alterações miotendíneas associadas deve ser relatada para auxiliar o ortopedista em uma possível reabordagem cirúrgica, e inclui avulsões tendíneas, edema muscular, decorrente de miosite inicial (Figura 4), e atrofia muscular, decorrente da cirurgia e do desuso(4,6,8,9). Pode haver ainda linfadenopatia regional por efeito tóxico direto dos íons metálicos(6). O envolvimento das estruturas neurovasculares adjacentes também deve ser cuidadosamente avaliado, pois pode acarretar neuropatia, estase e/ou trombose(4,6,8). CONCLUSÃO A ressonância magnética é considerada o principal método na avaliação das partes moles pós-artroplastia do quadril, a despeito dos artefatos metálicos, minimizados com o uso de técnicas de "alta banda", cada vez mais apuradas no quesito qualidade versus sinal-ruído. O reconhecimento do pseudotumor inflamatório pelo radiologista torna-se fundamental, diante do número crescente de procedimentos cirúrgicos e das complicações pósoperatórias advindas. REFERÊNCIAS 1. Walsh AJ, Nikolaou VS, Antoniou J. Inflammatory pseudotumor complicating metal-on-highly cross-linked polyethylene total hip arthroplasty. J Arthroplasty. 2012;27:324.e5-8. 2. Mao X, Tay GH, Godbolt DB, et al. Pseudotumor in a well-fixed metal-on-polyethylene uncemented hip arthroplasty. J Arthroplasty. 2012;27:493.e13-7. 3. Murgatroyd SE. Pseudotumor presenting as a pelvic mass: a complication of eccentric wear of a metal on polyethylene hip arthroplasty. J Arthroplasty. 2012;27:820.e1-4. 4. Bestic JM, Berquist TH. Current concepts in hip arthroplasty imaging: metal-on-metal prostheses, their complications, and imaging strategies. Semin Roentgenol. 2013;48:178-86. 5. Ostlere S. How to image metal-on-metal prostheses and their complications. AJR Am J Roentgenol. 2011;197:558-67. 6. Yanny S, Cahir JG, Barker T, et al. MRI of aseptic lymphocytic vasculites-associated lesions in metal-on-metal hip replacements. AJR Am J Roentgenol. 2012;198:1394-402. 7. Hauptfleisch J, Pandit H, Grammatopoulos G, et al. A MRI classification of periprosthetic soft tissue masses (pseudotumours) associated with metal-on-metal resurfacing hip arthroplasty. Skeletal Radiol. 2012;41:149-55. 8. Hayter CL, Gold SL, Koff MF, et al. MRI findings in painful metal-on-metal hip arthroplasty. AJR Am J Roentgenol. 2012;199:884-93. 9. Campe CB, Palmer WE. MR imaging of metal-on-metal hip prostheses. Magn Reson Imaging Clin N Am. 2013;21:155-68. 10. Hasegawa M, Yoshida K, Wakabayashi H, et al. Pseudotumor with dominant B-lymphocyte infiltration after metal-on-metal total hip arthroplasty with a modular cup. J Arthroplasty. 2012;27:493.e5-7. 11. Maurer-Ertl W, Friesenbichler J, Sadoghi P, et al. Metal ion levels in large-diameter total hip and resurfacing hip arthroplasty - preliminary results of a prospective five year study after two years of follow-up. BMC Musculoskelet Disord. 2012;13:56. 12. Arend CF. The carpal boss: a review of different sonographic findings. Radiol Bras. 2014;47:112-4. 13. Arend CF. Sonography of the iliotibial band: spectrum of findings. Radiol Bras. 2014;47:33-7. 14. Terazaki CRT, Trippia CR, Trippia CH, et al. Synovial chondromatosis of the shoulder: imaging findings. Radiol Bras. 2014;47:38-42. 15. Nakamura SA, Lorenzato MM, Engel EE, et al. Incidental enchondromas at knee magnetic resonance imaging: intraobserver and interobserver agreement and prevalence of imaging findings. Radiol Bras. 2013;46:129-33. 16. Souza CG, Gasparetto EL, Marchiori E, et al. Pyogenic and tuberculous discitis: magnetic resonance imaging findings for differential diagnosis. Radiol Bras. 2013;46:173-7. 17. Machado BB, Lima CMAO, Junqueira FP, et al. Magnetic resonance imaging in intersection syndrome of the forearm: iconographic essay. Radiol Bras. 2013;46:117-21. 18. Alves MPT, Fonseca COP, Granjeiro JM, et al. Carpal tunnel syndrome: comparative study between sonographic and surgical measurements of the median nerve in moderate and severe cases of disease. Radiol Bras. 2013;46:23-9. 19. Simão MN, Helms CA, Richardson WJ. Magnetic resonance imaging findings of disc-related epidural cysts in nonsurgical and postoperative microdiscectomy patients. Radiol Bras. 2012;45:205-9. 20. Chojniak R, Grigio HR, Bitencourt AGV, et al. Percutaneous computed tomography-guided core needle biopsy of soft tissue tumors: results and correlation with surgical specimen analysis. Radiol Bras. 2012;45:259-62. 21. Tavares Jr WC, Faria FM, Figueiredo R, et al. Bone attrition: a cause of knee pain in osteoarthritis. Radiol Bras. 2012;45:273-8. 22. Jacob Junior C, Barbosa DM, Batista PR, et al. Thoracolumbar burst fracture: what the radiologist should know. Radiol Bras 2012;45:101-4. 23. Bayerl JS, Oliveira ARN, Peçanha PM, et al. Osteomyelitis of the wrist in a patient with disseminated paracoccidioidomycosis: a rare presentation. Radiol Bras. 2012;45:238-40. 24. Arend CF. Tenosynovitis and synovitis of the first extensor compartment of the wrist: what sonographers should know. Radiol Bras. 2012;45:219-24. 1. Membros Titulares do Colégio Brasileiro de Radiologia e Diagnóstico por Imagem (CBR), Médicas Radiologistas da Clínica Axial Medicina Diagnóstica, Belo Horizonte, MG, Brasil 2. Membro Titular do Colégio Brasileiro de Radiologia e Diagnóstico por Imagem (CBR), Médica Radiologista Especialista em Imagem do Sistema Músculoesquelético da Clínica Axial Medicina Diagnóstica, Belo Horizonte, MG, Brasil 3. Membros Titulares da Sociedade Brasileira de Quadril e da Sociedade Brasileira de Ortopedia e Traumatologia, Cirurgiões de Quadril do Hospital das Clínicas da Universidade Federal de Minas Gerais (UFMG), Belo Horizonte, MG, Brasil Endereço para correspondência: Dra. Alexia Abuhid Lopes Rua Antônio de Albuquerque, 1185/601, Funcionários Belo Horizonte, MG, Brasil, 30112-011 E-mail: lopesbr@terra.com.br Recebido para publicação em 18/10/2013. Aceito, após revisão, em 16/7/2014. Trabalho realizado na Clínica Axial Medicina Diagnóstica, Belo Horizonte, MG, Brasil. |
|
Av. Paulista, 37 - 7° andar - Conj. 71 - CEP 01311-902 - São Paulo - SP - Brazil - Phone: (11) 3372-4544 - Fax: (11) 3372-4554