Radiologia Brasileira - Publicação Científica Oficial do Colégio Brasileiro de Radiologia
AMB - Associação Médica Brasileira CNA - Comissão Nacional de Acreditação
 Vol. 48 nº 2 - Mar. / Abr. of 2015
Vol. 48 nº 2 - Mar. / Abr. of 2015
|
ARTIGO ORIGINAL
|
|
|
|
|
Autho(rs): Yvana Lopes Pinheiro da Silva1; Rita Zanlorensi Visneck Costa2; Kátia Elisa Prus Pinho3; Ricardo Rabello Ferreira4; Sueliton Miyamoto Schuindt5 |
|
|
Descritores: Artrorressonância magnética; Meios de contraste; Ressonância magnética; Xilocaína. |
|
|
Resumo: INTRODUÇÃO
A utilização da ressonância magnética (RM) tem aumentado nos últimos anos, tanto pela maior quantidade de aparelhos disponíveis quanto pela sua ampla aplicação em diversas situações clínicas(1). É considerada como método referência (gold standard) na aquisição de imagens abdominais com o uso de contraste à base de gadolínio(2) e em imagens cardíacas, para quantificação de massa e volume cardíacos(3), sendo também amplamente utilizada no estudo e na avaliação das articulações, permitindo a visualização direta de estruturas anatômicas importantes, incluindo ligamentos, meniscos e tecidos moles periarticulares. Estudos mostram que a delimitação de muitas estruturas intra-articulares, a visualização da anatomia articular normal e a descrição de anormalidades são reforçadas pela presença de uma efusão articular. No exame de artrorressonância magnética (ARM), essa efusão articular é obtida iatrogenicamente, combinando as vantagens da distensão articular, a resolução de alto contraste e imagem multiplanar(4). Antes da aquisição das imagens por meio da RM, uma agulha é inserida dentro da articulação em estudo e a localização intra-articular é confirmada mediante injeção de um pequeno volume de contraste iodado, utilizando orientação fluoroscópica ou da tomografia computadorizada (TC). Em seguida, uma solução diluída de contraste paramagnético em solução salina é injetada na região intra-articular, e a aquisição das imagens é realizada. A técnica pode incluir a injeção simultânea de xilocaína sem vasoconstritor junto ao agente de contraste, com o intuito de proporcionar alívio da dor, ajudando o paciente a permanecer imóvel durante o exame(5). De acordo com a literatura, a diluição do contraste paramagnético juntamente com o contraste iodado pode ter um efeito significativo sobre a qualidade do exame de ARM(6). Assim, os objetivos do estudo foram verificar se a presença do contraste iodado e da xilocaína sem vasoconstritor na solução injetada na articulação altera a qualidade da imagem e o sinal emitido pelo contraste paramagnético, e mensurar qual a concentração de contraste paramagnético mais adequada na realização do exame de ARM. MATERIAIS E MÉTODOS O estudo in vitro foi realizado utilizando gadodiamida (gadolínio) em três diferentes concentrações: 2,5 mmol/L, 5,0 mmol/L e 10,0 mmol/L, e cada concentração foi diluída em 100 mL de solução salina (0,9% de cloreto de sódio). Em seguida, 8 mL de cada uma dessas três soluções, com diferentes concentrações de gadolínio, foram injetadas em nove seringas de 10 mL. Nessas nove seringas contendo 8 mL, nas seringas números 1, 2 e 3 foi adicionado 1,5 mL de solução salina, nas seringas números 4, 5 e 6 foi adicionado 1,5 mL de contraste iodado não iônico, e nas seringas números 7, 8 e 9 foi adicionado 1,5 mL de xilocaína sem vasoconstritor. O volume final em cada seringa da amostra foi 9,5 mL. As soluções de cada seringa foram colocadas em frascos de poliestireno standard com capacidade para 15 mL, os quais foram inseridos em um bloco de poliestireno expandido para imobilização durante a aquisição das imagens (Figura 1). Além disso, seis tubos de controle foram utilizados, três deles preenchidos com 9,5 mL de solução salina e os outros três preenchidos com 9,5 mL de óleo vegetal de soja, para auxiliar na orientação das amostras durante o estudo (Figura 2). 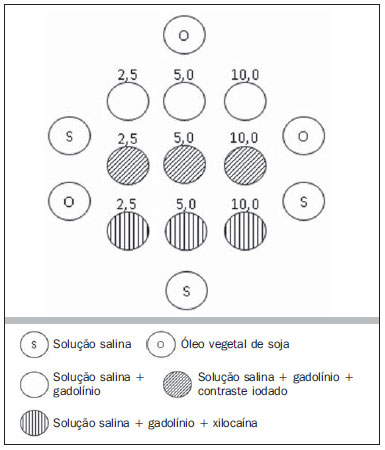 Figura 1. Representação das amostras de teste, em que os números representam a concentração (em mmol/L) de gadolínio utilizada em cada frasco. 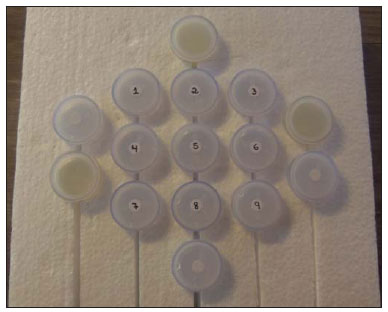 Figura 2. Amostras de teste. Na confecção das amostras do objeto de teste não foram utilizados plásticos coloridos, colas com alta concentração de prótons e outros materiais que possuíssem suscetibilidade magnética muito diferente das soluções que o preencheram, pois estes tipos de materiais podem provocar artefatos locais de inomogeneidade e suscetibilidade(7). Aquisição das imagens As imagens das amostras foram adquiridas com aparelho de RM de 1,5 T, usando a bobina de crânio. A sequência de pulso aplicada foi fast spin eco ponderada em T1 com saturação de gordura, TR = 416,7 ms, TE = 7,9 ms, matriz de 256 × 256 pixels, espessura de corte de 3,0 mm e FOV de 21. Os frascos foram mantidos fechados durante a aquisição das imagens para minimizar mudanças nas soluções (por exemplo, evaporação). O ar condicionado permaneceu com a temperatura de 18°C, fornecendo a mesma temperatura ambiente e, consequentemente, a mesma temperatura das amostras durante o procedimento de aquisição das imagens. Análise das imagens As imagens foram transferidas e analisadas com o software Advantage Workstation GE 2010. A região de interesse (region of interest - ROI) foi utilizada para delimitar a região central das amostras e quantificar o sinal emitido pelo gadolínio em suas diferentes diluições e concentrações na imagem, verificando o valor médio dos níveis de cinza pertencentes a todos os pixels na ROI, isto é, o brilho médio da ROI. As ROIs foram determinadas no centro de cada frasco, onde as intensidades de sinal foram medidas e os valores de amplitude foram registrados. Foram utilizados três tamanhos diferentes de ROI em formato elíptico (6 mm, 9 mm e 12 mm de diâmetro), a fim de realizar a média da intensidade do sinal medida nesses três tamanhos de ROI distintos. Os gráficos foram traçados de acordo com os valores de amplitude (intensidade do sinal na ROI) versus a concentração de gadolínio para cada uma das três misturas de amostra (solução salina, contraste iodado e xilocaína). RESULTADOS Utilizando a sequência de pulso fast spin eco ponderada em T1 (TR/TE = 416,7/7,9) com saturação de gordura (Figura 3), o pico da amplitude de sinal foi produzido na concentração de gadodiamida de 2,5 mmol/L diluída em solução salina normal, para todas as medidas de ROI. A diluição de gadodiamida com contraste iodado e xilocaína resultou em diminuição da amplitude do sinal, para todas as medidas de ROI, em comparação com a diluição de gadodiamida com solução salina. 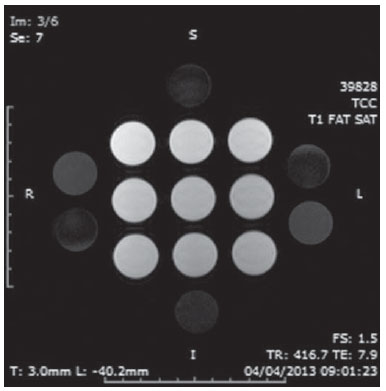 Figura 3. Imagem do objeto de teste obtida por sequência de pulso T1 FSE (TR/TE = 416,7/7,9) com fat sat. Nas medidas de ROI com diâmetro de 6 mm (Figura 4), a intensidade do sinal emitido pelo gadolínio com diluição em contraste iodado diminuiu 18,56% para a concentração de 2,5 mmol/L, 20,13% para a concentração de 5,0 mmol/L e 23,21% para a concentração de 10,0 mmol/L, em comparação com as suas respectivas concentrações diluídas apenas em solução salina. Para a diluição em xilocaína, houve diminuição do sinal emitido pelo gadolínio de 27,80% para a concentração de 2,5 mmol/L, 29,21% para a concentração de 5,0 mmol/L e 27,68% para a concentração de 10,0 mmol/L, também em comparação com as suas respectivas concentrações diluídas apenas em solução salina. 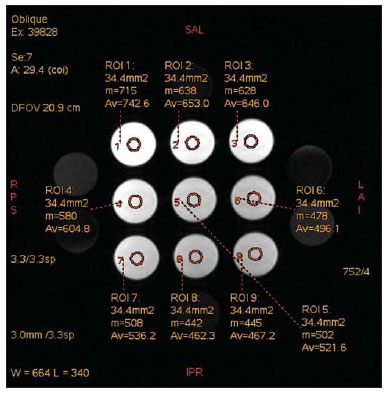 Figura 4. Imagem do objeto de teste analisada com a ROI com diâmetro de 6 mm. Utilizando a ROI com diâmetro de 9 mm (Figura 5), a intensidade do sinal emitido pelo gadolínio com diluição em contraste iodado diminuiu 18,57% para a concentração de 2,5 mmol/L, 20,20% para a concentração de 5,0 mmol/L e 23,48% para a concentração de 10,0 mmol/L, em comparação com as suas respectivas concentrações diluídas somente em solução salina. Para a diluição em xilocaína, houve diminuição de 27,97% para a concentração de 2,5 mmol/L, 29,37% para a concentração de 5,0 mmol/L e 27,87% para a concentração de 10,0 mmol/L do sinal emitido pelo gadolínio, também em comparação com as suas respectivas concentrações diluídas apenas em solução salina. 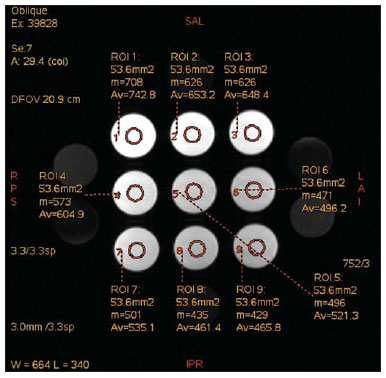 Figura 5. Imagem do objeto de teste analisada com a ROI com diâmetro de 9 mm. Nas medidas de ROI com diâmetro de 12 mm (Figura 6), a intensidade do sinal emitido pelo gadolínio com diluição em contraste iodado diminuiu 18,42% para a concentração de 2,5 mmol/L, 20,38% para a concentração de 5,0 mmol/L e 23,01% para a concentração de 10,0 mmol/L, em comparação com as suas respectivas concentrações diluídas em solução salina. Para a diluição em xilocaína, a diminuição do sinal emitido pelo gadolínio foi 27,72% para a concentração de 2,5 mmol/L, 29,20% para a concentração de 5,0 mmol/L e 27,87% para a concentração de 10,0 mmol/L, também em comparação com as suas respectivas concentrações diluídas apenas em solução salina.  Figura 6. Imagem do objeto de teste analisada com a ROI com diâmetro de 12 mm. A Figura 7 mostra a queda da intensidade do sinal de gadodiamida emitido após ser diluída ao contraste iodado e à xilocaína. Foi considerado que o sinal emitido por essas três soluções de gadodiamida diluídas apenas em solução salina representa as intensidades máximas (100%) que o gadolínio emite para cada uma das diferentes concentrações, pois a solução salina é utilizada apenas como diluente da solução injetada na articulação. A intensidade do sinal com diluição de contraste iodado foi 81,48% para a concentração de gadodiamida de 2,5 mmol/L, 79,76% para a concentração de gadodiamida de 5,0 mmol/L e 76,76% para a concentração de gadodiamida de 10,0 mmol/L. Já a intensidade do sinal com diluição de xilocaína foi 72,17% para a concentração de gadodiamida de 2,5 mmol/L, 70,74% para a concentração de gadodiamida de 5,0 mmol/L e 72,09% para a concentração de gadodiamida de 10,0 mmol/L. 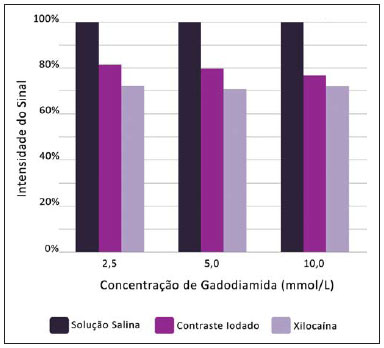 Figura 7. Comparação da diminuição da intensidade do sinal, considerando a diluição de gadodiamida com solução salina como sendo a intensidade máxima. DISCUSSÃO Uma maior resolução de contraste intrínseco dos tecidos moles, associada a não exposição à radiação ionizante, tornaram a RM uma ótima escolha para fins de rastreio(8), como na avaliação das articulações. A ARM tem sido utilizada para uma avaliação detalhada dos transtornos internos das articulações, em virtude da sua capacidade de descrever pequenos detalhes anatômicos e aumentar a precisão diagnóstica. Em muitas circunstâncias é superior ao exame convencional de RM sem contraste e à artrografia por TC na avaliação de várias doenças que afetam o ombro, o joelho, o quadril e outras articulações(9). Brown et al.(5) realizaram estudo in vitro, no qual três agentes de contraste iodados foram misturados e incubados com contraste paramagnético. Verificaram que nenhum íon de gadolínio se dissociava do complexo, mesmo após a adição de solução salina, de xilocaína ou de epinefrina. Esses resultados demonstram que a mistura de material de contraste à base de gadolínio e contraste iodado é segura, podendo também ser misturado com xilocaína e/ou epinefrina para uso clínico. Segundo Montgomery et al.(6), a literatura relata inconsistência, tanto na concentração de gadolínio utilizada no exame de ARM como na quantidade de contraste iodado e xilocaína injetados. Esta variabilidade indica que não existe um protocolo estabelecido para a administração intra-articular de gadolínio, contraste iodado e xilocaína. No presente estudo, as concentrações de gadolínio foram diferentes (2,5 mmol/L, 5,0 mmol/L e 10,0 mmol/L) e as quantidades de contraste iodado (1,5 mL) e xilocaína (1,5 mL) foram mantidas iguais, sendo que tais quantidades são as mesmas utilizadas pelos médicos que realizam os exames de ARM na clínica onde o estudo foi realizado. Foi constatado que o aumento da concentração de gadolínio nas amostras ocasiona a diminuição da intensidade do sinal emitida pelo gadolínio, para todas as diluições. Isto porque, segundo Bushong(10), se a concentração de gadolínio em uma área torna-se extremamente elevada, é possível que o efeito T2 domine mesmo em uma imagem ponderada em T1, causando perda de intensidade do sinal em ambos os tipos de imagens. De acordo com Montgomery et al.(6), isso pode ser prejudicial, principalmente em exames realizados em articulações com baixo volume de líquido sinovial, como na região do punho, pois nessas articulações há uma menor diluição do contraste. Portanto, a utilização de uma concentração de gadolínio de 2,5 mmol/L permite alguma diluição no líquido sinovial, que pode até aumentar a intensidade do sinal, com base nos resultados e no estudo realizado por Montgomery et al.(6). Aprimorar a concentração de gadolínio e a quantidade de contraste iodado e xilocaína utilizadas resulta em diferenças visualmente perceptíveis que podem afetar significativamente a qualidade do diagnóstico do exame de ARM. Outra implicação destes dados é que relatórios anteriores, estudando a eficácia do exame de ARM, podem não ter utilizado concentrações adequadas de gadolínio e/ou minimizado o uso de contraste iodado e xilocaína. Como resultado, a importância diagnóstica da ARM em relação às outras modalidades de exames pode ter sido subestimada(6). O presente estudo demonstra que a adição de contraste iodado ou de xilocaína faz com que haja diminuição do sinal emitido pelo gadolínio, coincidindo com a sugestão de Kopka et al.(11), que diz que o contraste iodado diminui o efeito T1 do gadolínio, embora este exato mecanismo ainda não esteja claro. Com relação à xilocaína, até o momento não existem estudos comparativos que demonstrem o seu efeito nas imagens de ARM. Isto pode ser pelo fato de a xilocaína não ser utilizada com a mesma frequência que o contraste iodado neste tipo de exame. CONCLUSÃO Os resultados demonstram que o pico de intensidade do sinal emitido foi obtido com uma concentração de gadodiamida na faixa de 2,5 mmol/L, diluída em solução salina normal (Figuras 4, 5 e 6). Sendo assim, com base nos resultados, em razão da presença de contraste iodado e da xilocaína sem vasoconstritor na solução injetada na articulação, recomenda-se a utilização de uma concentração de gadolínio próxima ou inferior a 2,5 mmol/L. As diluições de gadolínio em contraste iodado e em xilocaína diminuíram a intensidade de sinal em 20,67% para o contraste iodado e 28,34% para a xilocaína, em comparação com as amostras de concentração idêntica diluídas em solução salina. Esses valores percentuais são as médias calculadas em relação às três diferentes concentrações de gadolínio, com suas diluições em contraste iodado e xilocaína, e aos diferentes tamanhos de ROI. Portanto, de acordo com os resultados, minimizar o uso do meio de contraste iodado e da xilocaína e/ou a utilização de uma concentração de gadolínio com 2,5 mmol/L diluída em solução salina irá aperfeiçoar a sensibilidade e a especificidade do exame de ARM na avaliação de transtornos internos das articulações. REFERÊNCIAS 1. Galvão BVT, Torres LR, Cardia PP, et al. Prevalência de cistos simples e hemangiomas hepáticos em pacientes cirróticos e não cirróticos submetidos a exames de ressonância magnética. Radiol Bras. 2013;46:203-8. 2. Kim YH, Shin SS, Burke LMB, et al. Hemangioma hepático subcapsular com realce perilesional: achados de RM. Radiol Bras. 2010;43:384-8. 3. Barranhas AD, Santos AASMD, Coelho-Filho OR, et al. Cardiac magnetic resonance imaging in clinical practice. Radiol Bras. 2014;47:1-8. 4. Hajek PC, Sartoris DJ, Neumann CH, et al. Potential contrast agents for MR arthrography: in vitro evaluation and practical observations. AJR Am J Roentgenol. 1987;149:97-104. 5. Brown RR, Clarke DW, Daffner RH. Is a mixture of gadolinium and iodinated contrast material safe during MR arthrography? AJR Am J Roentgenol. 2000;175:1087-90. 6. Montgomery DD, Morrison WB, Schweitzer ME, et al. Effects of iodinated contrast and field strength on gadolinium enhancement: implications for direct MR arthrography. J Magn Reson Imaging. 2002;15:334-43. 7. Price RR, Axel L, Morgan T, et al. Quality assurance methods and phantoms for magnetic resonance imaging: report of AAPM Nuclear Magnetic Resonance Task Group No. 1. Med Phys. 1990;17:287-95. 8. Hernandes MA, Semelka RC, Elias Jr, et al. Whole-body MRI: comprehensive evaluation on a 48-channel 3T MRI system in less than 40 minutes. Preliminary results. Radiol Bras. 2012;45:319-25. 9. Choi JY, Kang HS, Hong SH, et al. Optimization of the contrast mixture ratio for simultaneous direct MR and CT arthrography: an in vitro study. Korean J Radiol. 2008;9:520-5. 10. Bushong SC. Magnetic resonance imaging: physical and biological principles. 3rd ed. Philadelphia, PA: Mosby; 2003. 11. Kopka L, Funke M, Fischer U, et al. MR arthrography of the shoulder with gadopentetate dimeglumine: influence of concentration, iodinated contrast material, and time on signal intensity. AJR Am J Roentgenol. 1994;163:621-3. 1. Tecnóloga em Radiologia pela Universidade Tecnológica Federal do Paraná (UTFPR), Curitiba, PR, Brasil 2. Doutora em Ciências, Docente da Universidade Tecnológica Federal do Paraná (UTFPR), Curitiba, PR, Brasil 3. Doutoranda em Ciências, Docente da Universidade Tecnológica Federal do Paraná (UTFPR), Curitiba, PR, Brasil 4. Médico Especialista em Radiologia e Ultrassonografia, Radiologista do Centro Diagnóstico Água Verde (Cedav), Curitiba, PR, Brasil 5. Tecnólogo em Radiologia, Estudante de Medicina na Universidade Federal do Paraná (UFPR), Curitiba, PR, Brasil Endereço para correspondência: Yvana Lopes Pinheiro da Silva Rua Pedro Collere, 699, Vila Izabel Curitiba, PR, Brasil, 80320-320 E-mail: yvanaa@gmail.com Recebido para publicação em 3/10/2013. Aceito, após revisão, em 3/9/2014. Trabalho realizado no Centro Diagnóstico Água Verde (Cedav), Curitiba, PR, Brasil. |
|
Av. Paulista, 37 - 7° andar - Conj. 71 - CEP 01311-902 - São Paulo - SP - Brazil - Phone: (11) 3372-4544 - Fax: (11) 3372-4554