Radiologia Brasileira - Publicação Científica Oficial do Colégio Brasileiro de Radiologia
AMB - Associação Médica Brasileira CNA - Comissão Nacional de Acreditação
 Vol. 47 nº 1 - Jan. / Fev. of 2014
Vol. 47 nº 1 - Jan. / Fev. of 2014
|
ARTIGO ORIGINAL
|
|
|
|
|
Autho(rs): Omar Carneiro Filho1; Osvaldo Vilela Filho2; Paulo César Ragazzo3; Lea Mirian Barbosa da Fonseca4 |
|
|
Descritores: Cirurgia radioguiada; Epilepsia; Gamaprobe; Eletrocorticografia; SPECT cerebral. |
|
|
Resumo: INTRODUÇÃO
A epilepsia é um dos distúrbios neurológicos crônicos mais prevalentes, afetando 1-2% da população mundial(1,2). Não obstante a grande variedade de drogas anticonvulsivantes atualmente disponíveis, 25-30% dos pacientes persistem refratários ao tratamento conservador otimizado. Essa refratariedade, geralmente maior nas epilepsias parciais do que nas generalizadas, é a causa de significativo prejuízo da qualidade de vida e da autoestima. Isto sugere que, nestes casos, o tratamento cirúrgico pode ser considerado como uma alternativa terapêutica(3). Nem todos os pacientes portadores de epilepsia refratária, mas apenas parte deles é candidata à cirurgia(4). Os pacientes que apresentam epilepsias parciais são, normalmente, mais frequentemente candidatos à cirurgia do que os com epilepsias generalizadas(5). A definição quanto à indicação cirúrgica e da técnica cirúrgica de eleição depende da localização e do número de focos epileptogênicos (FEs), além do tipo de epilepsia(6). Nas epilepsias generalizadas, os FEs são geralmente bilaterais e múltiplos. Assim, a ressecção dos focos é pouco viável, optando-se pelas técnicas desconectivas (calosotomia) ou neuromodulatórias (estimulação do nervo vago esquerdo ou estimulação cerebral profunda do núcleo centromediano do tálamo). Já nas epilepsias parciais (simples ou complexas), os focos são unilaterais e frequentemente bem localizados. Nestes casos, opta-se pelas cirurgias ressecantes do FE. Quando inviável, por estar o FE localizado em áreas cerebrais eloquentes, a opção cirúrgica recai sobre as técnicas neuromodulatórias, como a estimulação cerebral profunda do núcleo anterior do tálamo ou do hipocampo. Considerando-se o supramencionado, pode-se concluir que a identificação do FE é condição sine qua non para a indicação cirúrgica. Para tal fim, necessitamos de minuciosa propedêutica para a descrição da crise convulsiva: a avaliação neuropsicológica; o eletroencefalograma (EEG); o vídeo-EEG (permite a correlação eletroclínica), sem ou com eletrodos invasivos (forame oval, subdurais ou intracerebrais); a ressonância magnética (RM), que permite a identificação de lesões estruturais epileptogênicas, quando presentes, por meio da localização de esclerose mesial temporal, e pequenas áreas de displasia cortical; a tomografia computadorizada (TC) por emissão de fóton único (SPECT), no intervalo ou durante as crises convulsivas, isto é, interictal ou ictal; e a tomografia por emissão de pósitrons (PET), interictal ou ictal, que permite a identificação de áreas funcionalmente anormais, correspondentes aos FEs. No caso das cirurgias ressecantes, em especial das epilepsias extratemporais, quando a monitoração invasiva não foi empregada, é necessária a confirmação intraoperatória do FE. Para este fim se presta a eletrocorticografia, e sendo o FE desta forma identificado, é então ressecado no ato cirúrgico(6,7). A questão que apresentamos é a seguinte: poderíamos identificar o foco epileptogênico intraoperatoriamente de alguma outra forma? A cintilografia da perfusão cerebral ou o SPECT cerebral é hoje um exame complementar consagrado para o diagnóstico de uma série de doenças. O radiotraçador, administrado por via intravenosa, fica concentrado na área cortical normal e anormal por várias horas, ao contrário das demais regiões do organismo que mostram um washout fisiológico. Considerando-se esta característica, surgiu a ideia de se utilizar um detector portátil de raios gama para uso intraoperatório, o gamaprobe. O gamaprobe é geralmente utilizado para se localizar linfonodos sentinelas ou lesões primárias em casos oncológicos. A técnica de se utilizar o gamaprobe em cirurgias cerebrais, conhecida como cirurgia assistida por gamaprobe, foi introduzida pioneiramente na prática médica para guiar a ressecção de tumores cerebrais(8). Considerando que o SPECT cerebral ictal pode detectar os FEs e que o radiomarcador fica retido na área cortical anormal por várias horas, os autores consideraram a hipótese de que o gamaprobe pode permitir a identificação intraoperatória no ponto de origem da crise epiléptica (Figura 1). O presente estudo foi desenhado para testar tal hipótese. 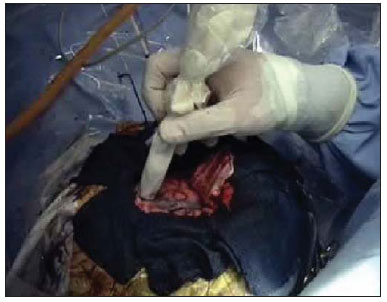 Figura 1. Neurocirurgia guiada por gamaprobe com base na captação mais intensa das contagens na região do foco epileptogênico. MATERIAIS E MÉTODOS Dois pacientes foram arrolados para este estudo piloto. Ambos apresentavam epilepsia refratária ao tratamento conservador otimizado. Uma vez informados sobre o objetivo da presente pesquisa - que o gamaprobe não seria utilizado para guiar a cirurgia, mas apenas para comparar os resultados obtidos com este instrumento com os obtidos pela eletrocorticografia -, ambos assinaram o termo de consentimento informado. Os estudos de SPECT cerebral foram realizados no estado basal (fase interictal) e sob crise epilética (fase ictal) horas antes da cirurgia. Não foi necessário acrescentar mais dose de radiofármaco, além do convencional. Todos os procedimentos cirúrgicos radioguiados foram realizados sob a dose padrão aplicada horas antes. As imagens dos exames de medicina nuclear (fases interictal e ictal) foram apresentadas à equipe de neurocirurgiões, imediatamente antes da cirurgia. Os demais exames foram realizados durante a internação dos pacientes. O paciente 1, do sexo masculino, 25 anos, destro, apresentava crises parciais complexas (média de cinco crises por mês) há 16 anos. O EEG interictal registrou atividade epileptogênica intermitente em lobo temporal esquerdo e o vídeo-EEG ictal mostrou início de crise nos eletrodos zigomático e mediotemporal esquerdos. À RM observou-se um cavernoma em giro fusiforme do mesmo lado (Figura 2) e ao SPECT ictal notou-se hiperperfusão temporal esquerda (Figura 3). A avaliação neuropsicológica revelou piora global da memória, em especial da memória verbal. 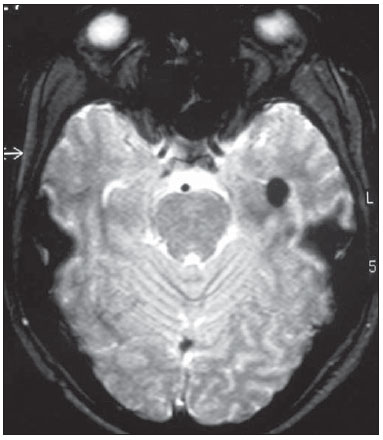 Figura 2. Ressonância magnética do paciente 1 mostrando cavernoma em giro fusiforme do lobo temporal esquerdo.  Figura 3. SPECT cerebral do paciente 1 em fase ictal mostrando incremento do microfluxo sanguíneo regional no lobo temporal esquerdo. A paciente 2, do sexo feminino, 29 anos, sinistra, apresentava crises parciais complexas e crises clônicas do pescoço com rotação da cabeça para a esquerda desde a adolescência. O EEG interictal revelou atividade epileptogênica nos eletrodos T6, P4 e O2. O vídeo-EEG ictal registrou três crises típicas, mas não permitiu localizar ou lateralizar o início da crise (inconclusivo). A RM demonstrou atrofia temporoparietal posterior e occipital direita (Figura 4), e o SPECT ictal mostrou grande área de hiperperfusão que circundava uma menor área de hipoperfusão (Figura 5). A avaliação neuropsicológica revelou apenas leve comprometimento da memória verbal. 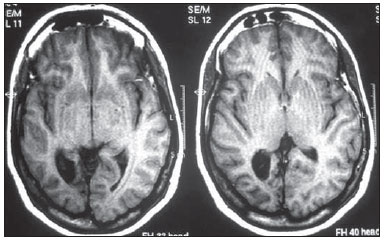 Figura 4. Atrofia cortical no hemisfério cerebral direito, especificamente nas áreas temporoparietal posterior e no lobo occipital. 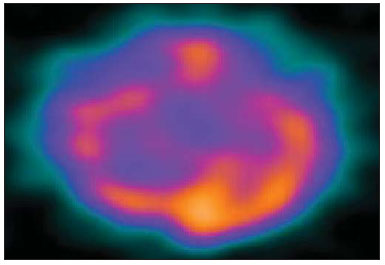 Figura 5. SPECT cerebral interictal do paciente 2, em que se nota redução do microfluxo sanguíneo cerebral na região posterior do hemisfério direito, nas áreas temporoparietal posterior e no lobo occipital. O radiofármaco utilizado no SPECT ictal foi a etilenodiaminocisteína (ECD) marcada com tecnécio-99m, ambos fabricados pelo Instituto de Pesquisas Energéticas e Nucleares/Comissão Nacional de Energia Nuclear, Brasil. Os pacientes foram operados poucas horas (menos que cinco horas) após a injeção do ECD, de fase ictal. A cirurgia foi realizada sob anestesia geral. Após realização da craniotomia sobre a provável área epileptogênica, procedeu-se à radiocontagem com o gamaprobe (Neoprobe 2000 - Johnson & Johnson; EUA). As áreas com contagem aumentada e também reduzida (paciente 2) foram demarcadas com fio de algodão. Em seguida realizou-se a eletrocorticografia com placa subdural, sendo implantados eletrodos de profundidade na cabeça do hipocampo e na amígdala, inicialmente da atividade espontânea e, a seguir, após ativação com alfentanil. A área de hiperperfusão em temporal esquerdo (paciente 1) foi demarcada e retirada. As áreas mapeadas (eletrocorticografia) de atividade epileptogênica foram então delimitadas e comparadas com aquelas detectadas pelo gamaprobe. Concluída a lesionectomia, procedeu-se a uma nova radiocontagem do local da excisão e da peça cirúrgica (ex-vivo). RESULTADOS No paciente 1, o estudo eletrográfico da atividade espontânea revelou-se basicamente normal. Após ativação com alfentanil(9) no intraoperatório, observou-se crise eletrocorticográfica iniciando-se na cabeça do hipocampo. A radiocontagem inicialmente revelou-se máxima no giro temporal médio, cerca de 3,5 cm posterior à ponta do lobo temporal esquerdo. Após realização da corticotomia, nova radiocontagem revelou-se máxima na cabeça do hipocampo, demonstrada pelo aparelho gamaprobe. Procedeu-se à ressecção do cavernoma e a lobectomia temporal anteromedial pela técnica de Spencer. Na paciente 2, uma vez aberta a dura-máter, observou-se área de atrofia e gliose correspondente àquela vista na RM. A radiocontagem confirmou os achados do SPECT ictal, isto é, radiocontagem reduzida na área atrófico-gliótica e radiocontagem aumentada em uma faixa superior, inferior e anterior àquela. O estudo eletrocorticográfico da atividade espontânea mostrou polipontas-ondas lentas na área atróficogliótica e, após ativação com alfentanil, pontas quase contínuas na mesma área propagando para o lóbulo parietal superior e, posteriormente, para o lobo temporal e cabeça do hipocampo(9). Após a ressecção das lesões, as áreas adjacentes mostraram atividade de radiocontagem normal. A congruência entre os achados eletrocorticográficos e de radiocontagem foram praticamente similares em ambos os pacientes. Após acompanhamento clínico por um período de dois anos, observamos a ausência de crises epiléticas nos dois pacientes. DISCUSSÃO Um número significativo de epilepsias intratáveis de longa duração pode se dever à presença de lesões cerebrais identificáveis aos exames de neuroimagem, destacando-se esclerose temporal mesial, displasias corticais, tumores benignos e cavernomas. A ressecção dessas lesões é de extrema relevância para o melhor controle das crises convulsivas. Tais lesões podem ou não ser visíveis a olho nu. A sua identificação pode necessitar de alguma técnica no pré-operatório ou mesmo no intraoperatório, incluindo métodos morfológicos (TC e RM), métodos funcionais (SPECT, PET, EEG) ou eletrocorticografia(10). Existem ainda a RM e a TC intraoperatórias, que implicam em elevado custo e estão disponíveis em apenas uns poucos centros no mundo(10). Uma alternativa viável seria o uso da neuronavegação(11), cujo equipamento pode ser locado. Além de estar restrito a poucos centros de medicina, um problema inerente à neuronavegação é o desvio cerebral decorrente da saída de liquor e da entrada de ar após a abertura da dura-máter. Estes métodos, a despeito de sua eficácia na identificação das lesões cerebrais, são ineficazes para a identificação de áreas funcionalmente anormais. Não infrequentemente, a área epileptogênica é maior do que a área estruturalmente anormal, como observado no paciente 1, portador de um cavernoma do giro fusiforme esquerdo, cujo FE se estendia à cabeça do hipocampo. Alguns pacientes apresentam, aos exames de neuroimagem estrutural, mais de uma lesão, podendo ser impossível definir qual delas seria a causa inicial da epilepsia intratável. Finalmente, cumpre salientar que muitos pacientes com epilepsia intratável não apresentam qualquer evidência de lesão estrutural (epilepsia criptogênica), e nesses casos a RM, a TC e a neuronavegação nada teriam a contribuir(11). Os estudos e pesquisas realizados corroboram que as crises parciais complexas perfazem aproximadamente 55% das crises convulsivas do adulto. A maioria destas é oriunda no lobo temporal; nestes casos, o tratamento cirúrgico é realizado utilizando-se de técnicas padrões, como a lobectomia temporal ou a amígdalo-hipocampectomia seletiva, tornando a eletrocorticografia virtualmente desnecessária(9). Todavia, cerca de 20% das crises parciais complexas têm origem extratemporal. Nessas situações, em especial quando lesões estruturais não são demonstradas, torna-se obrigatório o registro eletrocorticográfico no intraoperatório para a identificação da área epileptogênica. Este método é considerado padrão ouro para este fim. No presente estudo mostramos que a radiocontagem por meio do gamaprobe foi tão eficaz quanto o registro eletrocorticográfico no intraoperatório para a detecção da área epileptogênica nos dois pacientes em que foi empregada. Na técnica empregada não foi necessária a administração de radiofármaco adicional para a sua execução; basta a dose injetada para a realização do SPECT ictal, desde que a cirurgia seja realizada nas horas seguintes. O gamaprobe é capaz de detectar regiões de maior acúmulo do radiotraçador, por meio de som e da leitura de contagens. Diferentemente da gamacâmara que produz imagem, o gamaprobe fornece uma contagem digital. Funciona como um microfone unidirecional, captando proporcionalmente os raios gama apenas das estruturas situadas à sua frente. A área epileptogênica, funcionalmente anormal, concentra maior atividade do radiofármaco em relação ao tecido normal, por até cerca de 10 horas, cujos raios gama podem ser detectados pelo gamaprobe. Assim, enquanto a eletrocorticografia identifica a área epileptogênica, o gamaprobe identifica a área funcionalmente anormal (podendo também ser estruturalmente anormal), que corresponde virtualmente àquela. Vale ressaltar que é um método seguro, que não interfere em momento algum na dinâmica diagnóstica, auxiliando uma abordagem cirúrgica direcionada. A maior limitação deste estudo está no pequeno número de pacientes em que a técnica foi testada, tornando-se necessária a realização de um estudo prospectivo, randomizado, com um número muito maior de pacientes, comparando a eletrocorticografia e os achados do gamaprobe para se confirmar os resultados obtidos. CONCLUSÃO Este método parece ser de grande valia na detecção de áreas epileptogênicas, por mostrar estreita correlação com os achados da eletrocorticografia (padrão ouro), tendo a vantagem de não ser invasivo e de mostrar, in loco, o foco epileptogênico. Outra vantagem adicional seria a de poder mostrar a redução das contagens radioativas no local da exérese após a retirada da área epileptogênica. Concluímos que as possíveis indicações para a presente técnica estão nas epilepsias extratemporais, nos casos com mais de uma lesão estrutural (dual pathology) e nos casos em que a RM não mostra alterações estruturais (epilepsia criptogênica), casos em que a eletrocorticografia poderia ter significativa dificuldade na detecção do foco no intraoperatório. O estudo demonstra que a radiocontagem por meio do gamaprobe foi tão eficaz quanto o registro eletrocorticográfico intraoperatório para a detecção da área epileptogênica nos pacientes em que foi empregada. Assim, os resultados obtidos com as duas técnicas foram praticamente congruentes. REFERÊNCIAS 1. Shorvon S. Status epilepticus: its clinical features and treatment in children and adults. Cambridge: Cambridge University Press; 1994. 2. Fisher RS, van Emde Boas W, Blume W, et al. Epileptic seizures and epilepsy: definitions proposed by the International League Against Epilepsy (ILAE) and the International Bureau for Epilepsy (IBE). Epilepsia. 2005;46:470-2. 3. Blumer D. Psychiatric aspects of intractable epilepsy. Adv Exp Med Biol. 2002;497:133-47. 4. Carreño M, Lüders HO. General principles of presurgical evaluation. In: Lüders HO, editor. Textbook of epilepsy surgery. London, UK: Informa Healthcare; 2007. p. 407-22. 5. Roger J, Bureau M, Dravet C, et al. Epileptic syndromes in infancy, childhood, and adolescence. 4th ed. Montrouge, France: John Libbey Eurotext; 2005. 6. Schuele SU, Lüders HO. Intractable epilepsy: management and therapeutic alternatives. Lancet Neurol. 2008;7:514-24. 7. Palmini A, Gambardella A, Andermann F, et al. Intrinsic epileptogenicity of human dysplastic cortex as suggested by corticography and surgical results. Ann Neurol. 1995;37:476-87. 8. Vilela Filho O, Carneiro Filho O. Gamma probe-assisted brain tumor microsurgical resection. A new technique. Arq Neuropsiquiatr. 2002;60:1042-7. 9. McGuire G, El-Beheiry H, Manninen P, et al. Activation of electrocorticographic activity with remifentanil and alfentanil during neurosurgical excision of epileptogenic focus. Br J Anaesth. 2003;91:651-5. 10. von Oertzen TJ, Mormann F, Urbach H, et al. Prospective use of subtraction ictal SPECT coregistered to MRI (SISCON) in presurgical evaluation of epilepsy. Epilepsia. 2011;52:2239-48. 11. Cho DY, Lee WY, Lee HC, et al. Application of neuronavigator coupled with an operative microscope and electrocorticography in epilepsy surgery. Surg Neurol. 2005;64:411-8. 1. Especialista em Medicina Nuclear, Diretor do Cebramen - Centro Brasileiro de Medicina Nuclear e Imagem Molecular e do Imen - Instituto de Medicina Nuclear, Goiânia, GO, Brasil 2. Doutor, Professor Adjunto e Chefe do Serviço de Neurocirurgia do Hospital das Clínicas da Faculdade de Medicina da Universidade Federal de Goiás (UFG), Professor Adjunto da Pontifícia Universidade Católica de Goiás (PUC Goiás), Goiânia, GO, Brasil 3. Doutor, Neurologista, Diretor do Serviço de Epilepsia e Neurofisiologia do Instituto de Neurologia de Goiânia, Goiânia, GO, Brasil 4. Doutora, Professora Titular de Medicina Nuclear do Departamento de Radiologia da Universidade Federal do Rio de Janeiro (UFRJ), Rio de Janeiro, RJ, Brasil Endereço para correspondência: Dr. Omar Carneiro Filho Alameda dos Buritis, 600, Centro Goiânia, GO, Brasil, 74015-080 E-mail: dromarcarneiro@gmail.com Recebido para publicação em 29/10/2012. Aceito, após revisão, em 23/8/2013. Trabalho realizado no Instituto de Neurologia de Goiânia, no Imen - Instituto de Medicina Nuclear e no Cebramen - Centro Brasileiro de Medicina Nuclear e Imagem Molecular, Goiânia, GO, Brasil. |
|
Av. Paulista, 37 - 7° andar - Conj. 71 - CEP 01311-902 - São Paulo - SP - Brazil - Phone: (11) 3372-4544 - Fax: (11) 3372-4554