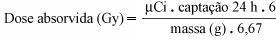Radiologia Brasileira - Publicação Científica Oficial do Colégio Brasileiro de Radiologia
AMB - Associação Médica Brasileira CNA - Comissão Nacional de Acreditação
 Vol. 34 nº 6 - Nov. / Dez. of 2001
Vol. 34 nº 6 - Nov. / Dez. of 2001
|
ARTIGO ORIGINAL
|
|
|
|
|
Autho(rs): Marcelo Tatit Sapienza, Bernardo Pedreira Coelho, Miriam R.Y. Okamoto, Fábio L.N. Marques, Tomoco Watanabe, Carla Rachel Ono, Paulo Aguirre Costa, Fausto Hironaka, Carlos Alberto Buchpiguel |
|
|
Descritores: Neoplasias de tireóide, Radioisótopos do iodo, Tireoidectomia, Adenocarcinoma folicular, Carcinoma papilífero, Imagem com radionuclídeos |
|
|
Resumo:
INTRODUÇÃO A pesquisa de corpo inteiro com iodo-131 (PCI) tem importante papel na detecção de restos tireoidianos e metástases dos carcinomas diferenciados da tireóide. As informações obtidas pela PCI auxiliam a estabelecer a atividade a ser posteriormente ministrada no tratamento desses pacientes. Nos últimos anos, porém, tem sido descrito o atordoamento da tireóide após a PCI(1-3). Este atordoamento deve-se à dose de radiação absorvida pelos restos e/ou tumores diferenciados após a administração do iodo-131 com finalidades diagnósticas. O atordoamento leva à redução da captação de iodo-131 em posterior dose terapêutica, reduzindo sua eficácia. Diferentes medidas são sugeridas para evitar o atordoamento, incluindo a redução da atividade utilizada no estudo diagnóstico, a modificação dos intervalos entre a PCI e o tratamento(4), a substituição do iodo-131 pelo iodo-123(4) e até a não realização da PCI pré-dose terapêutica(4-6). Apesar das implicações do atordoamento no tratamento do carcinoma diferenciado da tireóide, o seu estudo experimental é limitado. Os dados existentes são baseados na prática clínica, comparando-se a captação de iodo-131 nos estudos diagnósticos com a captação durante o tratamento. Um modelo experimental poderia permitir a melhor caracterização do atordoamento, por exemplo, quanto a sua evolução temporal e correlação entre dose equivalente e redução da captação. Os autores, neste trabalho, tentaram estabelecer um protocolo experimental de atordoamento tireoidiano actínico, avaliando a captação tireoidiana de iodo-131 por 26 dias após sua irradiação. A dose equivalente na tireóide dos camundongos, obtida pela administração de iodo-123, foi similar à de um estudo diagnóstico com 185 MBq de iodo-131.
MATERIAL E MÉTODOS Irradiação dos camundongos Estimou-se, inicialmente, a dose equivalente (D) resultante da administração de 185 MBq em um paciente hipotético, apresentando captação, em 24 horas, de 1% do iodo-131 por grama de tecido tireoidiano, com tempo de decaimento (T½) efetivo de seis dias. A dose absorvida foi calculada pela fórmula de Quimby-Marinelli(7):
A conversão da dose absorvida (Gray) para dose equivalente (Sievert) foi feita diretamente, com fator de ponderação para a radiação b = 1. A dose equivalente no tecido tireoidiano (D) foi utilizada como referência para calcular a atividade de iodo-123 a ser administrada aos camundongos, a partir dos dados comparativos de dosimetria entre diferentes isótopos e espécies animais(8). O iodo-123 utilizado (IEN/RJ) apresenta pureza radionuclídica acima de 99%. No total, 63 camundongos Swiss com oito a dez semanas de idade e peso médio de 39,3 ± 4,3 g foram irradiados, recebendo a mesma dose equivalente D. Os animais foram mantidos com ração específica para camundongos, contendo 2 mg de iodo por quilo. Medidas de captação A captação foi analisada em lotes de nove animais, 2, 3, 5, 7, 12 e 26 dias após a irradiação. Também se mediu a captação, pela mesma técnica, em grupo controle de nove camundongos com as mesmas características de idade e peso, não irradiados previamente. Cada animal recebeu 2,22 kBq (60 nCi) de iodo-131 na cauda, por via intravenosa. As contagens administradas foram calculadas pela diferença entre as contagens na seringa pré e pós-administração, medidas em contador de poço (Gamma Nuclear NZ-138) durante 20 segundos, com janela de 15% no fotopico de 364 keV. Os animais foram sacrificados por luxação cervical, 24 horas após a administração do iodo-131. A região cervical foi dissecada e a cauda cortada, e medida a atividade de ambas em contador de poço durante 20 segundos. As contagens da cauda (extravasamento) foram subtraídas das contagens administradas e a captação foi calculada pela relação entre as contagens cervicais e as contagens administradas. Variação da captação A média e desvio-padrão da captação no tempo 0 (grupo controle) e em cada intervalo após a irradiação foi representada em gráfico "captação × tempo". Foram calculados os intervalos de confiança para as medidas de cada grupo e a captação nos diferentes intervalos foi comparada à captação do grupo controle, utilizando a prova de Kruskal-Wallis (Anova não-paramétrica).
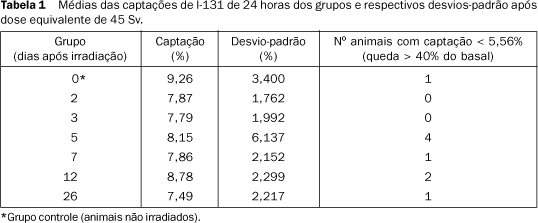
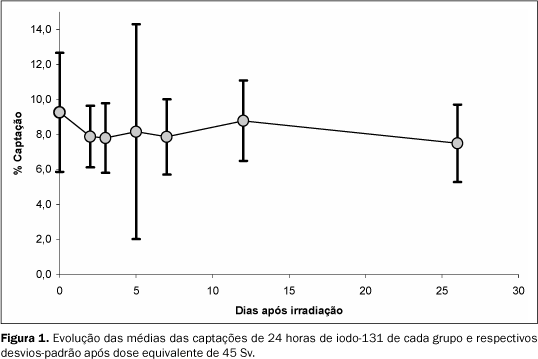
RESULTADOS A dose equivalente no tecido tireoidiano (D), estimada pela fórmula de Marinelli, foi de 45 Sv. Este valor foi obtido considerando-se que o paciente receba 185 MBq (5 mCi) de iodo-131 e apresente tecido tireoidiano com captação de 1%/g. Os camundongos receberam a dose equivalente D (45 Sv) mediante administração de 7,4 MBq (0,2 mCi) de iodo-123. A captação média nos camundongos do grupo controle, medida 24 horas após administração de 2,22 kBq (60 nCi) de iodo-131, foi de 9,26% (desvio-padrão = 3,4%). A captação do primeiro dia após a irradiação não foi considerada, devido à acentuada interferência do iodo-123 nas leituras do contador de poço. Os valores médios de captação obtidos nos intervalos de 2, 3, 5, 7, 12 e 26 dias após a irradiação e respectivos desvios-padrão estão demonstrados na Tabela 1 e Figura 1.
A distribuição das medidas de captação dos camundongos nos grupos foi normal, exceto no grupo 5. Observou-se aumento do desvio padrão nas medidas efetuadas cinco dias após a irradiação (grupo 5), quando quatro animais apresentavam captação menor que 5,56% (queda maior que 40% da média das captações do grupo controle). A diferença entre os intervalos de confiança para as medidas de captação de cada grupo não foi estatisticamente significativa e a prova de Kruskal-Wallis não demonstrou diferença estatisticamente significativa entre as distribuições das medidas de captação dos grupos.
DISCUSSÃO A possibilidade de redução da captação após doses diagnósticas de iodo-131 tem levado à modificação dos protocolos de tratamento, incluindo mesmo a não realização da PCI pré-dose terapêutica. No entanto, apesar de sua repercussão na prática clínica, vários aspectos do atordoamento são mal caracterizados, incluindo a sua evolução temporal. Outra explicação para a queda de captação, quando comparada a estudos diagnósticos, seria o efeito agudo da própria dose terapêutica, com destruição tecidual e liberação do iodo organificado(9). No entanto, esta explicação não é satisfatória, pois diversos estudos demonstram diferença de comportamento entre pacientes que realizaram PCI com altas e baixas atividades, seguida de idêntica dose ablativa. O atordoamento dos remanescentes parece ser dose-relacionado, reduzindo-se o sucesso da dose ablativa de 100% para apenas 37%, quando, em vez de 37 MBq (1 mCi), o estudo diagnóstico foi realizado com 370 MBq (10 mCi)(10). Similarmente, Muratet et al.(4) relatam sucesso de 76% na ablação após PCI com 37 MBq (1 mCi) e de 50% após PCI com 110 MBq (3 mCi), com piores resultados em pacientes com tireoidite crônica. Park et al.(2,3) também descrevem redução da captação nas imagens pós-dose terapêutica em relação à PCI em 40% dos indivíduos que receberam 110 MBq (3 mCi), em 67% dos que receberam 185 MBq (5 mCi) e em 89% dos que receberam 370 MBq (10 mCi). O atordoamento parece ser pouco significativo após o uso de 74 MBq (2 mCi) de iodo-131(11). O tempo de instalação do atordoamento ou se este é transitório são dados pouco conhecidos. A queda da captação é em geral descrita após intervalo de uma a quatro semanas(1,4,5,11). Uma das limitações dos estudos clínicos é que a maioria deles se baseia na descrição visual e qualitativa da redução da captação. Poucos autores realizaram avaliação quantitativa da captação. Leger et al.(5) constataram queda da captação, de 3,76% para 1,97%, após realizarem PCI com 185 MBq (5 mCi) de iodo-131, apesar de não terem a comprovação de níveis similares de TSH nos dois estudos. Huic et al.(12) realizaram também estudo quantitativo após PCI com dose de 74 MBq (2 mCi) em 24 pacientes, evidenciando queda significativa da captação após dose ablativa de 4,4 GBq (120 mCi). O modelo experimental de atordoamento é difícil de ser estabelecido. A administração de iodo-131 para provocar o atordoamento prejudica qualquer medida de captação posteriormente realizada com o mesmo isótopo. A meia vida de oito dias faz com que a atividade residual de iodo-131 dificulte a determinação da captação com uma segunda dose de iodo-131 inferior à primeira, mesmo com técnicas de subtração. Por outro lado, se a segunda dose de iodo-131 for semelhante ou maior que a primeira, torna-se difícil distinguir entre uma redução de captação por efeito da primeira dose (atordoamento) ou pela reação tecidual à segunda dose, levando a uma aceleração do clareamento. A interferência do isótopo administrado para gerar o atordoamento sobre as medidas de captação é eliminada se, em vez do iodo-131, utilizarmos um isótopo de meia vida mais curta ou mesmo a irradiação externa. No caso, escolhemos o iodo-123, com radiação gama de 159 keV e meia vida física de 13 horas, por sua disponibilidade e alta pureza radionuclídica. A radiação gama do iodo-123 (159 keV) também apresenta baixa interferência nas medidas feitas na janela do iodo-131 (364 keV), exceto o primeiro dia pós-irradiação. A dose equivalente decorrente dos 2,22 kBq (60 nCi) de iodo-131 usados na medida de captação foi inferior à empregada para atordoamento, próxima a 0,4 Sv(8). É evidente que a dose equivalente nos animais que receberam iodo-123 é decorrente de radiação g, enquanto, na prática clínica, com o uso de iodo-131, a maior parte da dose se deve à radiação b. Porém, pela própria definição de dose equivalente, o efeito biológico (atordoamento) deveria se dar independentemente de a radiação ser eletromagnética ou particulada. A comparação de dosimetria dos diferentes isótopos de iodo em seres humanos e camundongos foi realizada de forma criteriosa, considerando inclusive aspectos de microdosimetria, no trabalho de VanBest(8) em 1981. O cálculo de dose equivalente após PCI com 5 mCi de iodo-131 (D) considerou uma captação de 1% por grama de tecido(13). Porém, a definição precisa da massa dos remanescentes tireoidianos e, conseqüentemente, da dosimetria, é difícil, em particular quando eles têm pequenas dimensões. Nos resultados apresentados neste trabalho não se evidenciou redução significativa da captação até 26 dias após a dose equivalente de 45 Sv no tecido tireoidiano. O atordoamento não pôde, portanto, ser previsto ou ter o seu comportamento temporal predito nestas condições. Uma possível explicação para este resultado seria a variação da radiossensibilidade interespécies, com menor resposta da tireóide dos camundongos. O atordoamento verificado nos estudos clínicos também pode se dever à variação de radiossensibilidade e dosimetria entre os pacientes. Dentre as características individuais dos pacientes que estão associadas a maior chance de atordoamento destaca-se a tireoidite crônica(4). A variação de radiossensibilidade entre os animais poderia ser também uma explicação para a maior variância das medidas feitas após cinco dias.
CONCLUSÕES Não houve queda sistemática da captação nos camundongos submetidos a dose equivalente de 45 Sv, notando-se tendência a maior flutuação na captação cinco dias após a irradiação. Estes achados podem ser decorrentes de diferenças interespécies ou podem indicar que o atordoamento com doses nesta faixa dependa de características individuais ou anormalidades funcionais prévias que se somam ao efeito da radiação.
REFERÊNCIAS 1.Jeevanram RK, Shah DH, Sharma SM, Ganatra RD. Influence of initial large dose on subsequent uptake of therapeutic radioiodine in thyroid cancer patients. Int J Rad Appl Instrum B 1986;13: 277¾9. [ ] 2.Park HM, Park YH, Zhou XH. Detection of thyroid remnant/metastasis without stunning: anongoing dilemma. Thyroid 1997;7:277¾80. [ ] 3.Park HM, Perkins OW, Edmonson JW, Schnute RB, Manatunga A. Influence of diagnostic radioiodines on the uptake of ablative dose of iodine-131. Thyroid 1994;4:49¾54. [ ] 4.Muratet JP, Daver A, Minier JF, Larra F. Influence of scanning doses of iodine-131 on subsequent first ablative treatment outcome in patients operated on for differentiated thyroid carcinoma. J Nucl Med 1998;39:1546¾50. [ ] 5.Leger FA, Izembart M, Dagousset F, et al. Decreased uptake of therapeutic doses of iodine-131 after 185-MBq iodine-131 diagnostic imaging for thyroid remnants in differentiated thyroid carcinoma. Eur J Nucl Med 1998;25:242¾6. [ ] 6.Reynolds JC, Robbins J. The changing role of radioiodine in the management of differentiated thyroid cancer. Semin Nucl Med 1997;27:152¾64. [ ] 7.Silver S. Radioactive nuclides in medicine and biology. Philadelphia: Lea & Febiger, 1968. [ ] 8.Van Best JA. Dose calculations for 123I, 124I, 125I and 131I in the thyroid gland of the mouse, rat and man and comparison with thyroid function for mice and rats. Phys Med Biol 1981;26:1035¾53. [ ] 9.Hurley JR, Becker DV. The use of radioiodine in the management of thyroid cancer. In: Freeman LM, Weissman HS, eds. Nuclear medicine annual. New York: Raven, 1983:329¾84. [ ] 10.Kim CK, Tse K, SanPedro E, et al. Influence of various scanning doses on subsequent I-131 ablation of thyroid remnants. J Nucl Med 1994;35:14. [ ] 11.McDougall IR. 74 MBq radioiodine 131I does not prevent uptake of therapeutic doses of 131I (i.e. it does not cause stunning) in differentiated thyroid cancer. Nucl Med Commun 1997;18: 505¾12. [ ] 12.Huic D, Medvedec M, Dodig D, et al. Radioiodine uptake in thyroid cancer patients after diagnostic application of low-dose 131I. Nucl Med Commun 1996;17:839¾42. [ ] 13.Schlumberger M, Parmentier C, Vathaire F. 131-I and external radiation in the treatment of local and metastatic thyroid cancer. In: Falk SA, ed. Thyroid disease: endocrinology, surgery, nuclear medicine and radiotherapy. New York: Raven, 1990. [ ]
* Trabalho realizado no Centro de Medicina Nuclear do Departamento de Radiologia da Faculdade de Medicina da Universidade de São Paulo (FMUSP), São Paulo, SP. |
|
Av. Paulista, 37 - 7° andar - Conj. 71 - CEP 01311-902 - São Paulo - SP - Brazil - Phone: (11) 3372-4544 - Fax: (11) 3372-4554