Radiologia Brasileira - Publicação Científica Oficial do Colégio Brasileiro de Radiologia
AMB - Associação Médica Brasileira CNA - Comissão Nacional de Acreditação
 Vol. 34 nº 5 - Set. / Out. of 2001
Vol. 34 nº 5 - Set. / Out. of 2001
|
RELATO DE CASO
|
|
|
|
|
Autho(rs): Antonio Carlos Andersson Westphalen, José Hamilton Pinheiro Ferreira, Alexander Welaussen Daudt, Ana Maria Gaiger |
|
|
Descritores: Tumor de pequenas células desmoplásico, Tumor desmoplásico |
|
|
Resumo:
INTRODUÇÃO O tumor de pequenas células redondas desmoplásico intra-abdominal (TPCRDI) é uma entidade relativamente recente, descrita em 1987 por Sesterhenn et al.(1) e em 1989 por Gerald e Rosai(2), caracterizada pela ocorrência em pacientes na infância e adolescência, predominantemente do sexo masculino, e pela co-expressão de elementos derivados de todos os tecidos embrionários(3). É uma neoplasia agressiva, com curso progressivo e sobrevida média de 17 a 25 meses, que se apresenta como volumosa massa abdominopélvica e múltiplos implantes peritoneais, sem origem visceral identificada(4¾7). A revisão da literatura nacional localizou apenas dois casos anteriormente relatados(4,5). O presente artigo descreve os achados cirúrgicos, de ultra-sonografia (US), tomografia computadorizada (TC) e ressonância magnética (RM), assim como aqueles do estudo de macroscopia, microscopia e imuno-histoquímica de um caso de TPCRDI.
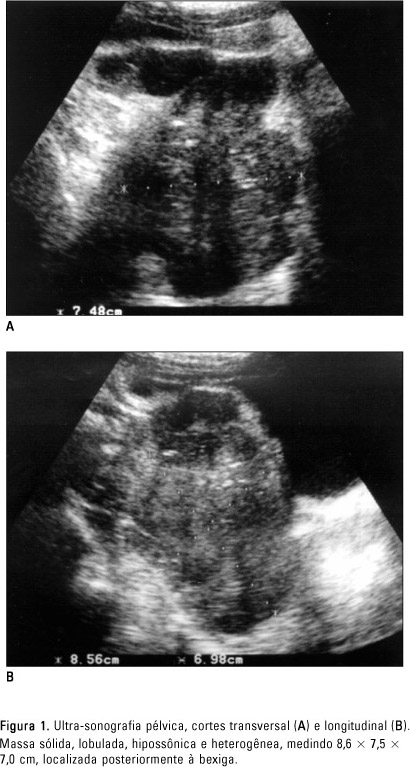
RELATO DO CASO Paciente do sexo masculino, 21 anos de idade, negro, estudante, natural e procedente de Porto Alegre, RS. Em agosto de 1999, o paciente foi atendido com quadro de dor abdominal, trombose do membro inferior direito e perda da função renal, de causa obstrutiva, necessitando de nefrostomia bilateral. No exame físico foi constatada presença de massa fixa no quadrante inferior esquerdo, medindo cerca de 15,0 cm no maior eixo. A investigação inicial demonstrou volumosa lesão pélvica, sólida, bocelada, com possíveis áreas císticas internas, situada posteriormente à bexiga, causando obstrução do fluxo ureteral e englobamento do reto. Ao estudo ultra-sonográfico a lesão se mostrou bocelada, com contornos bem definidos, hipossônica, porém heterogênea, não tendo sido observadas áreas líquidas ou calcificadas no seu interior (Figura 1).
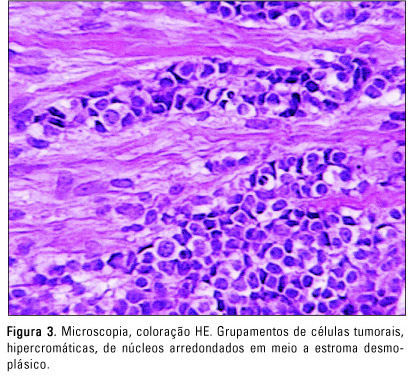
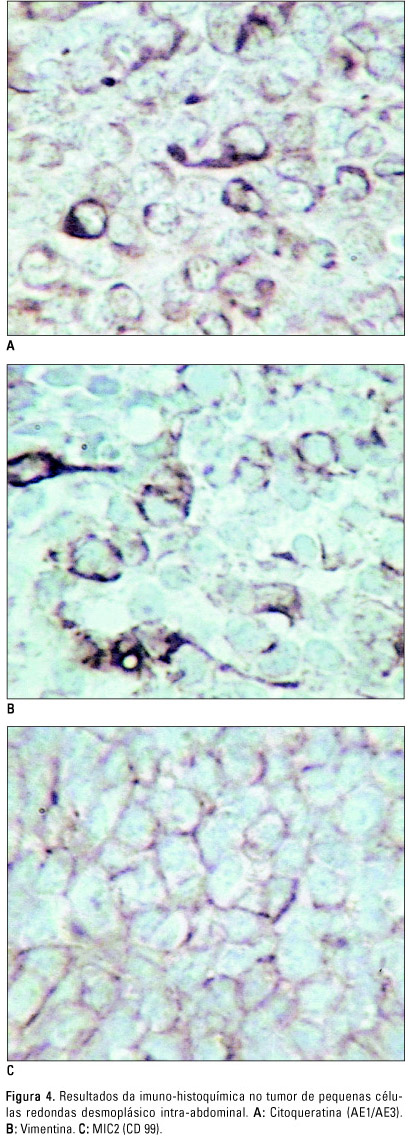
Na TC foi identificada massa de tecidos moles, com contornos bocelados e definidos, heterogênea, com possíveis áreas císticas no seu interior. A lesão impregnou-se moderada e heterogeneamente após a administração endovenosa de meio de contraste iodado (Figura 2). Em ambos os exames foram descritas imagens nodulares compatíveis com adenomegalias intra e retroperitoneais. A radiografia simples da pelve não evidenciou lesão óssea. Foi realizada a laparotomia, na qual se observou grande massa abdominopélvica causando obstrução ureteral à direita, obstrução da veia ilíaca direita e oclusão parcial do reto. Associados a essa volumosa lesão, foram identificados vários nódulos menores disseminados na pelve e no meso intestinal. Devido ao grande volume do tumor, foi apenas obtido material para o diagnóstico anatomopatológico. O estudo microscópico com coloração hematoxilina-eosina (HE) demonstrou ilhotas de células tumorais hipercromáticas, com núcleos arredondados, nucléolos pouco visíveis e citoplasma escasso, bem delimitadas por abundante estroma fibroso (Figura 3). A avaliação imuno-histoquímica (Figura 4) foi positiva para AE1/AE3 (panqueratina) ¾ marcador epitelial; vimentina e actina de músculo liso ¾ marcadores mesenquimais; além de NSE e MIC2 ¾ marcadores neuroectodérmicos. Esses resultados, associados às manifestações clínico-radiológicas, estabeleceram o diagnóstico de tumor de pequenas células redondas desmoplásico intra-abdominal.
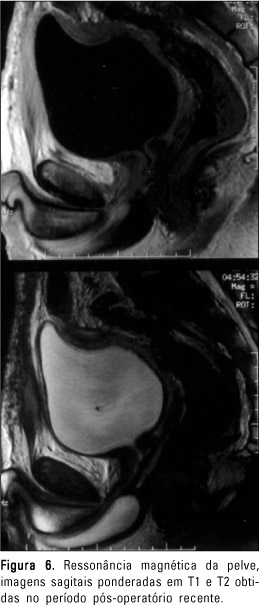
O paciente foi encaminhado para tratamento quimioterápico, tendo recebido um curso com ciclofosfamida, doxorrubicina e vincristina, ao qual apresentou severa toxicidade hematológica. Recebeu alta com resolução completa da trombose ilíaco-femoral direita e melhora da função renal, com fechamento da nefrostomia. Seguiram-se dois cursos de etoposide e ifofosfamida. Um estudo de RM (Figura 5), realizado em março de 2000, durante o período de tratamento quimioterápico, mostrou uma lesão sólida, lobulada, hipointensa e homogênea em T1 e hiperintensa, heterogênea, com definidas áreas císticas em T2. Após a administração endovenosa de gadolínio-DTPA houve nítida impregnação, de forma ligeiramente heterogênea, que persistiu, menos intensamente, em aquisições tardias. Foi possível a determinação de plano de clivagem com a bexiga e o reto, mas não com a próstata. Em maio de 2000, uma vez obtida redução de 50% no volume tumoral e estabilidade após dois novos ciclos, o paciente foi submetido a novo procedimento cirúrgico, que identificou massa tumoral situada junto da implantação do mesocólon sigmóide, estendendo-se à pelve, entre a bexiga, anteriormente, e o reto, posteriormente, quase que envolvendo este último completamente. O assoalho pélvico foi descrito como a origem do tumor. Além dessa lesão, foram observados diversos outros nódulos de tamanho variado na pelve sobre os vasos ilíacos direitos, aderidos ao ureter esquerdo, junto da base do ceco e apêndice cecal e do mesentério do jejuno médio. Foi realizada ressecção da tumoração maior, de todos os nódulos visíveis na pelve, do apêndice cecal e de dois nódulos aderidos ao meso do jejuno. A localização da massa principal foi marcada com clipes metálicos.
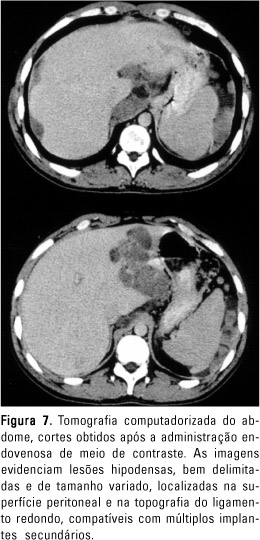
Ao exame patológico macroscópico foi observada massa ovóide, multibocelada, de tecido pardo e elástico, medindo 14,0 × 8,5 × 4,0 cm e pesando 353 g. Aos cortes a lesão mostrou-se cinza-amarelada e brilhante, com áreas císticas de necrose. O paciente teve alta hospitalar após duas semanas e manteve acompanhamento ambulatorial. No período de julho a agosto de 2000 realizou um curso de radioterapia, constituído de 5.580 cGy em 31 frações, com boa tolerância. Em outubro de 2000, exames de controle identificaram implantes peritoneais secundários difusos, mais proeminentes ao redor do contorno hepático e junto do ligamento redondo. O paciente permanece em acompanhamento clínico e iniciará novo ciclo quimioterápico com protocolo a ser estabelecido.
DISCUSSÃO O TPCRDI é entidade relativamente recente, descrita pela primeira vez em 1987 por Sesterhenn et al.(1) e por Gerald e Rosai em 1989(2). Vários outros casos foram posteriormente descritos na literatura internacional; entretanto, a revisão da casuística brasileira só localizou dois relatos anteriores(4,5). A neoplasia acomete principalmente pacientes jovens, com média de idade de aproximadamente 19 anos, tendo, entretanto, sido relatados casos dos cinco aos 68 anos de idade(2,3,6,8). Os indivíduos são predominantemente do sexo masculino, numa proporção de 4:1.
Na maioria dos casos os pacientes referem dor abdominal e apresentam massa palpável no exame físico. Os achados clínicos são bastante variados, tendo sido relatada uma gama de sintomas gastrointestinais e genitourinários, incluindo náuseas, vômitos, constipação, obstrução intestinal, hérnias, obstrução ureteral, incontinência urinária, impotência, entre outros. Também é identificada sintomatologia relacionada a eventuais metástases a distância, para órgãos como o fígado, os pulmões e as cadeias ganglionares(3,4,6,9). No caso presentemente descrito foi diagnosticada trombose venosa do membro inferior direito, em decorrência da compressão da veia ilíaca, associada a hidronefrose com perda da função renal e dor abdominal. Na laparotomia exploradora o achado mais freqüente é uma grande massa abdominopélvica acompanhada de múltiplos implantes peritoneais, sem um órgão primariamente acometido(4¾8). Os tumores são predominantemente intraperitoneais, em situação paravesical e omental (67% dos casos)(6). Existem relatos de tumores no retroperitônio, túnica vaginalis, pleura e sistema nervoso central(9¾12). A ascite também é observada em alguns casos. Macroscopicamente, o tumor caracteriza-se por ser massa de tecido firme e elástico, bocelada, que aos cortes tem cor que oscila entre o amarelo-acinzentado e o pardo, podendo apresentar focos internos de hemorragia ou necrose. Em alguns poucos casos foram identificadas áreas de calcificação. Seu tamanho pode variar amplamente, desde 2,0 até 15,0 cm de diâmetro(3,6). Histologicamente, é típica a formação de agregados de células tumorais hipercromáticas, redondas, entremeadas em denso estroma fibroso desmoplásico. Geralmente o citoplasma é escasso, com núcleo arredondado ou elipsóide ocupando a quase totalidade da célula. O nucléolo é pouco visível. Além dos achados macroscópicos e histológicos, o fator diagnóstico mais importante é a expressão por imuno-histoquímica de uma combinação de marcadores para tecidos de origem epitelial, mesenquimal e neuroectodérmica, concomitantemente. Apesar de o TPCRDI ser reconhecido como entidade nosológica com características clínicas, morfológicas e citogenéticas próprias, sua histogênese permanece desconhecida. Especula-se uma origem a partir de células mesoteliais ou submesoteliais, teoria sustentada pela distribuição predominantemente peritoneal e eventual ocorrência na pleura e túnica vaginalis(3,13). Não existem características imagenológicas específicas para o diagnóstico do TPCRDI. O achado mais característico é o de uma massa tumoral, intraperitoneal, sem a identificação de um órgão sede, associada a múltiplos implantes peritoneais(5¾7). Em um dos poucos estudos realizados visando à determinação dos parâmetros diagnósticos pelos métodos de imagem, foram descritas áreas de hipoatenuação na TC, em 78% dos casos, resultado de focos de necrose e hemorragia, impregnação moderada pelo meio de contraste endovenoso e calcificações em 22% dos tumores(6). Ao exame de US as lesões mostram-se hipossônicas e bem delimitadas. Apenas um trabalho descreve os achados na RM(7), relacionando focos de hipointensidade em T1 e hiperintensidade em T2 a áreas de necrose, bem como focos hiperintensos em T1 a hemorragias focais. O caso relatado mostrou alterações semelhantes às descritas para os exames de US e TC. No estudo por RM foi identificada lesão sólida, lobulada, hipointensa e homogênea em T1 e hiperintensa, heterogênea, com definidas áreas císticas em T2, relacionadas a focos de necrose. Não foi identificada nenhuma área sugestiva de sangramento intralesional, como foi confirmado no exame patológico. Após a administração endovenosa do meio de contraste paramagnético, ocorreu impregnação ligeiramente heterogênea. A utilização do método também foi útil na determinação de planos de clivagem para o planejamento cirúrgico. Existem relatos de tentativa de utilização de métodos cintilográficos para um diagnóstico mais específico do TPCRDI(14). Não existem protocolos de tratamento oncológico definitivamente estabelecidos. Geralmente são realizados cursos de quimioterapia com múltiplas drogas, obtendo-se tão somente respostas parciais. Eventualmente, é associada a radioterapia adjuvante. O tratamento cirúrgico caracteriza-se pela ressecção paliativa da maior quantidade possível de massa tumoral, visando, principalmente, à resolução das manifestações associadas (por exemplo, obstruções do trato gastrointestinal)(15,16). A recidiva é freqüente, mesmo nos casos de ressecção macroscópica completa, e se caracteriza por implantes peritoneais múltiplos, metástases para as cadeias ganglionares locais, ascite e, menos freqüentemente, metástases a distância. A doença tem curso progressivo e fatal, com sobrevida máxima de aproximadamente 24 meses.
REFERÊNCIAS 1. Sesterhenn I, Davis CJ, Mostofi FK. Undifferentiated malignant epithelial tumors involving serosal surfaces of scrotum and abdomen in young males. J Urol 1987;137(suppl.):214. [ ] 2. Gerald WL, Rosai J. Desmoplastic small round cell tumor with divergent differentiation. Pediatr Pathol 1989;9:177¾83. [ ] 3. Ordoñez NG. Desmoplastic small round cell tumor. I: a histopathologic study of 39 cases with emphasis on unusual histological patterns. Am J Surg Pathol 1998;22:1303¾13. [ ] 4. Pereira EM, Maeda AS, Domingues MA, et al. Tumor de pequenas células intra-abdominal desmoplásico com diferenciação divergente. Relato de caso e revisão da literatura. Rev Bras Cancerol 1993;39:61¾3. [ ] 5. Santos LV, Siciliano AAO, D'Annunciação GE, Nunes VCSR, Marchiori E. Tumor de pequenas células desmoplásico intra-abdominal ¾ relato de um caso. Rev Imagem 1999;21:77¾80. [ ] 6. Pickhardt PJ, Fisher AJ, Balfe DM, Dehner LP, Huettner PC. Desmoplastic small round cell tumor of the abdomen: radiologic-histopathologic correlation. Radiology 1999;210:633¾8. [ ] 7. Outwater E, Schiebler ML, Brooks JJ. Intraabdominal desmoplastic small cell tumor: CT and MR findings. J Comput Assist Tomogr 1992;16:429¾32. [ ] 8. Reich O, Justus J, Tamussino KF. Intra-abdominal desmoplastic small round cell tumor in a 68-year-old female. Eur J Gynaecol Oncol 2000;21:126¾7. [ ] 9. Cummings OW, Ulbright TM, Young RH, Del Tos AP, Fletcher CDM, Hull MT. Desmoplastic small round cell tumors of the paratesticular region: a report of six cases. Am J Surg Pathol 1997;21:219¾25. [ ] 10. Roganovich J, Bisogno G, Cecchetto G, D'Amore ES, Carli M. Paratesticular desmoplastic small round cell tumor: case report and review of the literature. J Surg Oncol 1999;71:269¾72. [ ] 11. Parkash V, Gerald WL, Parma A, Miettinen M, Rosai J. Desmoplastic small round cell tumor of the pleura. Am J Surg Pathol 1995;19:659¾65. [ ] 12. Tison V, Cerasoli S, Morigi F, Ladanyi M, Gerald WL, Rosai J. Intracranial desmoplastic small-cell tumor: report of a case. Am J Surg Pathol 1996;20: 112¾7. [ ] 13. Ordoñez NG. Desmoplastic small round cell tumor. II: an ultrastructural and immunohistochemical study with emphasis on new immunohistochemical markers. Am J Surg Pathol 1998;22:1314¾27. [ ] 14. Pickhardt PJ. F-18 fluorodeoxyglucose positron emission tomographic imaging in desmoplastic small round cell tumor of the abdomen. Clin Nucl Med 1999;24:693¾4. [ ] 15. Kurre P, Felgenhauer JL, Miser JS, Patterson K, Hawkins DS. Successful dose-intensive treatment of desmoplastic small round cell tumor in three children. J Pediatr Hematol Oncol 2000;22:446¾50. [ ] 16. Kretschmar CS, Colbach C, Bhan I, Crombleholme TM. Desmoplastic small cell tumor: a report of three cases and a review of the literature. J Pediatr Hematol Oncol 1996;18:293¾8. [ ]
* Trabalho realizado no Moinhos Centro de Imagem, Hospital Moinhos de Vento, Porto Alegre, RS. |
|
Av. Paulista, 37 - 7° andar - Conj. 71 - CEP 01311-902 - São Paulo - SP - Brazil - Phone: (11) 3372-4544 - Fax: (11) 3372-4554