Radiologia Brasileira - Publicação Científica Oficial do Colégio Brasileiro de Radiologia
AMB - Associação Médica Brasileira CNA - Comissão Nacional de Acreditação
 Vol. 34 nº 1 - Jan. / Fev. of 2001
Vol. 34 nº 1 - Jan. / Fev. of 2001
|
QUAL O SEU DIAGNÓSTICO?
|
|
|
|
|
Autho(rs): Lauro Cézar Maito Filho, Simone Caetano, João Saldanha, Ana Lúcia Kefalas O. Melo |
|
|
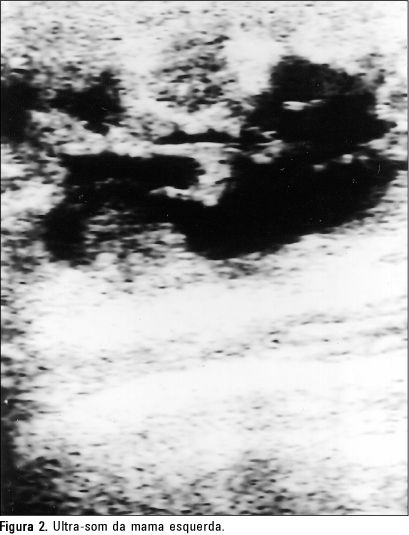
COMENTÁRIOS De acordo com Ibrahim et al.(1), a hiperplasia estromal pseudo-angiomatosa (PASH) é uma entidade clínico-patológica, variando de achados microscópicos incidentais focais até massa clínica e mamograficamente evidente. No estudo de Ibrahim et al.(1), de 200 espécimes de mama avaliados consecutivamente, 46 casos (23%) demonstraram este achado à histologia. Em contraste, a forma tumoral da PASH é rara, com somente 71 casos relatados previamente na literatura(1-6). Na revisão feita por Polger et al.(2), foram analisadas sete pacientes com pseudo-angiomatose de mama biopsiadas: seis pacientes estavam na pré-menopausa e uma estava na pós-menopausa, fazendo terapia de reposição hormonal. As sete pacientes apresentavam massa ou massas visíveis à mamografia, três das quais eram palpáveis. As massas mediam de 1,1 a 11 cm. Em três pacientes as bordas das lesões eram bem circunscritas, em duas eram parcialmente circunscritas e em duas as bordas eram indistintas. Apenas uma das lesões tinha borda lobulada. A característica mamográfica mais comum na PASH foi de massa circunscrita ou parcialmente circunscrita, revelando, ao ultra-som, massa hipoecóica, levemente heterogênea. Em outros estudos, como os de Cohen et al.(3) e Powell et al.(4), mamograficamente as massas com o diagnóstico de PASH são, usualmente, não calcificadas e de aparência bem circunscrita ou parcialmente circunscrita. Bordas obscuras ou indistintas também têm sido descritas. Ao ultra-som, essas massas são vistas como massas sólidas hipoecóicas, levemente heterogêneas, segundo a ecotextura. Um componente cístico foi relatado em um caso, semelhante ao apresentado no presente estudo(2). Uma característica importante da pseudo-angiomatose é que ela apresenta crescimento ao longo do tempo; além disso, pode ocorrer recorrência após biópsia excisional. No entanto, segundo Polger et al.(2), "a pseudo-angiomatose de mama não está associada com malignidade nem é considerada pré-maligna". Em análises histológicas, segundo Vuitch et al.(5), este tumor benigno do estroma mamário tem "característica padrão de miofibroblastos proliferativos que formam fendas". Acredita-se que os miofibroblastos têm reação aberrante aos hormônios (particularmente à progesterona), que começa com acentuada alteração mamária focal, que é fisiológica durante o ciclo menstrual. Fatores hormonais contribuem, provavelmente, para a PASH de mama, já que a idade média das pacientes com esta entidade tem sido relatada como sendo de 40 anos. Segundo Anderson et al.(7), a PASH de mama pode ocorrer em pacientes na pós-menopausa que estejam fazendo terapia de reposição hormonal. O mais importante diagnóstico diferencial considerado pelos patologistas é o angiossarcoma de baixo grau. As células do estroma da pseudo-angiomatose usualmente têm núcleos de aparência benigna, em contraste à aparência altamente atípica das células endoteliais de um angiossarcoma(6). Quanto aos diagnósticos diferenciais clínicos, mamográficos, ultra-sonográficos e histológicos, a PASH de mama também pode ser confundida com o tumor filóide e com o fibroadenoma(6). Quanto ao diagnóstico histológico definitivo, é possível ser realizado por biópsia excisional ou por "core"-biópsia. No estudo de Cohen et al.(3), quatro dos sete casos foram diagnosticados histologicamente através da "core"-biópsia, indicando que, se os achados de imagem forem consistentes com a PASH de mama, a confirmação com biópsia cirúrgica não é necessária. Uma opção é o acompanhamento mamográfico, e se há mais tumor crescendo a biópsia cirúrgica pode então ser feita. É importante que os radiologistas estejam atentos a essa entidade para sugerir o seu diagnóstico. O radiologista também deve estar atento para o fato de que a lesão não é maligna, mas tem propensão para crescer ao longo do tempo e apresentar recorrência local.
REFERÊNCIAS 1. Ibrahim RE, Sciotto CG, Weidner N. Pseudoangiomatous hyperplasia of mammary stroma: some observations regarding its clinicopathologic spectrum. Cancer 1989;63:1154-60. 2. Polger MR, Denison CM, Lester S, Meyer JE. Pseudoangiomatous stromal hyperplasia: mammographic and sonographic appearances. AJR 1996; 166:349-52. 3. Cohen MA, Morris EA, Rosen PP, Dershaw DD, Liberman L, Abramson AF. Pseudoangiomatous stromal hyperplasia: mammographic, sonographic, and clinical patterns. Radiology 1996;198:117-20. 4. Powell CM, Cranor ML, Rosen PP. Pseudoangiomatous stromal hyperplasia (PASH): a mammary stromal tumor with myofibroblastic differentiation. Am J Surg Pathol 1995;19:270-7. 5. Vuitch MF, Rosen PP, Erlandson RA. Pseudoangiomatous hyperplasia of mammary stroma. Hum Pathol 1986;17:185-91. 6. Cyrlak D, Carpenter PM. Breast imaging case of the day. Pseudoangiomatous stromal hyperplasia. RadioGraphics 1999;19:1086-8. 7. Anderson C, Ricci A Jr, Pedersen CA, Cartun RW. Immunocytochemical analysis of estrogen and progesterone receptors in benign stromal lesions of the breast: evidence for hormonal etiology in pseudoangiomatous hyperplasia of mammary stroma. Am J Surg Pathol 1991;15:145-9.
1. Acadêmico de Medicina do VIII Período da Faculdade de Medicina do Triângulo Mineiro (FMTM), Uberaba, MG. |
|
Av. Paulista, 37 - 7° andar - Conj. 71 - CEP 01311-902 - São Paulo - SP - Brazil - Phone: (11) 3372-4544 - Fax: (11) 3372-4554