Radiologia Brasileira - Publicação Científica Oficial do Colégio Brasileiro de Radiologia
AMB - Associação Médica Brasileira CNA - Comissão Nacional de Acreditação
 Vol. 39 nº 6 - Nov. / Dez. of 2006
Vol. 39 nº 6 - Nov. / Dez. of 2006
|
ARTIGO ORIGINAL
|
|
|
|
|
Autho(rs): Néstor Hugo Kisilevzky |
|
|
Descritores: Hipertensão portal, Cirrose, TIPS, Sangramento por varizes esofagianas, Ascite |
|
|
Resumo:
INTRODUÇÃO TIPS (transjugular intrahepatic portosystemic shunt) é um procedimento radiológico percutâneo que consiste em estabelecer uma comunicação intra-hepática entre um ramo da veia porta e a veia cava inferior com intuito de descomprimir a veia porta e controlar, assim, as complicações clínicas provocadas pela elevação da pressão portal em pacientes com hepatopatia crônica. Do ponto de vista técnico, o TIPS é considerado um dos procedimentos de radiologia intervencionista mais desafiadores porque combina várias técnicas, como a de angiografia, punção de víscera parenquimatosa, angioplastia, manuseio de stents, embolização, etc. A idéia do TIPS foi inicialmente concebida por radiologistas da Universidade de Oregon, em Portland, EUA, no final dos anos 60, como uma extensão do procedimento de colangiografia transjugular(1,2). Entretanto, a sua aplicação clínica começou a se desenvolver universalmente somente a partir da publicação do primeiro caso em 1989(3). Desde então, a técnica foi refinada, as indicações foram definidas e a sua eficácia foi bem documentada em grandes séries(4–8). O TIPS representa, hoje, a grande contribuição que os radiologistas desenvolveram como uma alternativa minimamente invasiva para o tratamento de pacientes com síndrome de hipertensão portal (HP). Apresenta-se, neste artigo, a experiência realizada por um único operador numa única instituição e discutem-se as indicações e fatores que podem condicionar o resultado do procedimento desde o ponto de vista técnico e clínico.
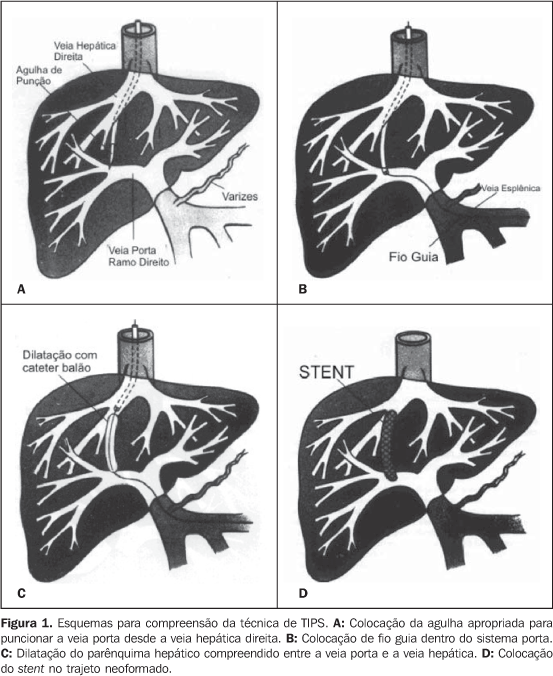
MATERIAIS E MÉTODOS Este foi um estudo retrospectivo descritivo que consistiu na revisão de todos os casos de pacientes submetidos a TIPS numa única Instituição (Hospital Santa Catarina, São Paulo, SP) por um único operador, durante um período de oito anos (1996–2004). Ao todo, 44 pacientes, sendo 30 do sexo masculino e 14 do sexo feminino e com idades entre 34 e 67 anos (média de 52 anos), foram submetidos a TIPS. Todos os pacientes apresentavam hepatopatia crônica e hipertensão portal, tendo como doença de base cirrose alcoólica em 22, hepatite crônica por vírus B em 7, hepatite crônica por vírus C em 4, cirrose autoimune em 1, cirrose biliar em 2 e cirrose criptogênica em 8. O sintoma principal que originou o tratamento da hipertensão portal foi: recidiva hemorrágica por ruptura de varizes esofagogástricas ou gastropatia congestiva em 28 e ascite refratária em 16, sendo que 5 destes últimos apresentavam a síndrome hepatorrenal. Foram verificados os níveis séricos de bilirrubina, albumina, tempo de protrombina e creatinina. Verificou-se que 16 (36,36%) pacientes eram portadores de ascite moderada e outros 16 tinham ascite tensa. Adicionalmente, 11 (25%) pacientes tinham antecedentes de encefalopatia discreta. O estado da função hepática dos pacientes avaliada pela classificação de Child-Pugh(8) revelou que 7 eram Child-Pugh A, 24 eram Child-Pugh B e 11 eram Child-Pugh C. Todos os procedimentos de TIPS foram realizados no Setor de Angiografia do Centro de Diagnóstico por Imagens do Hospital Santa Catarina, que conta com um equipamento para angiografia por subtração digital GE modelo Advantx®. Dos pacientes submetidos a TIPS, 34 encontravam-se hospitalizados na própria Instituição e 9 foram transportados de ambulância desde um outro local para realizar o procedimento e retornaram para o hospital de origem após o procedimento. Em 30 (68,18%) oportunidades o procedimento foi programado com antecedência e ocorreu de forma eletiva, mas em 14 (31,82%) deles o procedimento foi realizado em caráter de urgência (sem programação prévia). Verificou-se que 37 (84,09%) pacientes fizeram o procedimento com anestesia local e sedação consciente endovenosa com um hipnótico (Midazolan) e um analgésico (Fentanil), mas 7 (15,91%) pacientes realizaram o procedimento sob anestesia geral e respiração assistida em virtude de já estarem previamente sob esta condição. A técnica para realização do TIPS obedeceu as seguintes etapas (Figura 1):
Todos os sujeitos foram acompanhados durante a sua permanência hospitalar para verificar a evolução clínica. Consultas aos pacientes ou a seus médicos assistentes foram realizadas durante o primeiro ano após a realização do TIPS. Todos os dados necessários à pesquisa e obtidos da revisão dos prontuários médicos foram anotados em uma ficha pré-codificada especialmente desenhada para este estudo. O preenchimento dessa ficha foi realizado inteiramente pelo pesquisador responsável. Para registrar em meio eletrônico todas as variáveis envolvidas neste estudo foi utilizado o gerenciador de banco de dados Excel. Foram utilizados os programas: The SAS System for Windows (Statistical Analysis System), versão 8.02 (SAS Institute Inc., 1999-2001, Cary, NC, USA); SPSS for Windows, versão 10.0.5 (SPSS Inc., 1989-1999, Chicago, IL, USA). Para análise dos dados foi utilizada a seguinte metodologia estatística:
Para análise dos resultados foram utilizados os seguintes conceitos: Sucesso técnico: Refere-se à viabilidade da colocação de TIPS permitindo a passagem de sangue portal para a circulação sistêmica(8). Sucesso clínico: Refere-se ao controle clínico pós-operatório do sintoma principal que motivou o procedimento. Sucesso hemodinâmico: Refere-se à capacidade do procedimento para reduzir o gradiente pressórico porto-sistêmico. Mortalidade pós-operatória: Refere-se ao número de óbitos ocorridos no período de 30 dias que seguiram ao procedimento. Sobrevida: Refere-se à quantidade de pacientes que permaneceram vivos durante o tempo de observação do estudo. Tempo de censura: Representa o tempo de observação que foi considerado em 12 meses após a realização do procedimento. Complicações: Eventos diretamente relacionados ao procedimento que motivaram o prolongamento da permanência hospitalar ou terapias adicionais. Oclusão do TIPS: Refere-se ao momento no qual se comprovou a ausência de passagem de fluxo portal através do TIPS, esteja ou não acompanhado de sintomas.
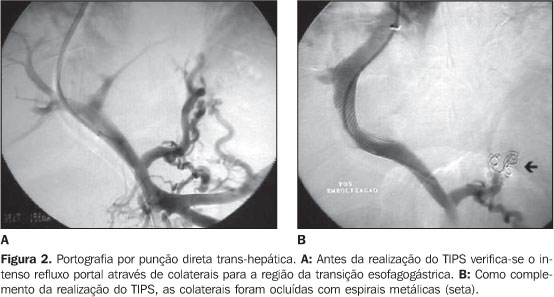
RESULTADOS Sucesso técnico: O procedimento foi realizado tecnicamente com sucesso em todos os casos (100%). Em 11 (25%) oportunidades foi realizada a embolização de colaterais como complemento do procedimento principal (TIPS) (Figura 2).
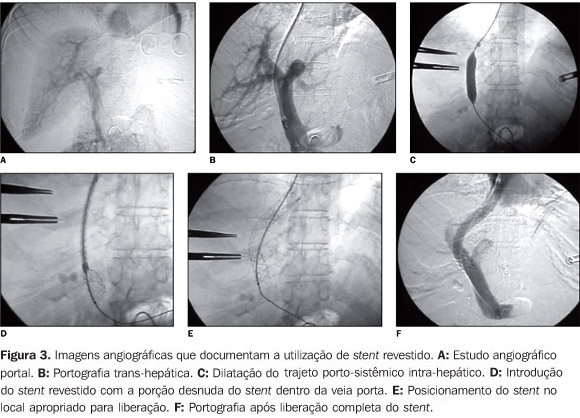
Em 31 (70,45%) oportunidades foram utilizados stents metálicos "desnudos" de várias marcas e em 13 (29,55%) foi utilizado um novo stent metálico recoberto de politetrafluoroetileno (Viatorr®) (Figura 3).
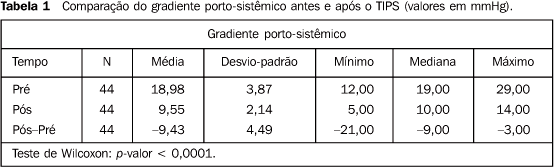
Em um caso (2,27%) foi necessária a colocação de dois stents para realizar TIPS "em paralelo" (Figura 4). Sucesso hemodinâmico: O TIPS provocou mudança nos valores de todas as pressões aferidas em todos os pacientes. Previamente à colocação do TIPS, a média do gradiente pressórico porto-sistêmico, estabelecido pela diferença entre a pressão portal e a pressão venosa central, foi de 18,98 mmHg, e caiu após a colocação de TIPS para uma média de 9,55 mmHg, representando uma queda de 49,69%, que foi estatisticamente significativa (Tabela 1).
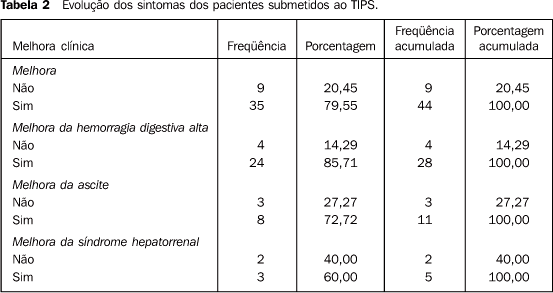
Sucesso clínico: Com relação ao quadro clínico que motivou o procedimento, comprovou-se que em 35 pacientes (79,55%) houve melhora clínica, sendo que dos 28 (63,64%) pacientes nos quais o TIPS foi indicado para tratar sangramento, 24 (85,71%) pararam de sangrar; adicionalmente, verificou-se que entre os 11 pacientes com ascite refratária conseguiu-se controlar a ascite em 8 (72,72%), e 3 (60%) dos 5 pacientes com síndrome hepatorrenal reverteram o quadro após o TIPS (Tabela 2).
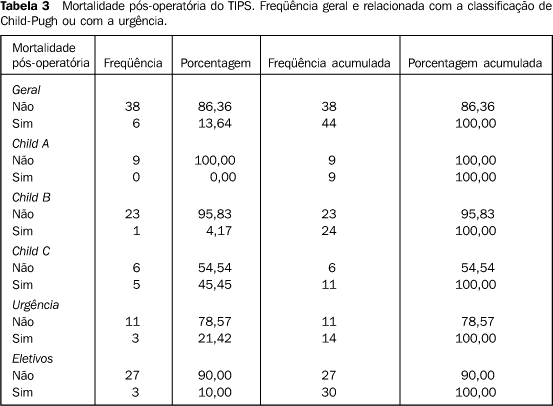
Mortalidade pós-operatória: No acompanhamento pós-operatório de 30 dias comprovou-se a morte de seis pacientes (13,64%), sendo cinco de classe Child-Pugh C e um de classe Child-Pugh B. Uma metade desses procedimentos foi realizada na urgência e a outra metade foram procedimentos eletivos (Tabela 3).
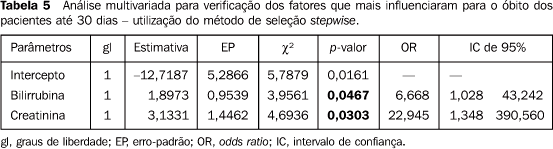
A análise das variáveis que condicionaram a mortalidade pós-operatória por meio de regressão logística evidenciou que a bilirrubina, o tempo de protrombina e o nível de creatinina foram os fatores que influenciaram significativamente (Tabela 4). Já a análise multivariada mostrou que os fatores que influenciaram com naior significância na mortalidade pós-operatória foram a bilirrubina e a creatinina, sendo que pacientes com hiperbilirrubinemia têm chance 6,7 vezes maior de morrer no pós-operatório imediato, enquanto os pacientes com creatinina elevada têm chance 22,9 vezes maior de morrer no pós-operatório imediato (Tabela 5).
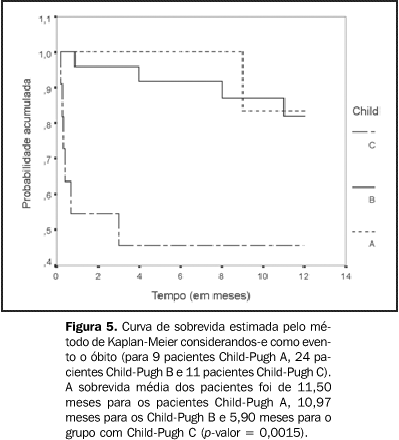
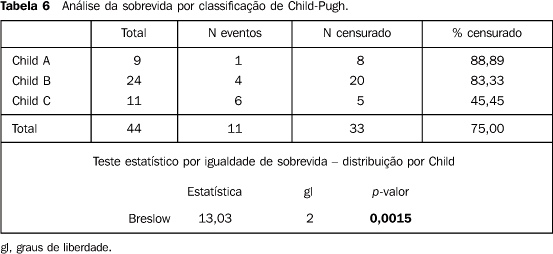
Sobrevida: Trinta e três pacientes (75%) sobreviveram durante o período de censura, sendo 8 de 9 pacientes Child-Pugh A, 20 de 24 Child-Pugh B e somente 5 de 11 Child-Pugh C. Evidenciou-se, assim, diferença estatisticamente significativa na sobrevida dos pacientes relacionada com a classificação de Child-Pugh. A sobrevida média dos pacientes foi de 11,50 meses para os Child-Pugh A, 10,97 meses para os Child-Pugh B e 5,90 meses para o grupo com Child-Pugh C (Figura 5; Tabela 6).
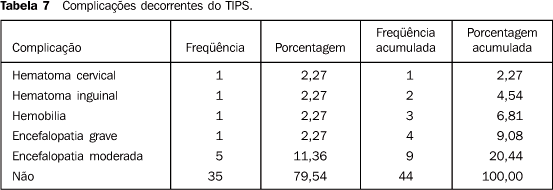
Complicações: Eventos imprevistos imediatos relacionados ao procedimento ocorreram em nove (20,44%) pacientes (Tabela 7).
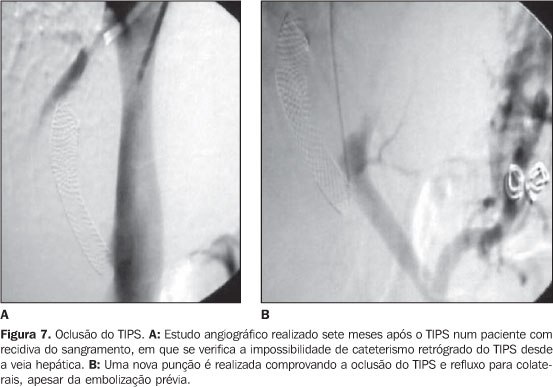
Um paciente desenvolveu hematoma no pescoço e um segundo desenvolveu hematoma na virilha. Ambos os casos foram resolvidos com tratamento clínico. Um paciente apresentou hemobilia no 14º dia pós-operatório, o que motivou nova hospitalização. Foi realizado estudo angiográfico, o qual evidenciou lesão acidental do ramo direito da artéria hepática, que tornou necessária embolização com espirais metálicas para resolução do quadro (Figura 6). Verificou-se que seis pacientes apresentaram encefalopatia, sendo em cinco de magnitude moderada e resolvida com tratamento clínico. Num outro paciente, além da encefalopatia grave, comprovou-se piora substancial da função hepática, que obrigou inicialmente a reduzir o calibre do TIPS e posteriormente a ocluí-lo. Entre os seis pacientes com encefalopatia, quatro (66,66%) tinham cirrose alcoólica como doença de base e antecedente de encefalopatia prévias à colocação do TIPS. Oclusão do TIPS: Comprovou-se oclusão do TIPS em cinco pacientes (11,36%), sendo que em dois deles ocorreu de forma aguda (8 e 20 dias do pós-operatório) e nos outros três, de forma crônica (7, 9 e 11 meses do pós-operatório) (Figura 7).
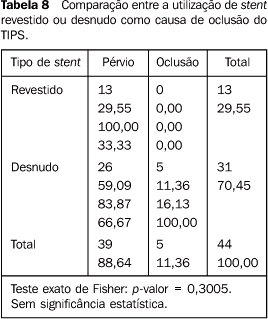
Constatou-se que quatro pacientes foram a óbito em conseqüência de piora ou recidiva dos sintomas. Em um paciente foi realizada revisão do TIPS oito meses após a sua colocação. Na ocasião foi colocado um novo stent, que permitiu boa descompressão portal, prolongando a sobrevida da comunicação e do paciente. Em todos os casos em que houve oclusão do TIPS foram utilizados stents metálicos "desnudos" (não revestidos). Porém, a relação entre oclusão do TIPS e tipo de stent utilizado não foi estatisticamente significativa (Tabela 8).
DISCUSSÃO A radiologia intervencionista é uma disciplina que tem experimentado profunda transformação. O desenvolvimento tecnológico ocorrido nas últimas décadas, tanto nos equipamentos de imagem quanto no material e instrumentos para intervenção, aliado à imaginação de pesquisadores comprometidos com a evolução da medicina tornou possível, nos dias de hoje, a utilização de procedimentos minimamente invasivos para resolver problemas graves. O TIPS é, sem dúvidas, um exemplo dessa evolução. Até o advento do TIPS, milhares de pacientes com hipertensão portal foram a óbito devido à falta de uma terapêutica efetiva, já que, em numerosas situações, nem a endoscópica nem a cirúrgica, constituem opções que possam oferecer um beneficio substancial(7). Na grande maioria das vezes o TIPS é indicado para controlar o sangramento por varizes e/ou ascite refratária(6). Indicações menos comuns incluem o manejo da síndrome de Budd-Chiari(9), o hidrotórax hepático(10), a síndrome hepatopulmonar(11) e varizes ectópicas(12), mas o papel do TIPS nessas situações não tem sido definido com precisão(13). Na experiência relatada neste trabalho houve duas indicações predominantes para a realização do TIPS: 1) hemorragia digestiva alta por ruptura de varizes da região esofagogástrica ou gastropatia congestiva; 2) ascite refratária, sendo que nesta última incluem-se pacientes com síndrome hepatorrenal. A melhora clínica observada em quase 80% dos pacientes permite afirmar que o TIPS é um método eficiente para controlar estas duas situações, principalmente quando comparado com outras alternativas terapêuticas. Os resultados de experiências prévias com descompressões portais cirúrgicas foram desalentadores em conseqüência da alta incidência de mortalidade (31% a 77%), principalmente quando a cirurgia é realizada em caráter de urgência(14). O TIPS mostrou também ser mais eficiente que o tratamento endoscópico para controlar a hemorragia digestiva em pacientes com hipertensão portal. Em 1999, um estudo de meta-análise agrupando 11 artigos comparando TIPS versus terapia endoscópica evidenciou uma menor incidência de recidiva hemorrágica nos pacientes tratados com TIPS(15). Nesses trabalhos verificou-se que a recidiva hemorrágica ocorreu, em média, em 40% a 50% dos pacientes tratados com o método endoscópico e em 15% a 25% dos pacientes tratados com o método percutâneo, isto num período de acompanhamento de 15 a 33 meses. Com relação à ascite refratária, o TIPS tem sido comparado com o tratamento mediante paracenteses repetitivas. Recentemente, um trabalho de meta-análise agrupando cinco artigos e mais de 300 casos foi publicado(16). Entre os pacientes que fizeram TIPS houve melhora sintomática média de 66%, enquanto naqueles tratados com parecentese a melhora foi de somente 24% no acompanhamento de quatro meses. A diferença foi de 55% contra 19% a favor do TIPS no acompanhamento de um ano. Quando se pretende indicar a realização de um TIPS deve-se considerar que há vários fatores que podem causar um impacto negativo na sobrevida pós-operatória. A classificação de Child-Pugh, o nível de bilirrubina, o nível de creatinina, o estado da coagulação ou a indicação em situação de urgência são alguns desses fatores(17). Num estudo multicêntrico nos EUA, observou-se que o TIPS realizado em condições de urgência conseguiu controlar o sangramento em 93,6% dos pacientes e verificou-se recidiva hemorrágica precoce em 12,4% destes. Entretanto, a mortalidade hospitalar até seis semanas foi considerada alta (35,8%)(18). Num outro estudo da França observou-se que em 58 pacientes com sangramento incontrolável que foram submetidos a TIPS de emergência o índice de mortalidade pós-operatória (até 30 dias) foi de 29% e a mortalidade até 60 dias foi de 35%(19). Encarnacion et al., nos EUA, relataram 65 TIPS realizados consecutivamente para controlar sangramento por ruptura de varizes. Nesse estudo, 60% dos pacientes estavam hemodinamicamente instáveis e foram levados ao procedimento em condição emergencial(20). Os autores documentaram claramente que pacientes submetidos a TIPS na urgência têm prognóstico significativamente pior que aqueles que são realizados de forma eletiva. A mortalidade aos 30 dias nos primeiros foi de 28%, ao passo que nos segundos foi de somente 4% (p = 0,013). Na experiência relatada neste artigo não foi encontrada diferença estatisticamente significativa na mortalidade de pacientes submetidos a TIPS quando comparados aos realizados em situação eletiva ou na urgência. Isto pode ocorrer pela diferente interpretação de termos como "urgência" ou "emergência", empregados em serviços e comunidades diferentes. Houve sim, uma evidente diferença na evolução dos pacientes conforme a sua caracterização clínica de acordo com a classificação de Child. Complementarmente, foi observado risco potencialmente maior de mortalidade nos pacientes com aumento da bilirrubina e da creatinina, constituindo-se nos fatores de pior prognóstico após o TIPS. Em geral, a maioria dos autores coincide com a opinião que pacientes Child-Pugh classe C, com pontuação de 12 ou maior, apresentam elevado risco de mortalidade precoce quando submetidos a TIPS(21). Num estudo realizado nos EUA, com 231 pacientes submetidos a TIPS em condições eletivas, foram identificados quatro fatores condicionantes da sobrevida: nível de creatinina sérica, nível de bilirrubina, International Normalized Ratio (INR) e causa da cirrose(22). Os autores desenvolveram uma fórmula para calcular o risco usando essas quarto variáveis e verificaram que pacientes com pontuação maior que 1,8 tinham sobrevida média de 2,8 meses e pacientes com pontuação menor que 1,8 tinham sobrevida média de 1,3 ano. Dessa forma, estabeleceu-se que pontuação maior de 1,8 implicava prognóstico ruim. Os autores acharam este modelo bastante efetivo, com sensibilidade de 77%, especificidade de 79%, valor prognóstico positivo de 63% e valor prognóstico negativo de 88%(22). O modelo original desenvolvido por Malinchoc et al. foi discretamente modificado: pequenas mudanças na fórmula que incluíram a eliminação da causa da cirrose e a multiplicação da pontuação por 10 para facilitar a sua aplicação(23). O novo modelo ficou conhecido como model for end-stage liver disease (MELD) e é hoje aplicado universalmente para a seleção de candidatos para TIPS. TIPS é um procedimento invariavelmente realizado por um radiologista intervencionista, ou seja, um especialista em procedimentos percutâneos minimamente invasivos guiados por métodos de imagem. Em mãos experimentadas o procedimento pode ser completado com sucesso em mais de 95% dos casos(7,8,24,25). Se bem que neste trabalho foi verificado 100% de sucesso técnico para realização do TIPS, deve-se salientar que aqui foi relatada apenas uma experiência parcial do autor, feita numa única instituição em condições ideais e após completada a sua curva de aprendizagem com esse procedimento. O autor tem já realizado mais de 150 procedimentos de TIPS ao longo dos últimos dez anos em várias instituições no Brasil e no exterior e já experimentou alguns insucessos técnicos para realização de TIPS(7). O passo central para a conclusão do TIPS com sucesso é a obtenção da punção portal. Alguns autores têm aventado certos parâmetros anatômicos ou variações técnicas com intuito de facilitar a punção portal(26–29). Todavia, o sucesso para isso resulta imprevisível quando se desconhece o grau de atrofia hepática e de deslocamento das suas estruturas vasculares em um fígado cirrótico. O propósito do TIPS é a descompressão do sistema portal hipertenso e, assim, evitar o sangramento por varizes e/ou parar ou reduzir a formação de ascite. Com relação às varizes, foi bem estabelecido que a redução do gradiente porto-sistêmico até um patamar menor de 12 mmHg faz cair significativamente o risco de sangramento. Outro conceito utilizado é a redução proporcional do gradiente porto-sistêmico. Rossle et al. mostraram que o risco de ressangramento após TIPS foi de 18%, 7% e 1% em pacientes nos quais o gradiente porto-sistêmico tinha sido reduzido em 0%, entre 25% e 50% e em mais de 50%, respectivamente(30). Num outro estudo foi observado que a redução em 50% do gradiente porto-sistêmico inicial está associado a uma taxa de ressangramento ao ano de 11%, sendo que pacientes com redução menor do gradiente tiveram taxa de ressangramento de 31%(31). Nesse último estudo, o único valor absoluto para prevenir o ressangramento foi um gradiente porto-sistêmico menor de 12 mmHg, o que, de alguma forma, equipara ambos os conceitos. Vale salientar que uma redução excessiva do gradiente porto-sistêmico pode se associar com uma maior incidência de encefalopatia pós-TIPS. A Society of Interventional Radiology desenvolveu e publicou, em 2001, normas para a criação de TIPS, e o consenso foi que o sucesso técnico (criação da comunicação e diminuição do gradiente porto-sistêmico a 12 mmHg) deve ser alcançado em 95% dos pacientes e o sucesso clínico (resolução da complicação da hipertensão portal) deve ser alcançado em 90% dos pacientes(8). Um aspecto interessante é a decisão de complementar o TIPS com a embolização de colaterais. Salienta-se que em 25% dos pacientes da nossa experiência isto foi considerado necessário quando se verificou a presença de colaterais de dois tipos: colaterais com fluxo hepatofugal para a região da transição esofagogástrica (veia gástrica esquerda e/ou tributarias) e anastomoses esplenorrenais naturais. Essa decisão se baseia no fato de já termos observado que em casos em que persistem colaterais de calibre considerável após a abertura do TIPS há alta incidência de continuação do sangramento ou de ressangramento precoce, mesmo que o gradiente porto-sistêmico pós-TIPS tenha ficado abaixo de 12 mmHg. Já a embolização de anastomoses porto-sistêmicas naturais obedece à intenção de evitar a competência entre duas comunicações porto-sistêmicas, o que pode levar a trombose e disfunção precoce do TIPS. É importante mencionar que quando se oclui uma via de fuga há geralmente uma mudança na hemodinâmica local e, portanto, o gradiente porto-sistêmico deve ser sempre aferido após o fechamento de colaterais, para evitar que se deixe o sistema portal hipertenso. O TIPS tem mostrado ser um procedimento razoavelmente seguro e com índice de complicações aceitável(32). Na maioria das vezes o óbito após o TIPS ocorre em conseqüência da progressão da doença hepática, situação talvez influenciada pelo desvio do fluxo portal, mas não como conseqüência de uma complicação do procedimento em si, como poderia ser uma perfuração hepática ou portal com hemorragia intraperitoneal. Este tipo de complicação maior estima-se não ser superior a 3%(8,32). Os dois efeitos negativos mais temidos após o TIPS são a encefalopatia e a disfunção do shunt devido a estenose ou oclusão. O elemento central no aparecimento de encefalopatia é a presença de uma comunicação porto-sistêmica e, por definição, o TIPS pode ocasionar esta complicação em até 30% dos pacientes(33,34). Essa complicação, na maioria dos casos, pode ser manejada clinicamente sem dificuldades, mas em cerca de 5% dos casos a encefalopatia pode ser extremamente limitante obrigando uma nova intervenção, que pode consistir na diminuição do calibre do shunt ou na sua oclusão(35–37). A incidência de encefalopatia entre os pacientes da casuística apresentada neste trabalho foi de 25%. Verificamos, porém, que a maioria dos pacientes que apresentaram encefalopatia era portadora de hepatopatia alcoólica ou tinha antecedentes de encefalopatia. Alguns fatores de risco para aparecimento de encefalopatia foram já aventados, como a idade maior de 60 anos, o sexo feminino, a doença alcoólica, a hipoalbuminemia, a existência prévia de encefalopatia, o calibre da comunicação estabelecida, o gradiente pressórico final e a gravidade da doença de base(33,34). Nesses pacientes com elevado risco de apresentar encefalopatia pode ser interessante criar uma comunicação de calibre menor (8 mm) ou até duas em paralelo e completar o procedimento com a embolização de colaterais através do TIPS(38,39). O principal problema do TIPS é a sua curta durabilidade. Em 25% a 50% dos casos observa-se estenose da comunicação maior que 50%, que pode levar à recidiva da hipertensão portal num tempo variável entre 6 e 12 meses após a confecção do TIPS(40–44). Em 1993, LaBerge et al. relataram detalhadamente os achados em pacientes com TIPS estenosados e ocluídos(45). Os autores propuseram que o acumulo de bile em forma de pequenos lagos, produto da fratura de ductos biliares no procedimento de punção portal, provocava uma reação inflamatória que contribuía para a formação de coágulos e oclusão do TIPS(45). Um importante aspecto que deve ser observado por ocasião da realização do TIPS é a boa cobertura da veia hepática com prolongação do stent até o confluente entre a veia hepática e veia cava inferior. Foi observado que a veia hepática reduz o seu calibre em até 50% como resposta ao TIPS e desta forma limita a saída de fluxo que passa pela comunicação, tornando propícia e freqüente a oclusão a este nível(46). Isso foi o que observamos num caso em que se comprovou a oclusão do TIPS sete meses após a sua implantação. Por ocasião do controle angiográfico foi verificado que houve retração e deformidade do stent que fora colocado próximo do parênquima hepático e com pouca cobertura da veia hepática (Figura 7). Muitas pesquisas têm sido conduzidas apontando para vários caminhos, com o intuito de prolongar a permeabilidade do TIPS. A maioria dos investigadores tem concentrado os seus esforços na idéia de utilizar novos stents, recobertos por material prostético impermeável e biocompatível. Assim surgiu o conceito do stent-graft. Uma grande variedade de material prostético foi avaliada para revestir os stents metálicos incluindo silicone, politetrafluoroetileno (PTFE), polietileno tereftalato (PET), dacron, etc. Em 2001, a empresa americana W.L. Gore lançou no mercado um stent revestido especificamente desenvolvido para a criação de TIPS e denominado Viatorr®. Trata-se de um stent de nitinol (liga de níquel e titânio) revestido por dentro e por fora com PTFE, sendo que a coberta externa é revestida com um tipo especial de PTFE expandido e impermeável à bile (ePTFE). Em 2004, Charon et al. fizeram uma análise retrospectiva da utilização do stent Viatorr® na Europa(47). O stent da empresa Gore foi utilizado em 100 pacientes com hipertensão portal submetidos a TIPS. Verificou-se que a permeabilidade primária no primeiro ano de acompanhamento foi de 84%, o que representou uma melhora evidente com relação à permeabilidade histórica do TIPS(47). Rossi et al., usando o mesmo material na Itália, verificaram que uma permeabilidade primária de 84% e secundária de 98% no primeiro ano de acompanhamento(48). Hausegger et al., na Áustria, criaram TIPS usando o stent Viatorr® numa população de 71 pacientes(49). Quatro oclusões e três estenoses foram encontradas durante o primeiro ano de acompanhamento. Isto gerou 11,3% de novas intervenções. A permeabilidade primária após seis meses e um ano foi, respectivamente, de 87,4% e 80,8%. Bureau et al. compararam, num estudo randomizado, a durabilidade do TIPS em dois grupos de pacientes submetidos ao procedimento com stent revestido ou com stent clássico não revestido(50). Observaram que após um período de acompanhamento médio de 300 dias houve 13% de disfunção do TIPS no grupo em que foi usado o stent revestido contra 44% de disfunção naqueles em que foi usado o stent metálico clássico. Na nossa experiência comprovamos a oclusão do TIPS em cinco pacientes, sendo que em todos eles tinha sido utilizado stent metálico clássico não revestido. A partir de 2001, quando ficou disponível no mercado brasileiro, começamos a utilizar o stent Viatorr®. Em nenhum dos 13 casos em que foi usado o stent revestido houve disfunção do TIPS. Entretanto, se bem que isto mostra uma tendência favorável, não foi encontrada diferença estatisticamente significativa em comparação com a utilização de stents não revestidos, o que provavelmente se deve ao número pequenos de pacientes ou ao curto tempo de acompanhamento.
CONCLUSÃO Através do presente trabalho verifica-se que o TIPS constitui um método excelente para diminuir a pressão portal e controlar os sintomas de pacientes com hepatopatia crônica e hipertensão portal. Observou-se, adicionalmente, que a sobrevida dos pacientes que realizam TIPS é aceitável, podendo o método constituir valiosa alternativa para pacientes que aguardam por transplante hepático como terapia definitiva. As complicações decorrentes do procedimento são pouco freqüentes e a mortalidade é aceitável, considerando-se a complexidade clínica dos pacientes. A mortalidade está diretamente influenciada por alguns fatores clínicos, tendo maior impacto nos pacientes caracterizados clinicamente como Child-Pugh classe C, com nível de bilirrubina elevado ou com nível sérico de creatinina aumentado. Estes se constituíram em fatores de pior prognóstico para pacientes que realizaram TIPS. A variação eventual da técnica, com a utilização de stents revestidos, não modificou com significância estatística o resultado, embora foi observado que em nenhum desses pacientes houve oclusão da comunicação, diferentemente daqueles nos quais foram usados stents metálicos clássicos não revestidos.
REFERÊNCIAS 1. Rösch J, Hanafee W, Snow H, Barenfus M, Gray R. Transjugular intrahepatic portocaval shunt. Am J Surg 1971;121:588–592. [ ] 2. Hanafee W, Weiner M. Transjugular percutaneous cholangiography. Radiology 1967;88:35–39. [ ] 3. Richter GM, Palmaz JC, Noeldge G. Intrahepatic stent-assisted portosystemic shunt: a new nonoperative transjugular and percutaneous method. Radiologe 1989;29:406–411. [ ] 4. Laberge JM, Ring EJ, Gordon RL, et al. Creation of transjugular intrahepatic portosystemic shunt with the wallstent endoprosthesis: results in 100 patients. Radiology 1993;187:413–420. [ ] 5. Rossle M, Haag K, Ochs A, Sellinger M, Noldge G, Perarnau JM. The transjugular intrahepatic portosystemic stent-shunt procedure for variceal bleeding. N Engl J Med 1994;330:165-171. [ ] 6. Shiffman ML, Jeffers L, Hoofnalge JH, Tralka TS. The role of transjugular intrahepatica portosystemic shunt for treatment of portal hypertension and its complications: a conference sponsored by the National Digestive Diseases Advisory Board. Hepatology 1995;5:1591–1597. [ ] 7. Kisilevzky N. TIPS (transjugular intrahepatic portosystemic shunt) no controle das complicações da hipertensão portal. Experiência preliminar e revisão da literatura. GED 1999;18:7–18. [ ] 8. Haskal ZJ, Martin L, Cardella JF, et al. Quality improvement guidelines for transjugular intrahepatic portosystemic shunts. J Vasc Interv Radiol 2001;12:131–136. [ ] 9. Bilbao JI, Pueyo JC, Longo JM, et al. Interventional therapeutic techniques in Budd-Chiari syndrome. Cardiovasc Intervent Radiol 1997;20: 112–119. [ ] 10. Spencer EB, Cohen DT, Darcy MD. Safety and efficacy of transjugular intrahepatic portosystemic shunt creation for the treatment of hepatic hydrothorax. J Vasc Interv Radiol 2002;13:385–390. [ ] 11. Selim KM, Akriviadis EA, Zuckerman E, Chen D, Reynolds TB. Transjugular intrahepatic portosystemic shunt: a successful treatment for hepatopulmonary syndrome. Am J Gastroenterol 1998; 93:455–458. [ ] 12. Haskal ZJ, Scott M, Rubin RA, Cope C. Intestinal varices: treatment with the transjugular intrahepatic portosystemic shunt. Radiology 1994; 191:183–187. [ ] 13. Boyer TD. Transjugular intrahepatic portosystemic shunt: current status. Gastroenterology 2003; 124:1700–1710. [ ] 14. D'Amico G, Pagliaro L, Bosch J. The treatment of portal hypertension: a meta-analytic review. Hepatology 1995;22:332–353. [ ] 15. Papatheodoridis GV, Goulis J, Leandro G, Patch D, Burroughs AK. Transjugular intrahepatic portosystemic shunt compared with endoscopic treatment for prevention of variceal rebleeding: a meta-analysis. Hepatology 1999;30:612–622. [ ] 16.Deltenre P, Mathurin P, Dharancy S, et al. Transjugular intrahepatic portosystemic shunt in refractory ascites: a meta-analysis. Liver Int 2005;25: 349–356. [ ] 17. Ferral H, Patel NH. Selection criteria for patients undergoing transjugular intrahepatic portosystemic shunt procedures: current status. J Vasc Interv Radiol 2005;16:449–455. [ ] 18. Chalasani N, Kahi C, Francois F, et al. Improved patient survival after acute variceal bleeding: a multicenter, cohort study. Am J Gastroenterol 2003;98:653–659. [ ] 19. Azoulay D, Castaing D, Majno P, et al. Salvage transjugular intrahepatic portosystemic shunt for uncontrolled variceal bleeding in patients with decompensated cirrhosis. J Hepatol 2001;35: 590–597. [ ] 20. Encarnacion CE, Palmaz JC, Rivera FJ, et al. Transjugular intrahepatic portosystemic shunt placement for variceal bleeding: predictors of mortality. J Vasc Interv Radiol 1995;6:687–694. [ ] 21. Coldwell DM, Ring EJ, Rees CR, et al. Multicenter investigation of the role of transjugular intrahepatic portosystemic shunt in management of portal hypertension. Radiology 1995;196:335–340. [ ] 22. Malinchoc M, Kamath PS, Gordon FD, Peine CJ, Rank J, ter Borg PC. A model to predict poor survival in patients undergoing transjugular intrahepatic portosystemic shunts. Hepatology 2000; 31:864–871. [ ] 23. Kamath PS, Wiesner RH, Malinchoc M, et al. A model to predict survival in patients with end-stage liver disease. Hepatology 2001;33:464–470. [ ] 24. Bilbao JI, Quiroga J, Herrero JI, Benito A. Transjugular intrahepatic portosystemic shunt (TIPS): current status and future possibilities. Cardiovasc Intervent Radiol 2002;25:251–269. [ ] 25. Tripathi D, Helmy A, Macbeth K, et al. Ten years' follow-up of 472 patients following transjugular intrahepatic portosystemic stent-shunt insertion at a single centre. Eur J Gastroenterol Hepatol 2004;16:9–18. [ ] 26. Darcy MD, Sterling KM. Comparison of portal vein anatomy and bony anatomic landmarks. Radiology 1996;200:3, 707–710. [ ] 27. Shultz SR, Laberge JM, Gordon RL, Warren RS. Anatomy of the portal vein bifurcation: intra- versus extrahepatic location – implications for transjugular intrahepatic portosystemic shunt. J Vasc Interv Radiol 1994;5:457–459. [ ] 28. Uflacker R, Rechiert P, D'Albuquerque LC, Silva A. Liver anatomy applied to the placement of transjugular intrahepatic portosystemic shunt. Radiology 1994;191:705–712. [ ] 29. Krajina A, Lojik M, Chovanec V, Raupach J, Hulek P. Wedged hepatic venography for targeting the portal vein during TIPS: comparison of carbon dioxide and iodinated contrast agents. Cardiovasc Intervent Radiol 2002;25:171–175. [ ] 30. Rossle M, Siegersterrer V, Olschewski M, Ochs A, Berger E, Haag K. How much reduction in portal pressure is necessary to prevent variceal rebleeding? A longitudinal study in 225 patients with transjugular intrahepatic portosystemic shunts. Am J Gastroenterol 2001;96:3379–3383. [ ] 31. Casado M, Bosch J, Garcia-Pagan JC, et al. Clinical events after transjugular intrahepatic portosystemic shunt: correlation with hemodynamic findings. Gastroenterology 1998;114:1296–1303. [ ] 32 Barton RE, Rosch J, Saxon RR, Lakin PC, Petersen BD, Keller FS. TIPS: short- and long-term results: a survey of 1750 patients. Semin Interv Radiol 1995;12:364–367. [ ] 33. Sanyal AJ, Freedman AM, Shiffman ML, Purdum PP, Liketic VA, Cheathman AK. Portosystemic encephalophathy after transjugular intrahepatic portosystemic shunt: results of a prospective controlled study. Hepatology 1994;20:46–55. [ ] 34. Somberg KA, Riegler JL, Laberge JM, et al. Hepatic encephalophaty after transjugular intrahepatic portosystemic shunt: incidence and risk factors. Am J Gastroenterol 1995;90:549–555. [ ] 35. Haskal ZJ, Midlebrook MR. Creation of a stenotic stent to reduce transjugular intrahepatic portosystemic shunt flow. J Vasc Interv Radiol 1994;5: 827–830. [ ] 36. Hauenstein KH, Haag K, Ochs A, Langer M, Rossle M. Reducing stent for TIPS-induced refractory hepatic encephalophaty and livr failure. Radiology 1994;194:175–179. [ ] 37. Kerlan R, LaBerge JM, Baker E, Ring EJ. Successful reversal of hepatic encephalopathy by intentional occlusion of TIPS. SCVIR Proceedings 1995;242. [ ] 38. Somberg KA. Transjugular intrahepatic portosystemic shunt for refractory ascites: shunt diameter-optimizing risks and benefits. Hepatology 1997; 25:1, 254–255. [ ] 39. Haskal ZJ, Ring EJ, LaBerge JM, et al. Role of parallel transjugular intrahepatic portosystemic shunt in patients with persistent portal hypertension. Radiology 1992;185:813–817. [ ] 40. Haskal Z, Pentecost MJ, Soulen MC, et al. Transjugular intrahepatic portosystemic shunt stenosis and revision: early and midterm results. AJR Am J Roentgenol 1994;163:439–444. [ ] 41. LaBerge JM, Somberg KA, Lake JR, et al. 2-year outcome following transjugular intrahepatic portosystemic shunt for variceal bleeding: results in 90 patients. Gastroenterology 1995;108:143–151. [ ] 42. Nazarian GK, Ferral H, Castaneda-Zuniga WR, et al. Development of stenoses in transjugular intrahepatic portosystemic shunt. Radiology 1994; 192:231–234. [ ] 43. Saxon RS, Mendel-Hartvig J, Corless CL. Bile duct injury as a major cause of stenosis and occlusion in transjugular intrahepatic portosystemic shunts: comparative histopathologic analysis in humans and swine. J Vasc Interv Radiol 1996;7: 487–497. [ ] 44. Sterling KM, Darcy MD. Stenosis of transjugular intrahepatic portosystemic shunt: presentation and management. AJR Am J Roentgenol 1997; 168:239–244. [ ] 45. LaBerge JM, Ferrell LD, Ring EJ, Gordon RL. Histopathologic study of stenotic and occluded transjugular intrahepatic portosystemic shunts. J Vasc Interv Radiol 1993;4:779–786. [ ] 46. Saxon RR, Ross PL, Mendel-Hartvig J. Transjugular intrahepatic portosystemic shunt parency and the importance of stenosis location in the development of recurrent symptoms. Radiology 1998;207:683–693. [ ] 47. Charon JP, Alaeddin FH, Pimpalwar SA, et al. Results of a retrospective multicenter trial of the Viatorr expanded polytetrafluoroethylene-covered stent-graft for transjugular intrahepatic portosystemic shunt creation. J Vasc Interv Radiol 2004;15:1219–1230. [ ] 48. Rossi P, Salvatori FM, Fanelli F, et al. Polytetrafluoroethylene-covered nitinol stent-graft for transjugular intrahepatic portosystemic shunt creation: 3-year experience. Radiology 2004;231: 820–830. [ ] 49. Hausegger KA, Karnel F, Georgieva B, et al. Transjugular intrahepatic portosystemic shunt creation with the Viatorr expanded polytetrafluoroethylene-covered stent-graft. J Vasc Interv Radiol 2004;15:239–248. [ ] 50. Bureau C, Garcia-Pagan JC, Otal P, et al. Improved clinical outcome using polytetrafluoroethylene-coated stents for TIPS: results of a randomized study. Gastroenterology 2004;126:469–475. [ ]
Recebido para publicação em 7/12/2005.
* Trabalho realizado no Serviço de Radiologia Intervencionista do Hospital Santa Catarina, São Paulo, SP. |
|
Av. Paulista, 37 - 7° andar - Conj. 71 - CEP 01311-902 - São Paulo - SP - Brazil - Phone: (11) 3372-4544 - Fax: (11) 3372-4554