Radiologia Brasileira - Publicação Científica Oficial do Colégio Brasileiro de Radiologia
AMB - Associação Médica Brasileira CNA - Comissão Nacional de Acreditação
 Ahead of Print
Ahead of Print
|
ENSAIO ICONOGRÁFICO
|
|
|
|
|
Autho(rs): Bruno Jucá Ribeiro1,a; Aldo Maurici Araújo Alves1,b; Rafael Santiago de Oliveira1,b; Fernanda Velloni1,d; Giuseppe D'Ippolito1,e |
|
|
Descritores: Doença iatrogênica; Vias biliares; Ressonância magnética; Meios de contraste. |
|
|
Resumo: INTRODUÇÃO
As lesões iatrogênicas das vias biliares resultantes da manipulação cirúrgica são relativamente comuns e aumentam as taxas de morbimortalidade(1). As complicações biliares, entre as quais a fístula e a estenose, podem ocorrer após colecistectomia em até 0,6% dos casos(2). Além disso, o paciente submetido a anastomose biliodigestiva apresenta maior incidência de complicações (por exemplo: colangites e cálculos), que são estimadas entre 10% e 30% dos pacientes(3,4). Exames laboratoriais ou de imagem podem ser utilizados para avaliar o paciente com suspeita de lesão iatrogênica da via biliar. Os estudos laboratoriais, notadamente a quantificação de fosfatase alcalina e da gama-glutamil transferase, são sensíveis, porém pouco específicos, na caracterização das complicações(5). A ultrassonografia (US) e a tomografia computadorizada (TC), como regra, são limitadas em fornecer o detalhamento necessário para definir a terapêutica adequada, restringindo-se à detecção de dilatações das vias biliares e coleções peri-hepáticas(1). A colangiopancreatografia endoscópica retrógrada (CPRE) e a colangiografia intraoperatória possuem como principais desvantagens a invasividade, a dificuldade em acessar a via biliar na presença de derivação biliodigestiva pela da CPRE e o elevado risco de complicações, tais como sangramento endoluminal e sepse, além da própria dificuldade de realizar o acompanhamento evolutivo(5). Por essas razões, a colangiografia por ressonância magnética (CRM) se estabeleceu como um método não invasivo e eficaz na detecção de complicações pós-cirúrgicas. Por meio da CRM ponderada em T2 (CRM-T2) é possível caracterizar estenoses e dilatações das vias biliares, porém, informações funcionais relacionadas a excreção e fluxo biliar não podem ser avaliadas, limitando a diferenciação da dilatação leve não obstrutiva da obstrutiva, e caracterização de lesões nos casos sem dilatação(6,7). A CRM ponderada em T1 com contraste hepato-específico (Gd-EOB-DTPA ou ácido gadoxético), também conhecida como CRM funcional (CRM-F), é uma técnica emergente que já se mostrou útil em delinear a anatomia da árvore biliar préoperatória e pós-operatória, bem como em detectar e caracterizar doenças biliares e complicações cirúrgicas, entre elas: cálculos intraductais, estenoses, fístulas e cistos biliares(8,9). Além disso, é capaz de fornecer informação funcional, cuja utilidade reside em graduar as estenoses biliares, avaliar a dinâmica do fluxo biliar e estimar a função hepática segmentar(10). Vários estudos já demonstraram a utilidade da CRM-F baseada nas informações da dinâmica do fluxo biliar, alguns inclusive com maiores taxas de acurácia na detecção das lesões pós-cirúrgicas quando comparados à CRM-T2(1). O objetivo deste ensaio é apresentar a nossa experiência com a CRM-F no contexto do paciente com suspeita de complicações pós-cirúrgicas das vias biliares. FARMACOCINÉTICA E PROTOCOLO DE EXAME O ácido gadoxético, ou contraste hepatoespecífico, é um contraste iônico utilizado em RM, composto por gadolínio e etoxibenzil-dietilenotriamina-pentacético (Gd- EOB-DTPA) (Primovist; Bayer Schering Pharma, Berlim, Alemanha). Além das propriedades extracelulares próprias do componente DTPA (que permitem obter fases arterial, portal e de transição), esse meio de contraste possui propriedades lipofílicas fornecidas pelo componente EOB, que permitem a captação progressiva do ácido gadoxético pelos hepatócitos normofuncionantes em até 50% da dose injetada. Durante a fase hepatobiliar, que ocorre em média entre 10 e 20 minutos após a injeção em indivíduos saudáveis, observa-se a excreção do meio de contraste nos ductos biliares, que se traduz em contrastação da árvore biliar nas sequências ponderadas em T1(10,11). A meia-vida do ácido gadoxético é em torno de 2 horas, o pico de acúmulo no hepatócito ocorre entre 20 e 40 minutos e o início da concentração hepatocítica e a excreção biliar ocorrem após 3 minutos e 10 minutos, respectivamente (Figura 1). Níveis elevados de bilirrubina (> 3 mg/dL) e ferritina ou disfunção hepática podem reduzir a captação do meio de contraste no fígado e, consequentemente, retardar ou reduzir a excreção biliar (Figura 2). Dessa forma, podem ser necessárias aquisições tardias (20 a 180 minutos, na nossa experiência) ou dose dupla do meio de contraste para se conseguir a adequada contrastação da árvore biliar(10,11). 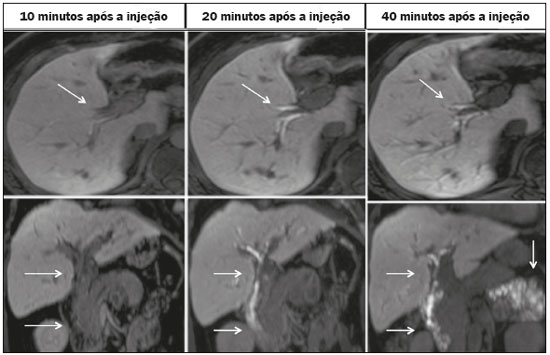 Figura 1. Representação do tempo normal de excreção de contraste (Gd- EOB-DTPA) pela via biliar na CRM-F: 10, 20 e 40 minutos após a injeção. 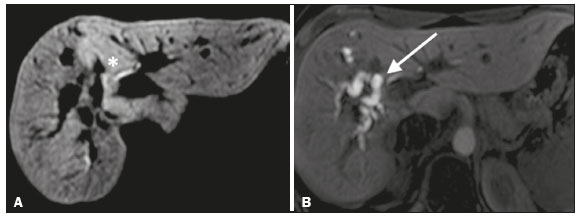 Figura 2. Estenose da via biliar intrahepática após colecistectomia. As imagens axiais ponderadas em T1 da CRM-F com 20 minutos (A) e 4 horas (B) após a injeção de Gd-EOB-DTPA demonstram dilatação moderada da via biliar direita causada por estenose no plano do ducto biliar direito (seta em B). Há uma maior concentração do meio de contraste pelo parênquima do lobo esquerdo (asterisco em A), quando comparado ao lobo hepático direito, onde há um retardo na contrastação das vias biliares (B). Foram considerados os diagnósticos de lesão térmica ou ligadura do ducto biliar. A CRM-F consiste em sequências ponderadas em T1 tridimensionais, com saturação de gordura, e aquisições na fase hepatobiliar adquiridas com 10, 20 e 40 minutos após a injeção do meio de contraste, nos planos axial e coronal. Eventualmente, podem ser necessárias aquisições até 824 horas. Os exames no nosso serviço têm sido realizados em aparelhos de RM operando em campo de 3T (Achieva 3.0 T TX; Philips Health Care System, Best, Holanda / Skyra 3.0 T; Siemens Healthcare, Erlangen, Alemanha), com os respectivos parâmetros técnicos na fase hepatobiliar: TR: 1.83/6.0 ms; TE: 3.89/2.46 ms; espessura: 3/3mm; flip angle: 30°/30°; duração: 18/18 s; matriz: 256 × 134/256 × 128. Os exames de CRM-F normalmente são complementados com as sequências tradicionais de abdome superior e CRM-T2. INDICAÇÕES Estenose A CRM-T2 é limitada para diferenciar um leve afilamento patente e esperado no plano da anastomose biliar, sem significado patológico, de uma estenose clinicamente significativa. Na CRM-F, o ácido gadoxético proporciona informação funcional da excreção biliar, de tal forma que o retardo ou a ausência de progressão do meio de contraste no local suspeito são importantes marcadores de estenose significativa. Na nossa experiência, assim como em relatos da literatura, o tempo de enchimento da via biliar foi diretamente proporcional ao grau de estenose, sendo por vezes necessárias aquisições em até 180 minutos após a injeção do meio de contraste (Figura 3). O raciocínio oposto pode ser usado para afastar com segurança essa complicação, ou seja, a progressão do meio de contraste pelo afilamento em um tempo considerado fisiológico (< 20 min) sugere que o estreitamento seja mais provavelmente desprovido de significado clínico (Figuras 4 e 5)(1,10). 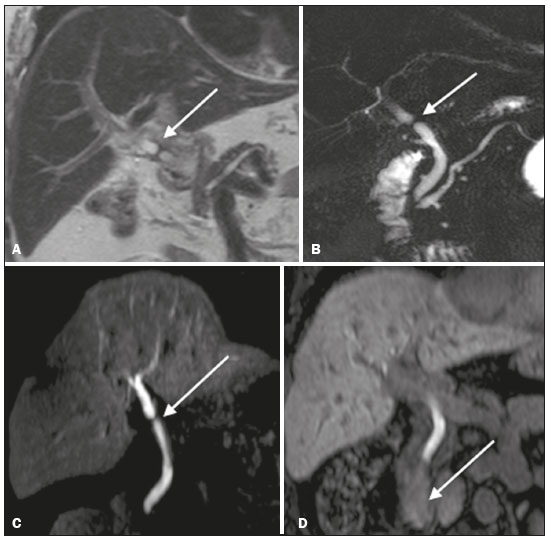 Figura 3. Estenose da anastomose biliar após transplante hepático. Coronal T2 (A) e T1 CRM (B): estenose da anastomose biliar com dilatação leve da árvore biliar intra-hepática. Coronal CRM-F 40 minutos (C,D): estenose (C) e retardo na progressão de contraste para o arco duodenal (D). Estenose patente com retardo na progressão do contraste pela via biliar. 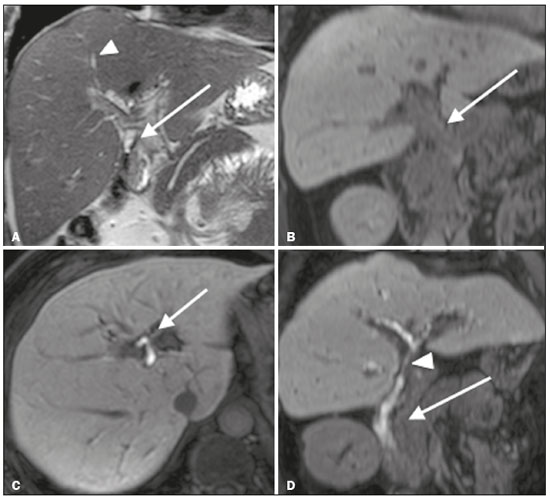 Figura 4. Avaliação da derivação biliodigestiva (após colecistectomia complicada). Coronal T2W (A), axial (C) e coronal (B,D) T1W CRM-F: derivação biliodigestiva e dilatação leve da via biliar intra-hepática 10 minutos após a injeção do meio de contraste (seta e cabeça de seta, respectivamente, em A), e atraso da excreção de contraste (B), observado apenas com 20 minutos após a injeção do meio de contraste (C,D). Estenose patente da anastomose biliodigestiva com retardo na excreção biliar. 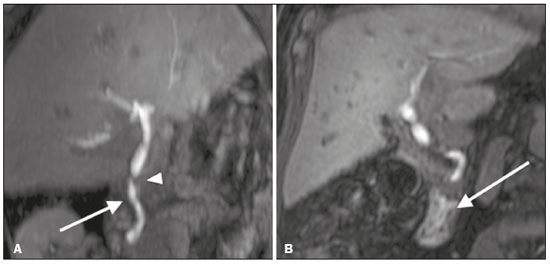 Figura 5. Estenose da anastomose biliar após transplante hepático. CRM-F coronal T1 (A,B) com progressão normal do meio de contraste na via biliar distal (seta em A) e no arco duodenal (seta em B). A anastomose permanece patente, apesar do estreitamento no plano da anastomose (cabeça de seta). Fístula biliar Coleções fluidas próximas ao leito cirúrgico, principalmente no contexto de cirurgias de grande porte, são achados comuns e muitas vezes irrelevantes. Entretanto, em situações em que a via biliar tenha sido manipulada, a possibilidade de fístula biliar surge como uma alarmante preocupação. A CRM-T2 detecta com precisão as coleções no leito cirúrgico, sendo, porém, limitada para identificar comunicação com a árvore biliar, por apresentar o mesmo elevado sinal nas imagens ponderadas em T2. A CRM-F permite identificar não somente o local da fístula biliar, mas também caracterizar o extravasamento do meio de contraste para o interior da coleção, achados inequívocos para o diagnóstico dessa complicação (Figura 6). Dessa forma, a CRM-F fornece informações complementares à CRM-T2, melhorando a identificação e localização das fístulas biliares(12,13). 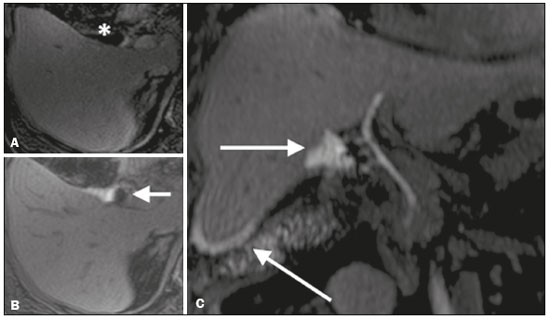 Figura 6. Fístula biliar após colecistectomia. Axial T1 pré-contraste (A): sem achados suspeitos para lesão na via biliar (asterisco). CRM-F axial (B) e coronal (C), 10 minutos após a injeção de Gd-EOB-DTPA, demonstram o extravasamento do contraste do ducto biliar direito para a cavidade abdominal (setas), o que é compatível com fístula biliar. CONCLUSÕES A CRM-F vem se mostrando uma ferramenta promissora na caracterização das estenoses e fístulas biliares, e parte dessa habilidade se deve às informações da dinâmica do fluxo biliar. Como restrições podemos citar a excreção limitada ou insuficiente do meio de contraste hepatoespecífico em pacientes com disfunção hepática e o tempo mais prolongado do exame. Ainda assim, a CRM-F vem se estabelecendo como um importante complemento às sequências ponderadas em T2, ao aumentar a acurácia na detecção de complicações após a manipulação cirúrgica das vias biliares. REFERÊNCIAS 1. Salvolini L, Urbinati C, Valeri G, et al. Contrast-enhanced MR cholangiography (MRCP) with GD-EOB-DTPA in evaluating biliary complications after surgery. Radiol Med. 2012;117:35468. 2. Sicklick JK, Camp MS, Lillemoe KD, et al. Surgical management of bile duct injuries sustained during laparoscopic cholecystectomy: perioperative results in 200 patients. Ann Surg. 2005;241:78692. 3. Nealon WH, Urrutia F. Long-term follow-up after bilioenteric anastomosis for benign bile duct stricture. Ann Surg. 1996;223:63948. 4. Gruessner RWG, Benedetti E. Living donor organ transplantation. New York, NY: McGraw Hill; 2008. 5. Polistina FA, Frego M, Bisello M, et al. Accuracy of magnetic resonance cholangiography compared to operative endoscopy in detecting biliary stones, a single center experience and review of literature. World J Radiol. 2015;7:708. 6. Kandasamy D, Sharma R, Seith Bhalla A, et al. MR evaluation of biliary-enteric anastomotic stricture: does contrast-enhanced T1W MRC provide additional information? Clin Res Hepatol Gastroenterol. 2011;35:56371. 7. Zurstrassen CE, Bitencourt AGV, Guimaraes MD, et al. Percutaneous stent placement for the treatment of malignant biliary obstruction: nitinol versus elgiloy stents. Radiol Bras. 2017;50:97102. 8. Salvadori PS, Torres US, D'Ippolito G, et al. Contrast-enhanced magnetic resonance cholangiography with gadoxetic-acid-disodium for the detection of biliary-cyst communication in Caroli disease. Gastroenterol Hepatol. 2016;39:66970. 9. Zattar-Ramos LC, Bezerra RO, Siqueira LTB, et al. Hepatocytespecific contrast agent-enhanced magnetic resonance cholangiography: perioperative evaluation of the biliary tree. Radiol Bras. 2017;50:38994. 10. Boraschi P, Donati F. Biliary-enteric anastomoses: spectrum of findings on Gd-EOB-DTPA-enhanced MR cholangiography. Abdom Imaging. 2013;38:13519. 11. D'Ippolito G. The role of MRI using liver-specific contrast agent in the assessment of focal liver lesion. Radiol Bras. 2014;47(5):viiviii. 12. Kantarcı M, Pirimoglu B, Karabulut N, et al. Non-invasive detection of biliary leaks using Gd-EOB-DTPA-enhanced MR cholangiography: comparison with T2-weighted MR cholangiography. Eur Radiol. 2013;23:271322. 13. Ribeiro KCP, Guimarães JPO, Aidar LB, et al. Hemobilia in a patient with arteriobiliary fistula after liver contusion. Radiol Bras. 2018;51:4134. 1. Escola Paulista de Medicina da Universidade Federal de São Paulo (EPM-Unifesp), São Paulo, SP, Brasil a. https://orcid.org/0000-0002-6947-1375 b. https://orcid.org/0000-0001-7310-5709 c. https://orcid.org/0000-0003-0838-3731 d. https://orcid.org/0000-0002-2019-7918 e. https://orcid.org/0000-0002-2701-1928 Correspondência: Dr. Bruno Jucá Ribeiro EPM-Unifesp Departamento de Diagnóstico por Imagem Rua Napoleão de Barros, 800, Vila Clementino São Paulo, SP, Brasil, 04024-002 E-mail: brunojucar123@gmail.com Recebido para publicação em 6/8/2018. Aceito, após revisão, em 13/9/2018. |
|
Av. Paulista, 37 - 7° andar - Conj. 71 - CEP 01311-902 - São Paulo - SP - Brazil - Phone: (11) 3372-4544 - Fax: (11) 3372-4554