Radiologia Brasileira - Publicação Científica Oficial do Colégio Brasileiro de Radiologia
AMB - Associação Médica Brasileira CNA - Comissão Nacional de Acreditação
 Ahead of Print
Ahead of Print
|
ARTIGO DE REVISÃO
|
|
|
|
|
Autho(rs): Ivie Braga de Paula1; Adriene Moraes Campos2 |
|
|
Descritores: Derrame papilar; Mamografia; Ultrassonografia; Ressonância magnética. |
|
|
Resumo: INTRODUÇÃO
O derrame papilar é um sintoma muito frequente, correspondendo à terceira queixa mamária mais comum, depois de dor e massas palpáveis, com uma prevalência de 5% a 10%(1,2). Ele é considerado suspeito quando ocorre espontaneamente, quando é persistente, unilateral, sanguinolento ou serossanguinolento, e quando não está associado a gravidez ou lactação. Na maioria dos casos, o derrame papilar suspeito é causado por lesões benignas, como ectasia ductal (6% a 59%) e papiloma (35% a 56%)(3). O risco de lesão maligna subjacente não é negligenciável, variando entre 5% e 23%(2). A anamnese e o exame físico, com inspeção visual e palpação das mamas e das papilas, têm papel essencial na diferenciação entre derrames papilares fisiológicos e patológicos. Deve-se investigar a data aproximada de aparecimento do sintoma, sua duração e frequência, se o derrame é espontâneo, e sua quantidade. Além disso, é importante investigar a data da última gravidez, aleitamento recente, uso de medicamentos (anticoagulantes, neurolépticos), trauma e tabagismo, assim como o estado hormonal da paciente e os antecedentes pessoais e familiares de doenças da mama ou dos ovários. A inspeção visual idealmente deve ser feita com o auxílio de uma lâmpada ou lupa que permita distinguir entre os derrames papilares e os pseudoderrames, que são provenientes de lesões do complexo areolopapilar. Deve-se localizar o derrame papilar (uni ou multiorificial, uni ou bilateral) e avaliar a coloração do líquido, o que é mais bem efetuado colocando um pouco dele sobre uma gaze. Os derrames papilares fisiológicos, ou não suspeitos, possuem as seguintes características: são bilaterais, não espontâneos, antigos ou intermitentes, multiorificiais, de coloração láctea, verde ou escura. Por sua vez, os derrames unilaterais, uniorificiais, espontâneos, persistentes, serosos ou hemáticos devem ser considerados como patológicos e ser investigados por meio de exames de imagem. Para o exame citológico do material proveniente da superfície papilar, a secreção pode ser colocada em lâmina seca (no caso de ser usado o método Giemsa) ou em lâmina fixada em álcool (no caso de ser usado o método de Papanicolau), sendo importante citar a cor do líquido no pedido de exame. A citologia tem a vantagem de ser um método fácil de ser realizado e indolor, porém tem a desvantagem de ser um método com sensibilidade variável, com taxas de falso-negativo superiores a 50% em caso de lesão maligna(4). O derrame papilar em homens deve ser sempre considerado um achado suspeito, dado que a incidência de carcinoma, neste contexto, é de cerca de 23%(5). Ele ocorre em 25% dos casos de carcinoma ductal invasor e a presença de linfonodomegalia axilar é comum no momento do diagnóstico. Calcificações suspeitas ocorrem em 13% a 30% dos casos(6). Os métodos de imagem têm papel fundamental na avaliação da paciente com derrame papilar, uma vez que permitem a realização de biópsias guiadas. Tais biópsias têm sido cada vez mais precisas e capazes de fornecer ao patologista maior quantidade de tecido para avaliação. Caso seja encontrado papiloma na biópsia de fragmento, a maioria das instituições realiza a excisão cirúrgica, em razão da sua associação com carcinoma em alguns casos(7). Estudos mais recentes mostram que pode ser feito o acompanhamento clínico e pelos métodos de imagem, sem a necessidade de cirurgia, em casos de papiloma único, intraductal, central e pequeno, diagnosticado por meio de mamotomia, e que não apresenta atipias celulares no anatomopatológico(8,9). AVALIAÇÃO PELOS MÉTODOS DE IMAGEM Mamografia A literatura radiológica brasileira vem, recentemente, enfatizando a importância da mamografia no aprimoramento do diagnóstico mamário(1015). A mamografia deve ser sempre o primeiro exame a ser solicitado, porém, ela apresenta baixa sensibilidade nos casos de derrame papilar, variando de 20% a 25%(16), pelo fato de serem as lesões geralmente retroareolares, pequenas, intraductais e não calcificadas(17). Assim, uma mamografia negativa não exclui a possibilidade de uma doença subjacente. O principal achado mamográfico são as calcificações. Elas podem ser tipicamente benignas, tais como calcificações com aspecto de casca de ovo, que podem estar associadas a papiloma, ou calcificações em bastão, usualmente associadas a ectasia ductal. Elas também podem ter morfologia e distribuição suspeitas, como as calcificações pleomórficas e o padrão de distribuição segmentar ou linear(1) (Figura 1). A mamografia também pode demonstrar a presença de nódulos, assimetria focal e ectasia ductal. 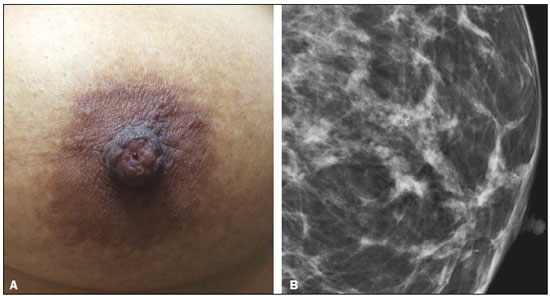 Figura 1. A: Foto do complexo areolopapilar de paciente portadora de carcinoma ductal in situ grau II sólido, cribriforme e com necrose, apresentando derrame papilar uniorificial sanguinolento. B: Mamografia, magnificação em incidência mediolateral oblíqua demonstrando calcificações pleomórficas finas com distribuição segmentar na região retroareolar da mama esquerda. Em casos de derrame papilar, deve-se ter mais atenção à região retroareolar. Não existem protocolos na literatura de análise específica da região, mas em caso de dúvida, deve ser feita uma compressão localizada ou magnificação. Ultrassonografia A ultrassonografia (US) deve ser sempre realizada em casos de derrame papilar, mesmo que a mamografia já se mostre alterada(5). Em estudo de Bahl et al., na detecção de carcinoma ductal in situ (CDIS) e carcinoma invasor em pacientes com derrame papilar suspeito, a US apresentou sensibilidade de 56% e especificidade de 75%(17). A técnica apropriada inclui uso de transdutores de alta frequência, gel aquecido e controle da temperatura ambiente para evitar contratura da musculatura da papila e aréola. Devem ser utilizadas manobras que melhorem a visualização das regiões intrapapilar e subareolar, como angulação do transdutor e observação ao longo do eixo do ducto, com discreta compressão periférica(18). Um dos principais achados na US é a ectasia ductal, considerada como calibre ductal maior que 3 mm. Nas pacientes com derrame papilar suspeito, o achado de ectasia ductal focal com conteúdo anecoide deve ser biopsiado, uma vez que este achado pode ser encontrado em metade dos casos de papiloma e em 14% dos casos de CDIS(1,19). A localização periférica da ectasia ductal focal, a irregularidade das margens do ducto, o espessamento da parede ductal e a presença de tecido hipoecoico adjacente são características que podem indicar malignidade(20). Na presença de derrame papilar patológico, nódulos e áreas de sombra acústica em localização subareolar devem ser classificados como BI-RADS 4 ou 5. Tais áreas podem estar relacionadas a CDIS, cujo diagnóstico ultrassonográfico é difícil, com falso-negativos em torno de 80%(1). O Doppler pode ajudar na diferenciação entre ducto com secreção espessa e nódulo intraductal, demonstrando vascularização no interior deste último(17). A causa mais comum de nódulo neste sítio é o papiloma único, localizado a poucos centímetros da papila, usualmente resultando em obstrução ductal (Figura 2). As características que aumentam o risco de malignidade são a idade da paciente acima de 50 anos, nódulo maior que 1 cm e distância da papila maior que 3 cm(20). 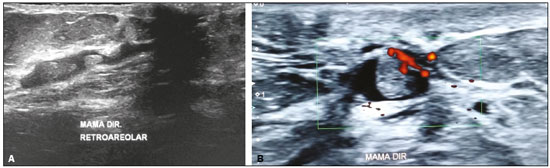 Figura 2. A: US mostrando nódulos intraductais. B: Nódulo intraductal com vascularização interna ao Doppler. A US é muito importante na avaliação second-look após o exame de ressonância magnética (RM), uma vez que é mais simples realizar a biópsia e a marcação pré-cirúrgica das lesões guiadas por ela. Os seus resultados são melhores na detecção de nódulo, comparativamente ao realce não nodular(21) (Figura 3). 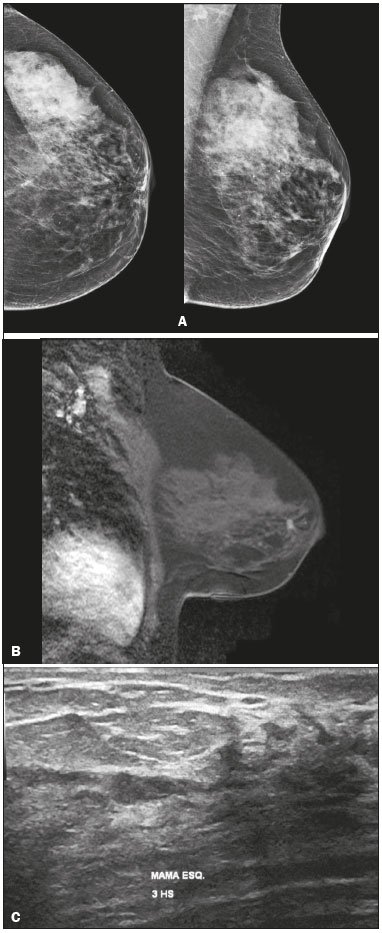 Figura 3. Paciente de 64 anos com derrame papilar sanguinolento à esquerda. A: Mamografia em incidências craniocaudal e mediolateral oblíqua mostrando assimetria focal retroareolar. B: RM, imagem ponderada em T1 com supressão de gordura, dois minutos após a injeção intravenosa de gadolínio, mostrando nódulo não circunscrito na mesma localização. C: US second-look demonstrando nódulo hipoecoico intraductal em correspondência com o achado da mamografia e da RM. Biópsia de fragmento demonstrou papiloma intraductal sem atipias. RM Existem poucos estudos sobre o uso da RM em casos de derrame papilar. Segundo a European Society of Breast Cancer Specialists, é uma indicação emergente, ainda sem validação, sendo os estudos com nível de evidência C. Na prática clínica, a RM pode ser realizada em caso de derrame papilar suspeito em que a mamografia e a US mostraram-se normais(22). A RM tem bom valor preditivo negativo, em torno de 90%, sendo os falso-negativos representados pelos CDISs de baixo grau ou muito pequenos(2224). A avaliação da localização e da extensão da lesão por RM é melhor comparativamente à mamografia e à US(1,25). A RM também pode identificar lesões que inicialmente passaram despercebidas e que poderão ser vistas na US ou na mamografia second-look, especialmente na região retroareolar (Figura 4). 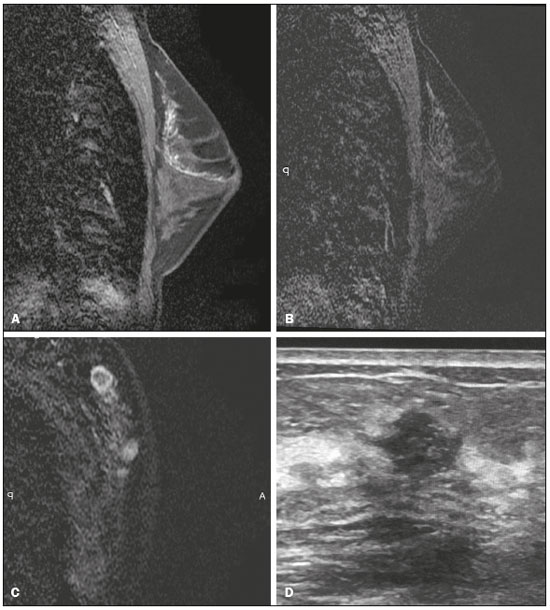 Figura 4. Paciente de 44 anos apresentando derrame papilar suspeito. Mamografia mostrou mamas densas com assimetria focal no quadrante superolateral esquerdo. US de outro serviço sem alterações. A: RM, corte sagital ponderado em T1 com supressão de gordura mostrando ectasia ductal com conteúdo hemorrágico/hiperproteico no quadrante superolateral esquerdo. B: RM, subtração digital de imagens dois minutos após a administração intravenosa do meio de contraste mostrando realce não nodular com distribuição segmentar e padrão de realce interno heterogêneo no quadrante superolateral esquerdo. C: RM, subtração digital de imagens após contraste identificando nódulo não circunscrito com realce anelar no quadrante superolateral esquerdo, em correspondência com o achado mamográfico. D: US second- look mostrando nódulo não circunscrito no quadrante superolateral esquerdo em correspondência com o achado da RM. Biópsia de fragmento demonstrou carcinoma mucinoso invasivo grau II. O principal achado da RM nas pacientes com derrame papilar suspeito é o realce não nodular. Em estudo de 47 pacientes com esta queixa, os achados mais frequentes em lesão maligna foram o realce não nodular com distribuição segmentar (59%), o padrão de realce interno heterogêneo (57%) e a curva de realce do tipo platô (40%)(26). O conteúdo hiperproteico ou hemorrágico intraductal pode ter hipersinal nas sequências ponderadas em T1, simulando realce com distribuição linear ou segmentar. Para diferenciar os dois achados, devem ser avaliadas as sequências pré-contraste e subtração digital das imagens. Na presença do sintoma, foco de realce pelo meio de contraste deve ser valorizado, pois pode corresponder a papiloma. As principais críticas à RM são o seu custo elevado, a detecção de imagens adicionais que podem gerar outros exames de controle ou biópsias não relacionadas à queixa clínica da paciente e a dificuldade de diferenciar se a lesão é intraductal ou não(25). Neste caso, é indispensável a realização da US second-look. Ductografia Por longo tempo a ductografia foi considerada o exame padrão para avaliação da descarga papilar. Estudo de Manganaro et al. comparou 53 pacientes com descarga unilateral que realizaram ductografia e RM e avaliou a capacidade de ambos os métodos de identificar doenças e distinguir entre lesões benignas e malignas. A RM mostrou maior sensibilidade (98%) em comparação com a ductografia (49%) para identificar a doença ductal e ambos os métodos apresentaram alta especificidade. A RM foi capaz não apenas de demonstrar a doença ductal, mas também demonstrou lesões no parênquima adjacente(27). DISCUSSÃO Embora o papel da RM no estudo do câncer de mama seja crescente(28,29), existem poucos estudos sobre o seu uso em casos de derrame papilar. Apesar da ausência de evidências científicas suficientes sobre o benefício do seu uso em pacientes com derrame papilar suspeito e mamografia e US normais, a maior parte dos autores recomenda realizar RM das mamas. Caso a RM encontre uma lesão suspeita, a US second-look já é rotina para tentar localizar o achado. Porém, caso a RM mostre realce não nodular com distribuição linear ou segmentar, em correspondência com o local do derrame papilar, a mamografia second-look com ampliação daquela região pode ser útil na pesquisa de calcificações suspeitas, permitindo a realização de biópsia estereotáxica. Não tendo sido encontrada nenhuma anormalidade, a biópsia do achado suspeito deve ser feita guiada por RM(1). Historicamente, a ressecção cirúrgica dos ductos terminais da mama era a regra para as pacientes com derrame papilar suspeito e mamografia, US e RM normais. Atualmente, tem sido demonstrado que o risco de lesão maligna é muito baixo nessas pacientes, principalmente se não existem outros sinais clínicos suspeitos. Além disso, quando existe alguma lesão maligna, trata-se de CDIS de baixo grau ou de tumores muito pequenos. A literatura mais recente recomenda que, em caso de paciente com derrame papilar com mamografia, US e RM normais, seja proposto acompanhamento semestral por dois anos, até a resolução espontânea do derrame, que ocorre em 81% dos casos(1,16,30). O protocolo de acompanhamento pode ser US e exame clínico semestrais e mamografia anual. Por outro lado, deve-se pensar em cirurgia para as pacientes com derrame papilar muito importante, causando desconforto, ou persistente por mais de dois anos(1). CONSIDERAÇÕES FINAIS A maioria dos derrames papilares suspeitos tem origem benigna, com risco de malignidade em torno de 5%, constituído principalmente de CDIS. Após avaliação clínica e exame físico, a investigação por imagem inicia-se com mamografia e US, com especial atenção para a região retroareolar, sendo a sensibilidade relatada de 20% a 25% para a mamografia e 65% a 85% para a US. A RM pode ser utilizada nos casos em que a mamografia e a US encontram-se normais, sendo seu uso baseado em sua alta sensibilidade para lesões papilares e para lesões malignas. O achado mais frequente na RM é o realce não nodular, sendo mais suspeito para malignidade quando apresentar distribuição segmentar e padrão de realce interno heterogêneo. Nos casos com achados suspeitos à RM, a mamografia ou a US second-look podem facilitar a biópsia das lesões. Nas pacientes com todos os exames de imagem normais, pode ser sugerido protocolo de acompanhamento clínico, mamográfico e ultrassonográfico, havendo resolução espontânea do derrame papilar em grande número de casos. REFERÊNCIAS 1. Lippa N, Hurtevent-Labrot G, Ferron S, et al. Les écoulements mamelonnaires. Journal de Radiologie Diagnostique et Interventionnelle. 2015;96:43450. 2. Chen L, Zhou WB, Zhao Y, et al. Bloody nipple discharge is a predictor of breast cancer risk: a meta-analysis. Breast Cancer Res Treat. 2012;132:914. 3. van Gelder L, Bisschops RH, Menke-Pluymers MB, et al. Magnetic resonance imaging in patients with unilateral bloody nipple discharge: useful when conventional diagnostic are negative? World J Surg. 2015;39:1846. 4. Das DK, Al-Ayadhi B, Ajrawi MY, et al. Cytodiagnosis of nipple discharge: a study of 602 samples from 484 cases. Diagn Cytopathol. 2001;25:2537. 5. Muñoz Carrasco R, Álvarez Benito M, Rivin del Campo E. Value of mammography and breast ultrasound in male patients with nipple discharge. Eur J Radiol. 2013;82:47884. 6. Lattin GE Jr, Jesinger RA, Mattu R, et al. From the radiologic pathology archives: diseases of the male breast: radiologic-pathologic correlation. Radiographics. 2013;33:46189. 7. Glenn ME, Throckmorton AD, Thomison JB 3rd, et al. Papillomas of the breast 15 mm or smaller: 4-year experience in a community- based dedicated breast imaging clinic. Ann Surg Oncol. 2015;22: 11339. 8. The American Society of Breast Surgeons. Consensus guideline on concordance assessment of image-guided breast biopsies and management of borderline or high-risk lesions. [cited 2017 Aug 25]. Available from: https://www.breastsurgeons.org/new_layout/about/statements/PDF_Statements/Concordance_and_High%20RiskLesions.pdf. 9. Kibil W, Hodorowicz-Zaniewska D, Popiela TJ, et al. Vacuum-assisted core biopsy in diagnosis and treatment of intraductal papillomas. Clin Breast Cancer. 2013;13:12932. 10. Freitas-Junior R, Rodrigues DCN, Corrêa RS, et al. Contribution of the Unified Health Care System to mammography screening in Brazil, 2013. Radiol Bras. 2016;49:30510. 11. Schwingel R, Almeida O, Ferreira TS. Fat necrosis associated with the use of oral anticoagulant therapy: atypical mammographic findings. Radiol Bras. 2016;49:26970. 12. Koch H. Mammography as a method for diagnosing breast cancer. Radiol Bras. 2016;49(6):vii. 13. Villar VCFL, De Seta MH, Andrade CLT, et al. Evolution of mammographic image quality in the state of Rio de Janeiro. Radiol Bras. 2015;48:8692. 14. Avelar MS, Almeida O, Alvares BR. Mammographic artifact leading to false-positive result. Radiol Bras. 2015;48:1989. 15. Paixão L, Oliveira BB, Viloria C, et al. Monte Carlo derivation of filtered tungsten anode X-ray spectra for dose computation in digital mammography. Radiol Bras. 2015;48:3637. 16. Ashfaq A, Senior D, Pockaj BA, et al. Validation study of a modern treatment algorithm for nipple discharge. Am J Surg. 2014;208;2227. 17. Bahl M, Baker JA, Greenup RA, et al. Diagnostic value of ultrasound in female patients with nipple discharge. AJR Am J Roentgenol. 2015;205:2038. 18. Da Costa D, Taddese A, Cure ML, et al. Common and unusual diseases of the nipple-areolar complex. Radiographics. 2007;27 Suppl 1:S6577. 19. Yang WT, Tse GMK. Sonographic, mammographic, and histopathologic correlation of symptomatic ductal carcinoma in situ. AJR Am J Roentgenol. 2004;182:10110. 20. Ferris-James DM, Iuanow E, Mehta TS, et al. Imaging approaches to diagnosis and management of common ductal abnormalities. Radiographics. 2012;32:100930. 21. Candelaria R, Fornage BD. Second-look US examination of MR-detected breast lesions. J Clin Ultrasound. 2011;39:11521. 22. Lorenzon M, Zuiani C, Linda A, et al. Magnetic resonance imaging in patients with nipple discharge: should we recommend it? Eur Radiol. 2011;21:899907. 23. Boisserie-Lacroix M, Adenet C, Trillaud H. Evaluation of suspicious nipple discharge with MRI: review of 50 cases. J Radiol. 2011;92:41220. 24. Morrogh M, Morris EA, Liberman L, et al. The predictive value of ductography and magnetic resonance imaging in the management of nipple discharge. Ann Surg Oncol. 2007;14:336977. 25. Eiada R, Chong J, Kulkarni S, et al. Papillary lesions of the breast: MRI, ultrasound, and mammographic appearances. AJR Am J Roentgenol. 2012;198:26471. 26. Tokuda Y, Kuriyama K, Nakamoto A, et al. Evaluation of suspicious nipple discharge by magnetic resonance mammography based on breast imaging reporting and data system magnetic resonance imaging descriptors. J Comput Assist Tomogr. 2009;33:5862. 27. Manganaro L, DAmbrosio I, Gigli S, et al. Breast MRI in patients with unilateral bloody and serous-bloody nipple discharge: a comparison with galactography. Biomed Res Int. 2015;2015:806368. 28. Almeida JRM, Gomes AB, Barros TP, et al. Predictive performance of BI-RADS magnetic resonance imaging descriptors in the context of suspicious (category 4) findings. Radiol Bras. 2016;49:13743. 29. Bitencourt AGV. Subdividing BI-RADS category 4 breast lesions observed on magnetic resonance imaging: is it feasible? Radiol Bras. 2016;49(3):v. 30. Sabel MS, Helvie MA, Breslin T, et al. Is duct excision still necessary for all cases of suspicious nipple discharge? Breast J. 2012; 18:15762. 1. Mestre, Membro Titular do Colégio Brasileiro de Radiologia e Diagnóstico por Imagem (CBR), Médica Radiologista da Conrad Diagnóstico por Imagem, Belo Horizonte, MG, Brasil 2. Membro Titular do Colégio Brasileiro de Radiologia e Diagnóstico por Imagem (CBR), Médica Radiologista da Conrad Diagnóstico por Imagem, Belo Horizonte, MG, Brasil Trabalho realizado na Conrad Diagnóstico por Imagem, Belo Horizonte, MG, Brasil. Endereço para correspondência: Dra. Ivie Braga de Paula Conrad Diagnóstico por Imagem Rua Rio Grande do Norte, 77, Santa Efigênia Belo Horizonte, MG, Brasil, 30130-130 E-mail: iviepaula@gmail.com Recebido para publicação em 15/6/2016. Aceito, após revisão, em 14/12/2016. |
|
Av. Paulista, 37 - 7° andar - Conj. 71 - CEP 01311-902 - São Paulo - SP - Brazil - Phone: (11) 3372-4544 - Fax: (11) 3372-4554